Конспект уроку з хімії для 8 класу на тему "Ковалентний полярний та неполярний зв’язок, йонний зв’язок"
Конспект уроку з хімії для 8 класу на тему "Ковалентний полярний та неполярний зв'язок, йонний зв'язок" розроблений за інтегральною технологією. Урок закріплення (розвиваюче диференційоване навчання). Містить цікаві завдання компетентісного характеру, дидактичну гру "Морський бій", посилання на інтерактивні вправи Learning.apps.
Урок № ____ 8 клас Дата ________
Тема: Ковалентний полярний та неполярний зв'язок, йонний зв'язок
Мета: вдосконалити знання про хімічні зв’язки у складних речовинах, вдосконалити вміння визначати вид хімічного зв’язку в типових випадках, полярність ковалентного зв'язку; використовувати поняття електронегативності для характеристики хімічних зв'язків; обґрунтовувати природу хімічних зв'язків; розвивати вміння записувати електронні та структурні формули речовин, визначати кількість валентних електронів, розвивати хімічну мову; виховувати наполегливість, комунікативність, дисциплінованість
Формування компетентностей:
Навчальної: формувати вміння здобувати інформацію, виділяти головне, уміння й бажання організовувати свою працю для досягнення успішного результату;
Комунікативної: формулювати власні твердження, висловлювати власну думку, доводити її на практиці, володіти словарним запасом, спілкуватися в колективі;
Соціальної: уміння адаптуватися і визначати особисті цілі, виконувати різні ролі в колективі;
Загальнокультурної: вміння аналізувати й оцінювати досягнення інших; виховувати культуру поведінки у суспільстві та культуру спілкування у колективі;
Інформаційної: вміння користуватися інформаційними джерелами для власного розвитку, опрацювання, систематизації та передачі інформації.
Тип уроку: закріплення (розвиваюче диференційоване навчання)
Методи: самостійна робота, робота у групах; прийоми: «Що у скриньці?», «німе кіно», гра «Морський бій»
Хід уроку
І. Організаційний етап
Доброго дня!
Перед початком роботи пропоную вам заручитися підтримкою своїх однокласників для цього доторкніться долонями одне до одного, посміхніться й побажайте добра та успіхів.
Ніколи не шкодуйте теплоти своєї душі, посмішки, доброго слова для інших людей.
ІІ. Оголошення теми та мети уроку
ІІІ. Самостійна робота
|
І варіант |
ІІ варіант |
|
1.Визначте тип зв’язку у речовинах. Складіть електронні і структурні формули їх будови. O2, PH3, Cl2, HBr |
1.Визначте тип зв’язку у речовинах. Складіть електронні і структурні формули їх будови. N2, H2S, NH3, H2 |
|
2. Дайте визначення поняттям:
|
2. Дайте визначення поняттям:
|
|
III варіант |
IV варіант |
|
1.Визначте тип зв’язку у речовинах. Складіть електронні і структурні формули їх будови. Br2, CH4, H2O, SiO2 |
1.Визначте тип зв’язку у речовинах. Складіть електронні і структурні формули їх будови. F2, HI, SiH4, CO2 |
|
2. Дайте визначення поняттям:
|
2. Дайте визначення поняттям:
|
IV. Навчаюча частина семінару
Казка природи не має кінця. Кожна людина впродовж життя встигає лише краєм ока зазирнути до її скарбниць, прочитати лише кілька рядків великої книги Природи. Але й людська цікавість - безмежна.
«ЩО У СКРИНЬЦІ?»
Ця речовина має йонний тип зв’язку. Перший атом має на останньому 4-му енергетичному рівні лише 1 електрон. А другий атом має 7 валентних електронів на 3-му енергетичному рівні. ∆χ= 3,0-0,8= 2,2 (КС1)
«Німе кіно»
Перегляньте відеоролик та вкажіть речовину про яку іде мова та тип хімічного зв’язку в ній.
Гра «Морський бій»
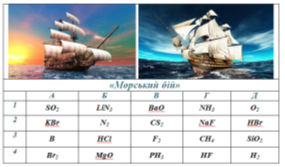
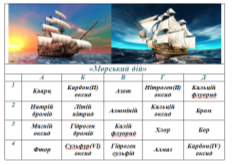
Робота у групах
- Хлор — жовто-зелений отруйний газ, потрапляючи в легені викликає задуху або опік легеневої тканини. В організмі людини в середньому міститься 95 г хлору, він потрібен для вироблення в шлунку соляної кислоти, яка сприяє травленню і знищенню хвороботворних бактерій. Хлор був одним з найперших хімічних отруйних речовин (він був застосований Німеччиною у Першій світовій війні під час битви при Іпрі в 1915 році).
- Запишіть молекулярну, електронну та структурну формулу даного газу;
- вкажіть тип зв’язку, тип кристалічної ґратки;
- передбачте, чи може дана речовина проводити електричний струм;
- запишіть схему утворення хімічного зв’язку у даній речовині.
- На глибині 500 м нижче рівня моря є так званий «блок» замороженого метану (СН4). Метан спливає з дна океану, і, через тиск і температуру, замерзає. У цьому крижаному «блоці» найчастіше «проживає» сімейство бактерій, які харчуються метаном. Бактеріями харчуються льодові червяки, яких зовсім недавно відкрили вчені. Маленькі рожеві черв’яки проводять все своє життя (всього два тижні) копаючи невеликі поглиблення в льоду метану, щоб отримати доступ до бактерій. Потім вони розмножуються і вмирають, залишивши своє потомство для продовження виду.
- Запишіть молекулярну, електронну та структурну формулу метану;
- вкажіть тип зв’язку, тип кристалічної ґратки;
- передбачте, чи може дана речовина розчинятися у воді.
- Існує клас так званих скляних губок, які будують свій скелет із скляних спікул, що є оптичними волокнами. Ці губки мають найрізноманітніші форми: трубки, вази, кошики, циліндри тощо. Їх скелет складається з силіцій(ІV) оксиду. Волокна губок досить міцні – вони не тріскаються і не ламаються як штучні оптичні волокна. Вони відмінно проводять світло бо мають незначну кількість йонів натрію, які покращують оптичні властивості.
- Запишіть молекулярну, електронну та структурну формулу силіцій(ІV) оксиду;
- вкажіть тип зв’язку, тип кристалічної ґратки;
- запишіть схему утворення хімічного зв’язку у даній речовині;
- передбачте твердість та температури кипіння і плавлення (високі чи низькі) даної речовини.
- Кальцій оксид називають негашеним вапном. При його взаємодії з водою (так званому гасінні) виділяється багато енергії, яка перетворює воду у водяну пару.
- Запишіть молекулярну формулу кальцій оксиду;
- вкажіть тип зв’язку, тип кристалічної ґратки;
- запишіть схему утворення хімічного зв’язку у даній речовині;
- передбачте твердість та температури кипіння і плавлення (високі чи низькі) даної речовини.
- Сльози людини містять сіль – натрій хлорид. Це встановив у 1791 році французький хімік Антуан Лавуазьє. Сльози також містять калій хлорид, кальцій, натрій карбонат і марганець.
- Запишіть молекулярні та електронні формули даних речовин;
- вкажіть тип зв’язку та тип кристалічної ґратки для кожної з речовин;
- запишіть схему утворення хімічного зв’язку у калій хлориді.
1. Визначте тип зв’язку у сполуках. Записати електронні та структурні формули речовин: PH3, H2S, NH3
2. Записати схему утворення хімічного зв’язку у молекулі калій броміду та гідроген йодиду
3. Вкажіть йон, який містить вдвічі менше електронів, ніж атом Кальцію
4. Вкажіть кількість електронів, яку приєднає атом Хлору при утворенні зв’язку з атомом Кальцію
V. Контролююча частина семінару
Тест «Перевір свої знання» - електронний посібник АБО За наявності Інтернету – вправи Learning.apps
Взаємоперевірка завдань
VІ. Підсумки уроку
VІІ. Домашнє завдання:
- Повторити §12-13 – повторити,
- № 4-5, с.66 - письмово
- Виконати вправи на сайті за посиланням
sites.google.com/site/himtown/himicni-igri 8 клас Обрії хімічних зв'язків
- Творча лабораторія с.62 або с. 66
Література:
- Навчальні програми для загальноосвітніх навчальних закладів: Хімія. 7-9 класи. – К.: Видавничий дім «Освіта», 2013.
- Хімія: підруч. для 8 кл. загальноосвіт. навч. закл./ Г.А.Лашевська. – Київ: Генеза. – 2016. – 216с.
- Данильченко В.Є., Фрадіна Н.В. Хімія. 8-9 класи: Навч.посібник. – Х: Країна мрійТМ, 2002. – 184с.
- Хімія. Комплексний довідник + профільний рівень: 3-тє вид./Укладачі: Гога С.Т., Ісаєнко Ю.В. – Х.: ФОП Співак В.Л., 2013. – 440с.
Інтернет-джерела:
- http://dovidka.biz.ua/tsikavi-fakti-pro-hlor/ Довідник цікавих фактів та корисних знань © dovidka.biz.ua)
- http://сikavо.com.ua
- http://shkolyar.in.ua
- www.origins.org.ua


про публікацію авторської розробки
Додати розробку
