конспект уроку "Загальні способи одержання оксидів, основ, кислот, солей"
1
Тема Загальні способи одержання
оксидів, основ, кислот, солей
Мета Ознайомити учнів із загальними способами одержання оксидів, кислот, основ, солей. Розвивати навички роботи з навчальною літературою. На прикладі одержання різних класів неорганічних сполук показати взаємозв’язок між будовою, властивостями та способами одержання цих речовин.
Обладнання та матеріали Періодична система хімічних елементів, опорна схема, ряд активності металів, навчальна таблиця.
Базові поняття й терміни оксиди, кислоти, основи, солі, валентність.
Тип уроку творчо-продуктивний.
Форма проведення урок-подорож-змагання
Методи та прийоми а) словесні:створення емоційного настрою, робота в групах, бесіда, рефлексія; б) практичні: робота з додатковими джерелами інформації; б) наочні: відео сюжет.
Міжпредметні зв’язки: математика, українська література.
Структура уроку
І. Організаційний етап ...........................................................................................5 хв
II. Перевірка домашнього завдання ...................................................................2-3хв
III. Актуалізація опорних знань учнів................................................................2-3хв
IV. Вивчення нового матеріалу ..........................................................................30 хв
1. Добування оксидів.
2. Добування кислот.
3. Добування основ.
4. Добування солей.
- 1. Буринська Н.М. §15 ст 86-89.
- Савчин М.М. Хімія. Робочий зошит
- О.В.Григорович Хімія 8 клас розш.календарне планув. ст.58-59.
- І.Ю.Старовойтова Усі уроки хімії 8клас м. Харків Видгрупа «Основа» 2008 ст.117-121
V. Узагальнення й систематизація знань учнів ..................................................5 хв
- Тестові завдання. Хімія. Вимірник навчальних досягнень 8 клас
- Ярошенко О.Г. § 21 ст. 98-101.
VI. Домашнє завдання ........................................................................................1-2 хв
1. Ярошенко О.Г. §21 ст. 98-101. № 1
2. Високий рівень – №4
VII. Підбиття підсумків уроку ...........................................................................1-2хв
ППЕРЕБІГ УРОКУ
I. Емоційне налаштування
Привітання з учнями:
В цьому класі усі друзі,
Я і ти, і ми, і всі.
Добрий день тому хто зліва,
Добрий день тому хто справа.
Посміхнись тому хто зліва,
Посміхнись тому хто справа.
Привітай того хто зліва,
Привітай того хто справа.
Тож почнемо наш урок.
Девіз уроку: «Будь завжди готовий допомогти товаришу»
Оголошення теми уроку, плану й основних цілей уроку.
Я б хотіла вас знову запросити до чарівної країни «Класи неорганічних сполук», де панує 4 королівства. Давайте згадаємо, які саме?
У нас вони зашифровані:
слитоки
сліо
сиокид
дксигіроди
Для того щоб наша подорож була цікава та захоплююча. Ми повинні зібрати багаж. А багажем є наші знання. Ото ж в путь!!!
Схема на обкладинці зошита (в кінці)
Хто може дати визначення цим класам?
Нашими цілями на сьогоднішньому уроці є:
Ст.86 Тобі треба зачитує учень
ІІ. Перевірка домашнього завдання
Учням було задано виконати завдання по групах.
- Скласти реакції – 2 учнів біля дошки
- Скласти формули сполук – 2 учнів зачитує
IІI. Актуалізація опорних знань учнів
Між класами неорганічних сполук існує генетичний зв'язок. Проаналізуємо, що означає поняття «генетичний зв’язок класів неорганічних сполук»:
- одні сполуки шляхом хімічних перетворень перевести в інші;
- існує тісний зв'язок між складом окремих класів сполук;
- взаємоперетворення кожного класу неорганічних сполук зумовлені їх фізичними й хімічними властивостями;
- генетичний зв'язок дає можливість припустити шляхи синтезу класів неорганічних сполук.
Можливе одержання різних класів неорганічних сполук із простих речовин шляхом взаємоперетворення складних речовин.
IV. Вивчення нового матеріалу
Логічна схема
Складаємо разом з учнями
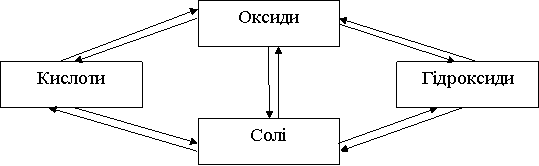
- Робота з зошитом: ст..90. розгляд таблиці
V. Узагальнення й систематизація
- ст. 88 №1 а - разом
- ст. 88 №1 б – самостійно, хто швидше
- Складіть схему перетворень (І і ІІ варіанти): на дошці
1) Са → СаО → Са(ОН)2 → СаСl2
2) S → SО2 → Н2SО3 → К2SО3
- Вхопіть правильну відповідь:
Чи реагує з хлоридною кислотою:
- Магній
- Кальцій оксид
- Нітратна кислота
- Барій сульфат
- Вуглець
- Карбон (ІІ) оксид
- Ферум (ІІ) гідроксид
Які сполуки є продуктами в кожній реакції? Яке це королівство з нашої країни?
- Знайди формули кислот (пірамідка)
Складіть формули 10 кислот, комбінуючи наведені нижче складові частини кислот по горизонталі, за умови, що частки кислот стоять поряд.
|
Н |
||||||||
|
Н2 |
Сl |
Н |
||||||
|
Н |
SО4 |
Н2 |
NО3 |
Н |
||||
|
Н2 |
Сl |
Н2 |
S |
Н3 |
РО4 |
Н2 |
||
|
Н |
Вr |
Н |
SО3 |
Н |
І |
Н4 |
SіО3 |
Н2 |
- Знайди пару та приховану хитрість. Співставте ліву та праві частини, зайві половинки відкиньте:
Хлоридна кислота
Магній
Купрум (ІІ) гідроксид
реагує з магнієм
реагує з киснем
розкладається при нагріванні
реагує з міддю
реагує кальцій карбонатом
- Хімічний привал
Я бачу ви вже й стомилися. Може трішечки відпочинемо. Вам доводилося читати книги різними мовами. Хімічна мова – це мова хімічних формул і символів. Тому я даю вам жартівливе завдання: перекласти рідною мовою такі вирази:
- Не все те Аурум, що блищить. (Не все те золото, що блищить)
- Ферумний характер. (Залізний характер)
- За купрумний гріш подавився. (За мідний гріш подавився)
- Перший день гість – Аурум, другий – Аргентум, а третій – Купрум, бери сумку та їдь. (Перший день гість – золото, другий – срібло, а третій – мідь, бери сумку та їдь)
- Білий як кальцій карбонат. (Білий як крейда)
- Слово – Аргентум, а мовчання – Аурум. (Слово – срібло, а мовчання - золото)
- Щоби друга пізнати, потрібно з ним пуд натрій хлориду з’їсти. (Щоби друга пізнати, потрібно з ним пуд солі з’їсти)
- Хрестики-нулики (І і ІІ варіанти)
Виграшний шлях:
- Оксиди
|
СО |
Fе2О3 |
|
|
СаО |
Сr2О3 |
Nа2О |
|
S |
Мg |
Сl2 |
- Кислоти
|
НF |
СО |
Н2SО3 |
|
Fе |
Н2СО3 |
НСl |
|
Н2SО4 |
СО2 |
Н2О |
- Гідроксиди
|
Аu |
КОН |
Н2О2 |
|
Ва(ОН)2 |
NаОН |
Н2S |
|
Са(ОН)2 |
LіОН |
АlСl3 |
- Солі
|
СаСО3 |
АgСl |
ВаSО4 |
|
Р2О3 |
Р2О5 |
В |
|
Nа2SО4 |
Н2 |
КСl |
Охарактеризуйте дану групу
- «Знайди помилку»
Виправте помилки в рівняннях:
Мg + О2 → МgО2
МgО + Н2С1 → МgС1 + Н2О
СаО + Н2О → СаН2 + О2
2HС1 + АgNO3→ АgС12 + H2NO3
Zn + НС12→ ZnС12 + Н
- Скринька моїх бажань. Напишіть реакцію до відео досліду:
- Взаємодія кислоти і металу
- Взаємодія кислоти і солі
- Взаємодія кислотних оксидів з водою
- Взаємодія металів з солями
- Взаємодія купрум (ІІ) оксиду і сульфатної кислоти
- Взаємодія основних оксидів з водою
- Взаємодія основних оксидів з кислотами
- Взаємодія сірки з цинком
- Горіння магнію в кисні
- Хімічні властивості нерозчинних гідроксидів
Яке це королівство з нашої країни? Який це клас?
VІ. Домашнє завдання
1. Буринська Н.М. §15 ст 86-89. №2 б, 3
2. Високий рівень – №4
VІІ. Підбиття підсумків
Рефлексія:
Взяти з літер слово
Дружба
На кожну літеру учні кажуть слово, якими вони були на уроці.
Д – добрими, доброзичливі, дружелюбні
Р – рішучі, розумні, риторичні
У – успішні, уважні
Ж – жваві, жадані,
Б – браві, боязкі
А – активні, артистичні
Літеру вішаємо – і в результаті утворюється слово.
Наша подорож добігла до кінця. Хотілося б вам побажати:
Я дуже рада за вас, діти,
Що ви могли чогось навчитись.
Отож, старайтесь й надалі
Щоби нові скорити далі,
Щоб знов змогли чогось навчитися
В житті, повірте, це згодиться.


про публікацію авторської розробки
Додати розробку
