Молекули і атоми(теорія)
Хімія 7 клас
Атоми і молекули
План:
- Атоми
- Молекули
- Молекулярні і немолекулярні речовини
- Термін «атом» запропонував Дж. Дальтон на початку 19 століття. Він назвав атомами найдрібніші частинки, які не змінюються в хімічних реакціях.
Атоми — найдрібніші електронейтральні частинки речовини, які складаються з позитивно зарядженого ядра і негативно заряджених електронів, які рухаються навколо ядра.
На сьогодні відомо 118 видів атомів. Більше 90 з них існують у природі, а інші —отримані штучно.
Атоми характеризуються:
- певними дуже малими розмірами;
- певною, дуже малою масою;
- певною будовою.
Розміри атомів настільки малі, що побачити їх неможливо навіть у найпотужніший мікроскоп. Радіуси атомів складають 0,046–0,25 нм (1 нм = 10−9 м). Найменшим є атом Гелію, а найбільшим — Францію.
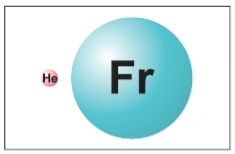 Атоми Гелію і Францію
Атоми Гелію і Францію
Маси атомів теж дуже малі. Так маса атома Гідрогену становить всього 1,67⋅10−24 г.
До кінця 19-го століття атоми вважали неподільними частинками. Але вчені довели, що атом має складну будову.
Відповідно до сучасних уявлень кожен атом складається з позитивно зарядженого ядра і електронів, що рухаються навколо нього. Електрони мають негативний заряд і нейтралізують позитивний заряд ядра.
Ядро набагато менше самого атома. Так, радіус атома Гідрогену становить 0,046 нм, а радіус його ядра — всього 0,00000065 нм.
Ядро практично усіх атомів складається з дрібніших частинок: протонів (p) і нейтронів (n). Протони заряджені позитивно і визначають заряд ядра. Нейтрони — частинки без заряду.
Заряд протона дорівнює за величиною заряду електрона, а число протонів в ядрі дорівнює числу електронів в атомі. Тому атоми нейтральні.
Атоми різняться між собою будовою (числом частинок, що містяться у них), а також масою і розмірами.
Атоми рідко зустрічаються в ізольованому вигляді. Зазвичай вони сполучаються один з одним у молекули або більші структури. Число варіантів сполучення атомів є практично нескінченним, і їх відносно невелике число призводить до утворення величезної кількості різноманітних речовин.
Приклад:
З атомів Оксигена можуть утворюватися дві речовини.
Коли сполучаються два атоми Оксигену, утворюється молекула кисню.

Молекула кисню
Якщо три атоми Оксигену сполучаються між собою, утворюється молекула озону.

Молекула озону
У молекулах атоми сполучені один з одним хімічними зв'язками.
- Молекули — найдрібніші частинки речовини, здатні існувати самостійно, що є носіями хімічних властивостей речовин.
Молекули характеризуються якісним і кільнісним складом.
Якісний склад показує з яких атомів складається молекула.
Приклад:
Молекули води і гідроген пероксиду складаються з атомів Гідрогену і Оксигену, а молекула вуглекислого газу — з атомів Карбону і Оксигену.
Кількісний склад показує, скільки атомів кожного виду міститься в молекулі.
Приклад:
Молекула води складається з двох атомів Гідрогену і одного атому Оксигену, а молекула пероксиду водню — з двох атомів Гідрогену і двох атомів Оксигену.
У молекулах може бути різна кількість атомів.
В інертних газах гелію, неону, аргону, криптону, ксенону, радону молекули одноатомні.
Молекули кисню, водню, азоту, хлору, брому, йоду — двохатомні.
Молекула озону складається з 3 атомів Оксигену, а сірки — з 8 атомів Сульфуру.
Молекула етилового спирту містить 2 атоми Карбону, 6 атомів Гідрогену і 1 атом Оксигену, а молекула цукру — 12 атомів Карбону, 22 атоми Гідрогену і 11 атомів Оксигену.
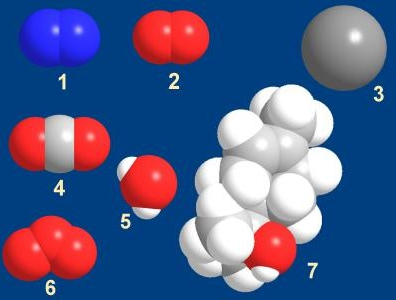
Моделі молекул: 1 — кисню, 2 — водню,
3 — неону, 4 — вуглекислого газу, 5 — води,
6 — озону, 7 — терпінеолу
Хімічні властивості молекули визначаються тим, скільки і яких атомів у ній міститься, а також в якому порядку вони з'єднані між собою.
Приклад:
Молекули кисню і озону відрізняються тільки кількісним складом. Кисень — газ без запаху, необхідний живим організмам для дихання. Озон має запах, може викликати отруєння.
- Існують речовини з молекулярною і немолекулярною будовою.
Між молекулами виникають сили взаємного притягування та відштовхування. Найбільше ці сили виражені у твердих речовинах, а найменше — у газах.
Сили взаємодії між молекулами є слабкими, тому молекулярні речовини леткі, мають низькі температури плавлення і кипіння. Усі газоподібні і рідкі за звичайних умов речовини складаються з молекул. Молекулярні речовини можуть бути і твердими, але відрізнити їх можна завдяки їх легкоплавкості.
Зверни увагу!
Гази, рідини і легкоплавкі тверді речовини мають молекулярну будову.
Усі речовини, що мають запах мають молекулярну будову.
Атоми можуть сполучатися один з одним і іншим способом. Так, у кристалах алмазу, графіту, піску всі атоми сполучені в єдине ціле, і молекулу виділити в них неможливо.
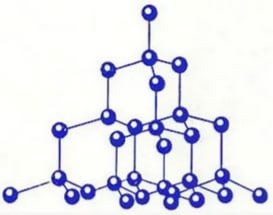
Будова алмазу
Зверни увагу!
Немолекулярну будову мають практично усі метали.
Наприклад: залізо, мідь, цинк, алюміній та інші.
У деяких складних речовинах атоми перетворюються на заряджені частинки — йони — і також не утворюють молекул. Протилежно заряджені йони притягуються один до одного і утворюють тверду тугоплавку речовину. Таку будову мають кухонна сіль, крейда, питна сода, мідний купорос, луг.
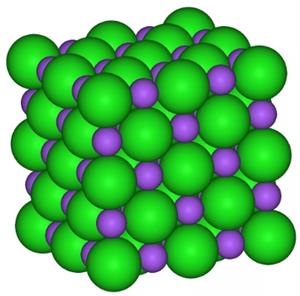
Будова кухонної солі
Такі речовини називають немолекулярними. У їх кристалах зв'язки між частинками міцні, тому усі немолекулярні речовини тверді, нелеткі, тугоплавкі.


про публікацію авторської розробки
Додати розробку
