Молекулярний рівень організації життя. АТФ











Енергія – це вічне захоплення! Вільям Блейк Запам’ятайте! Енергія (від грец. енергос – діяльний) – це фізична величина, загальна кількісна міра руху і взаємодії всіх видів матерії. Поняття енергії поєднує всі явища природи в одне ціле. Воно пов’язане зі здатністю фізичного тіла або системи виконувати певну роботу. При цьому тіло або система частково втрачає енергію.
Як забезпечується єдність та сталість хімічного складу клітини?Молекулярний рівень життя – це рівень організації, існування й властивості якого визначаються хімічними елементами й молекулами та їхньою участю в процесах перетворення енергії, речовин та інформації. Для підтримання упорядкованості хімічного складу в мінливих умовах існування клітинам необхідне безперервне надходження енергії ззовні. Джерелом цієї енергії є світло для клітин автотрофів або хімічна енергія органічних сполук для клітин гетеротрофів. Перший закон термодинаміки вказує на те, що енергія не може бути ні створена, ні знищена, вона лише переходить з однієї форми в іншу.
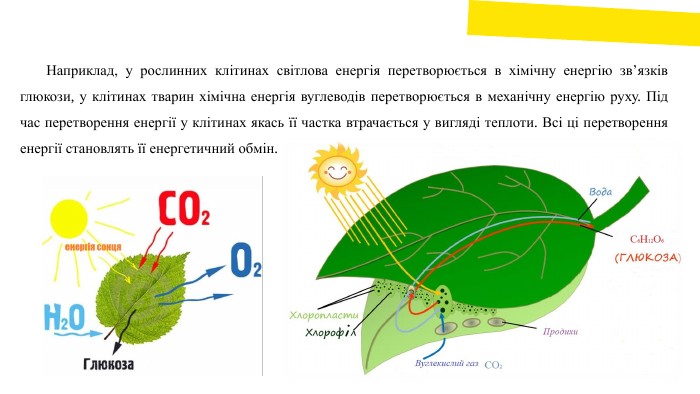
Наприклад, у рослинних клітинах світлова енергія перетворюється в хімічну енергію зв’язків глюкози, у клітинах тварин хімічна енергія вуглеводів перетворюється в механічну енергію руху. Під час перетворення енергії у клітинах якась її частка втрачається у вигляді теплоти. Всі ці перетворення енергії становлять її енергетичний обмін.
Під час енергетичного обміну енергія використовується для перетворення речовин: синтезу складних молекул із простих, утворення особливих енергетичних сполук з макроергічними зв’язками тощо. Завдяки енергії клітина здійснює й перетворення інформації: сприймає сенсорну інформацію ззовні, подає інформативні сигнали для інших клітин, передає спадкову інформацію наступному поколінню клітин. Ці приклади свідчать про те, що перетворення енергії відбувається водночас з перетвореннями речовин та інформації. Отже, єдність й сталість складників молекулярного рівня забезпечується триєдиним потоком енергії, речовин та інформації, що постійно проходять через клітини.
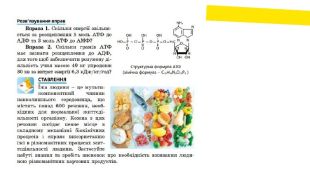
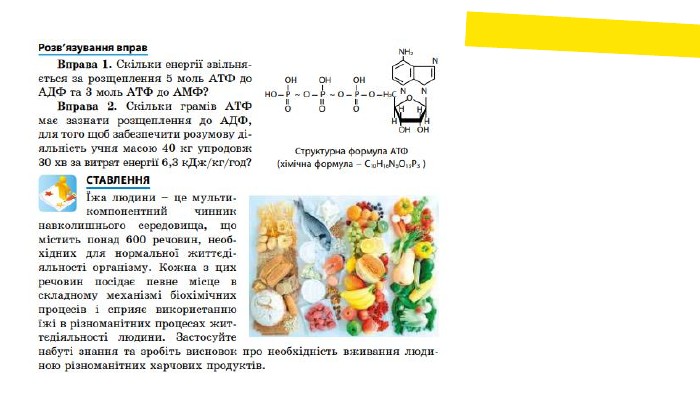
Як будова АТФ пов’язана з її функціями?Аденозинтрифосфатна кислота (АТФ) – органічна сполука, що належить до вільних нуклеотидів і є універсальним хімічним акумулятором енергії у клітині. Молекула АТФ є нуклеотидом, який складається із аденіну, рибози і трьох залишків ортофосфатної кислоти. При гідролітичному відщепленні фосфатної групи від АТФ вивільняється близько 40 к. Дж енергії та утворюється АДФ (аденозиндифосфатна кислота). Коли ж від молекули АТФ відщеплюються два ортофосфатні залишки, то утворюється АМФ (аденозинмонофосфатна кислота) і звільняється близько 80 к. Дж енергії. АТФ утворюється за рахунок енергії, що виділяється під час окиснення речовин у цитоплазмі клітин, мітохондріях, а під час фотосинтезу – ще й у хлоропластах.
Використання АТФ залежить від енергетичних потреб клітин. Так, у стані спокою у людини розпадається 28 г АТФ за 1 хв, а під час фізичного навантаження затрата АТФ досягає 500 г за 1 хв. У зворотному процесі, під час утворення АТФ з АДФ чи АМФ і неорганічного фосфату, енергія акумулюється у високоенергетичних макроергічних зв’язках, які виникають між залишками ортофосфатної кислоти. Молекули АТФ утворюються в кисневих (аеробних) і безкисневих (анаеробних) умовах. Процеси розщеплення і утворення АТФ відбуваються постійно відповідно до схеми: Отже, основна функція АТФ – це енергетична, оскільки бере участь в енергетичному обміні, запасаючи в своїх макроергічних зв’язках значну кількість енергії.
Яке значення ферментів у клітині?Установлено, що ферменти мають білкову природу, утворюються в клітинах організмів і слугують каталізаторами (прискорювачі) практично в усіх біохімічних реакціях. Відмінність ферментів від хімічних каталізаторів полягає у їхній специфічності. Кожний вид ферменту каталізує особливу хімічну реакцію. В природі є і РНК-ферменти, що називаються рибозимами. Їх вважають первісною формою органічних каталізаторів, які були замінені білковими ферментами в процесі еволюції. Наука про ферменти називається ензимологією.
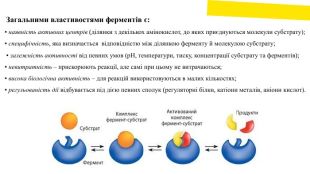
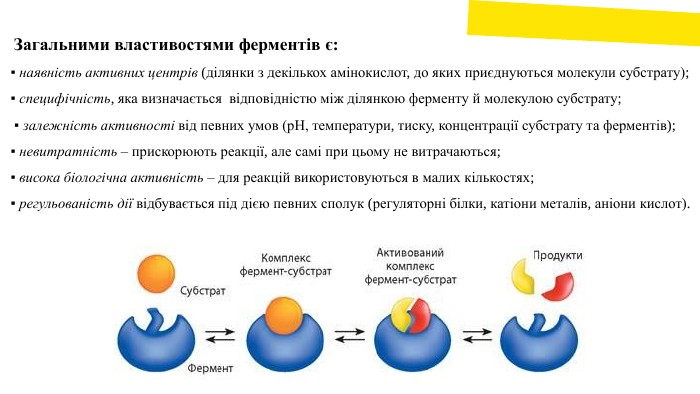
Загальними властивостями ферментів є: ▪ наявність активних центрів (ділянки з декількох амінокислот, до яких приєднуються молекули субстрату); ▪ специфічність, яка визначається відповідністю між ділянкою ферменту й молекулою субстрату; ▪ залежність активності від певних умов (р. Н, температури, тиску, концентрації субстрату та ферментів); ▪ невитратність – прискорюють реакції, але самі при цьому не витрачаються; ▪ висока біологічна активність – для реакцій використовуються в малих кількостях; ▪ регульованість дії відбувається під дією певних сполук (регуляторні білки, катіони металів, аніони кислот).
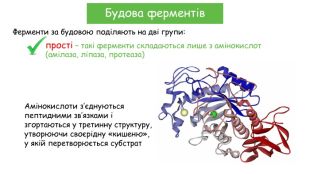
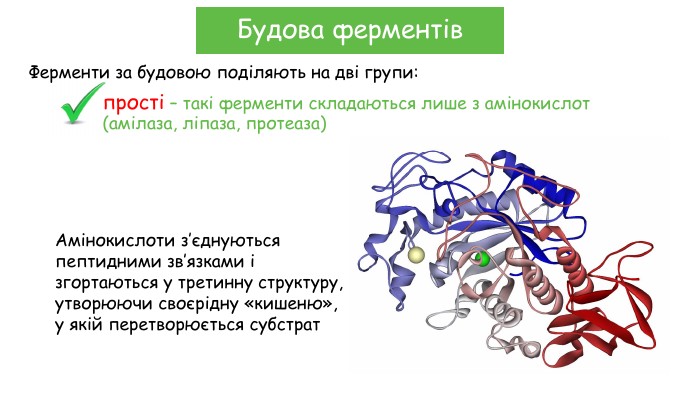
Найчастіше ферменти класифікують за хімічним складом на прості й складні. Прості ферменти є однокомпонентними, тобто мають лише білкову частину (наприклад, амілази, ліпази, протеази). Складні ферменти – двокомпонентні, складаються з апоферменту (білкова частина) й кофактора (небілкова частина) (наприклад, каталаза, ДНК-полімераза). Ферментні реакції поділяються на анаболічні (реакції синтезу) і катаболічні (реакції розпаду), а сукупність всіх цих процесів у живій системі називають метаболізмом. Значення ферментів полягає в тому, що вони збільшують швидкість хімічних реакцій у клітині, забезпечуючи хімічні перетворення речовин внаслідок зниження енергії активації (енергії, необхідної для надання реакційної здатності молекулі).
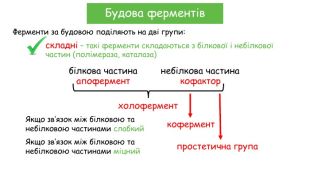
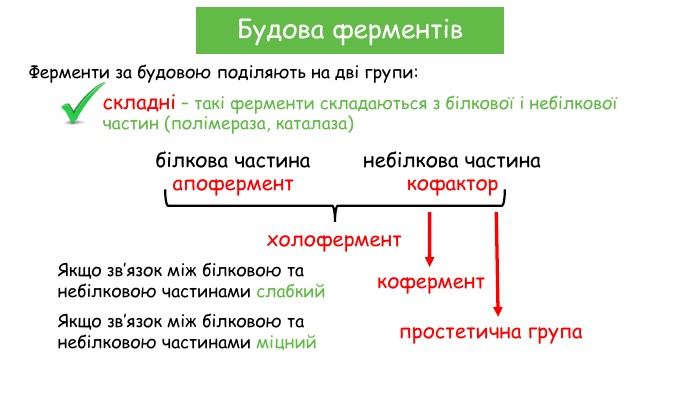
Будова ферментівскладні – такі ферменти складаються з білкової і небілкової частин (полімераза, каталаза)Ферменти за будовою поділяють на дві групи:білкова частинанебілкова частинаапоферменткофакторхолофермент. Якщо зв’язок між білковою та небілковою частинами слабкийкофермент. Якщо зв’язок між білковою та небілковою частинами міцнийпростетична група
Будова ферментівскладні – такі ферменти складаються з білкової і небілкової частин (полімераза, каталаза)Ферменти за будовою поділяють на дві групи:білкова частинанебілкова частинаапоферменткофакторвизначає специфічність ферменту і обумовлює швидкість реакціїутворює активний центр, забезпечує перетворення субстрату, перенесення атомів, електронів, функціональних груп. Коферменти – це вітаміни, йони Купруму, Феруму, Магнію, Мангану
Класифікація ферментів. Оксидоредуктази каталізують окисно-відновні реакціїТрансферази здійснюють перенесення функціональних груп всередині та між клітинами. Гідролази є ферментами розкладу субстратів за участю води. Ліази каталізують реакції розщеплення субстратів без участі водиІзомерази впливають на реакції внутрішньоклітинних перетворень. Синтетази беруть участь в утворенні різних сполук
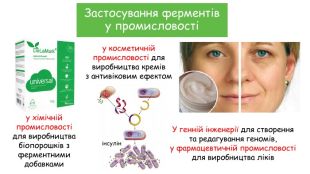
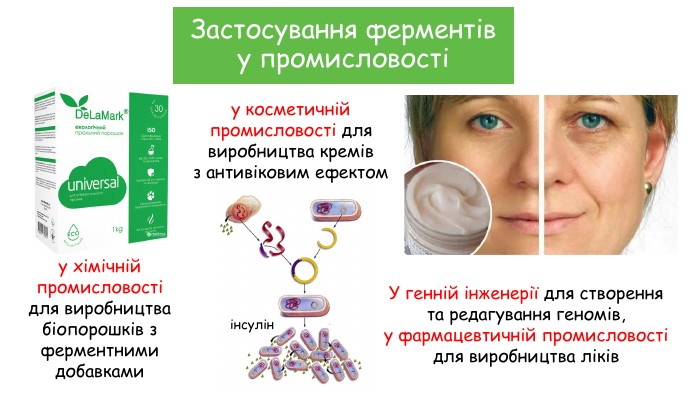
у хімічній промисловості для виробництва біопорошків з ферментними добавкамиу косметичній промисловості для виробництва кремів з антивіковим ефектом. У генній інженерії для створення та редагування геномів,у фармацевтичній промисловості для виробництва ліківінсулін. Застосування ферментіву промисловості


про публікацію авторської розробки
Додати розробку