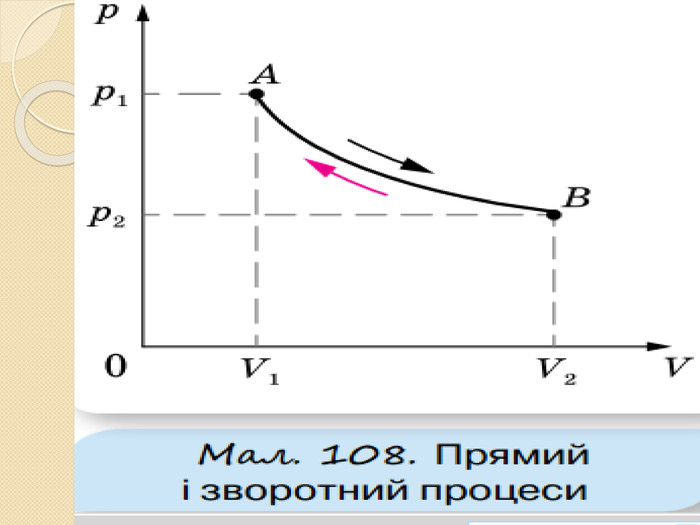
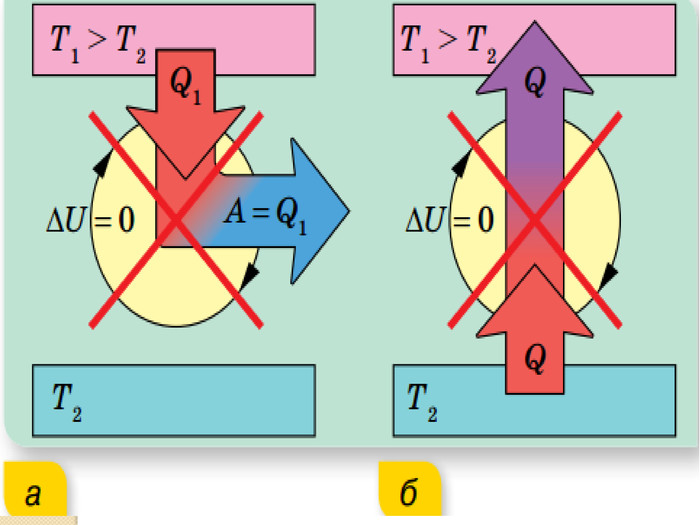
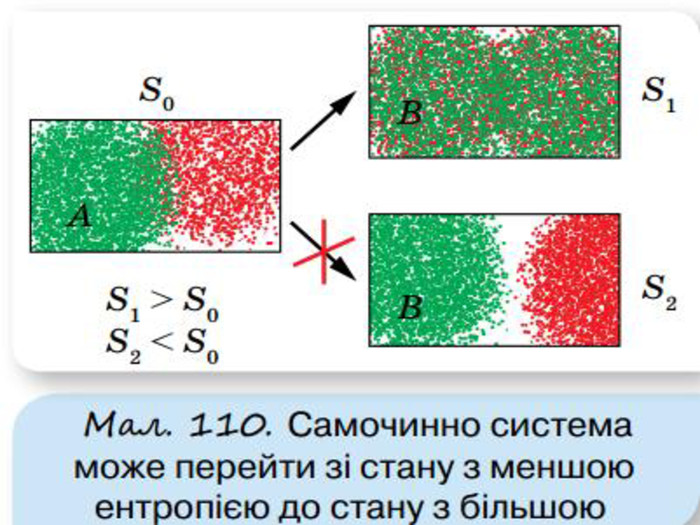
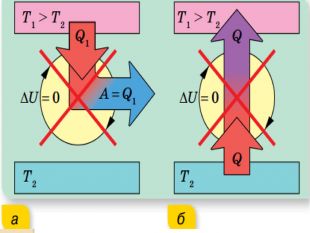
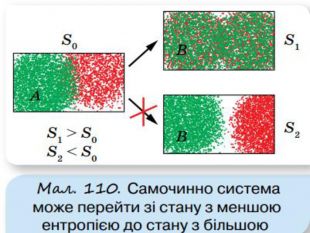
Напрямок теплових процесів. Другий закон термодинаміки. Ентропія
Про матеріал
Презентація створена для пояснення нового матеріалу з теми "Напрямок теплових процесів. Другий закон термодинаміки. Ентропія"
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
pptx
До підручника
Фізика (академічний та профільний рівень) 10 клас (Засєкіна Т.М., Засєкін Д.О.)
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку