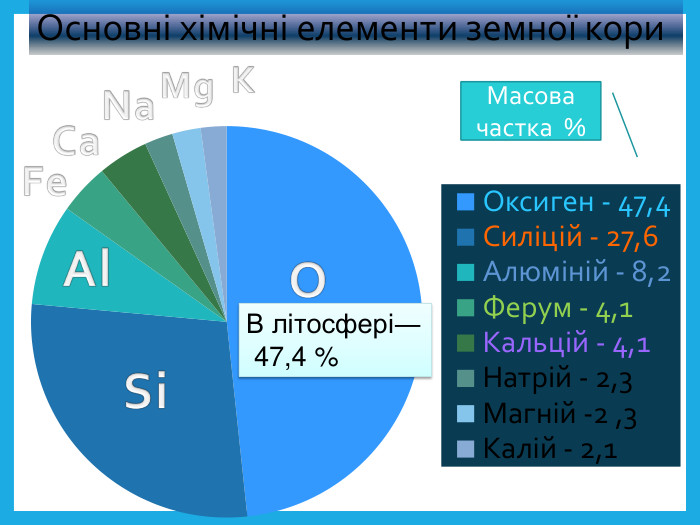
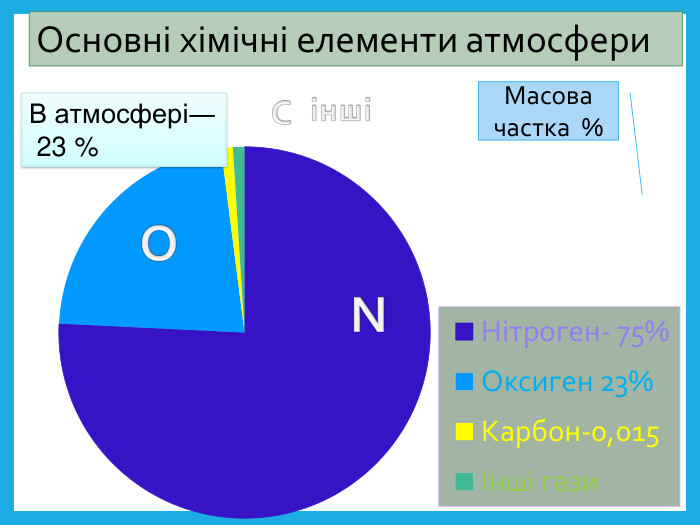
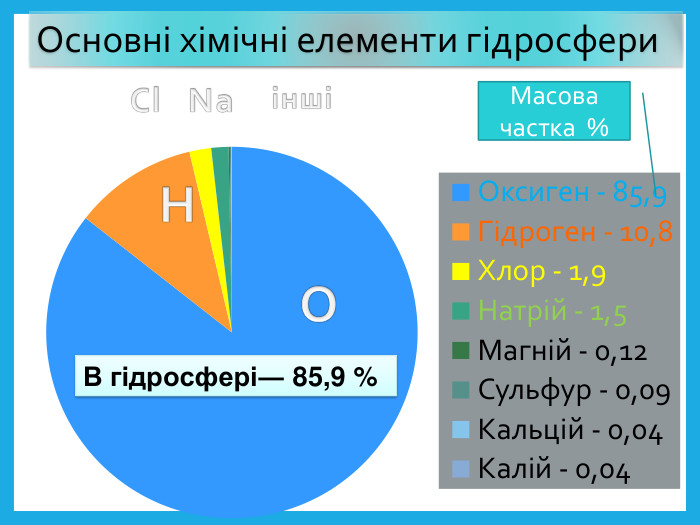
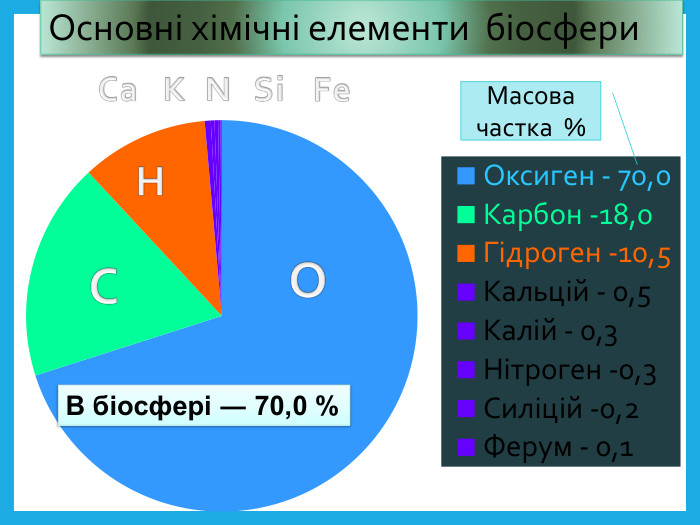
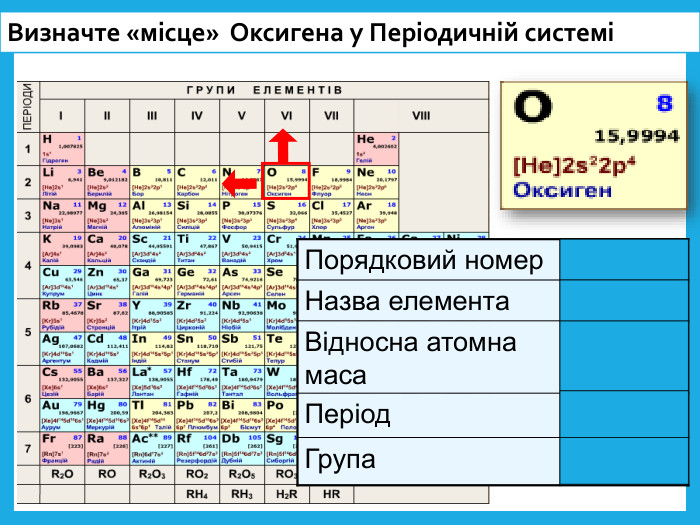
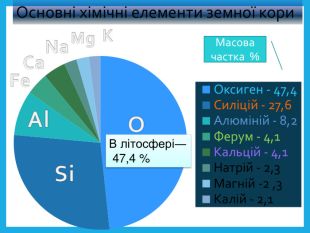
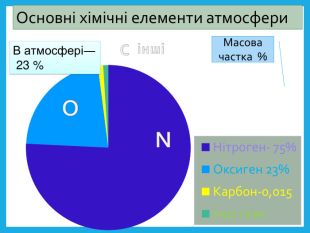
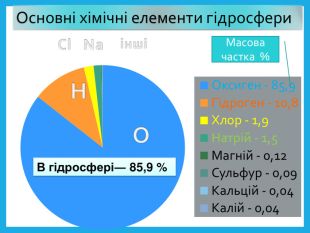
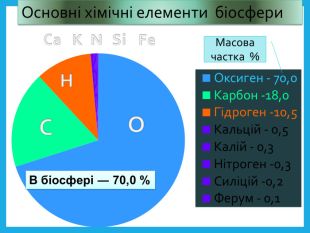
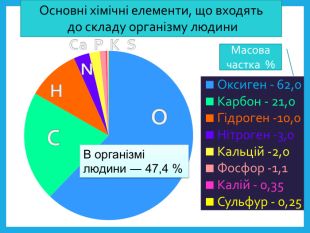
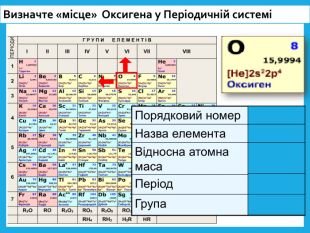
Оксиген. Кисень, склад його молекули, фізичні властивості.
Про матеріал
Презентація до уроку "Оксиген. Кисень, склад його молекули, фізичні властивості. "Матеріал викладений просто, у доступній формі. Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку