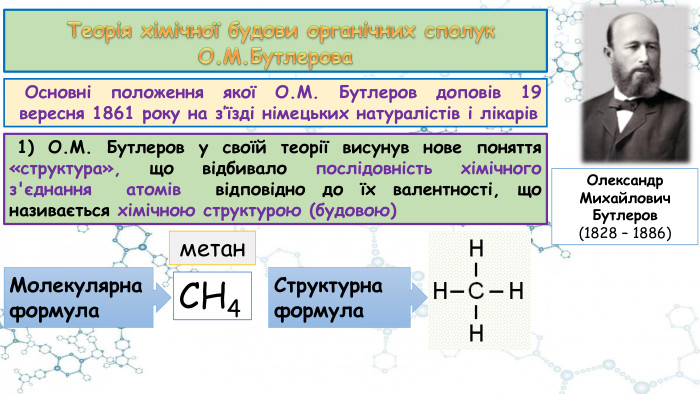
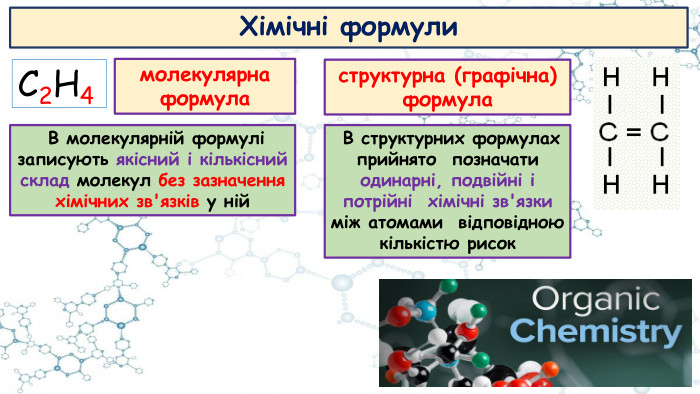
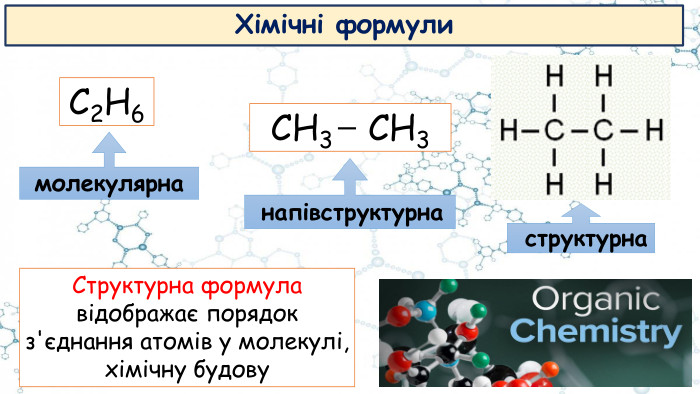
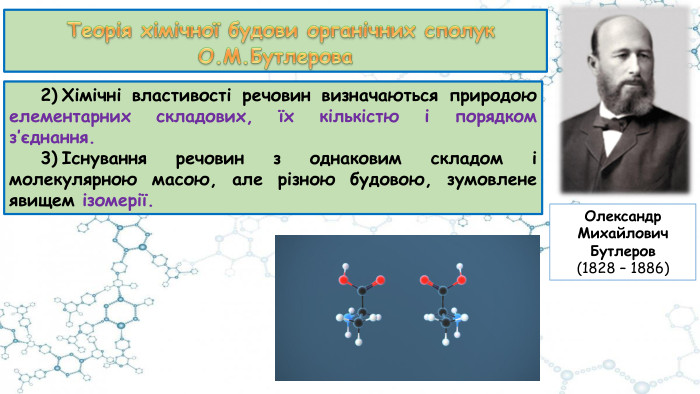
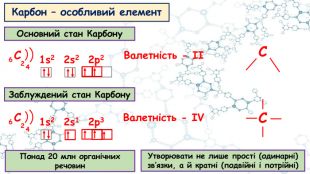
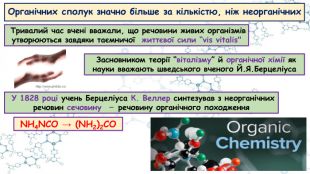
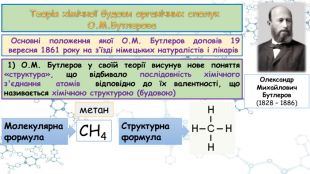
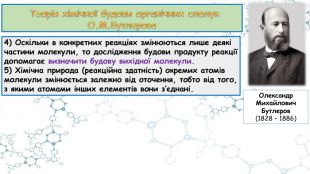
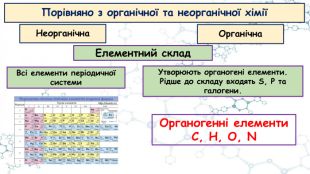
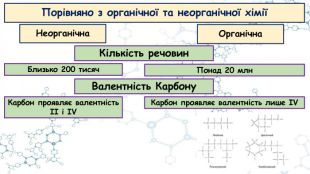
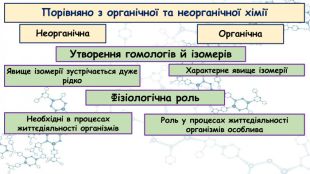
Особливості органічних сполук (порівняно з неорганічними). Елементи-органогени
Про матеріал
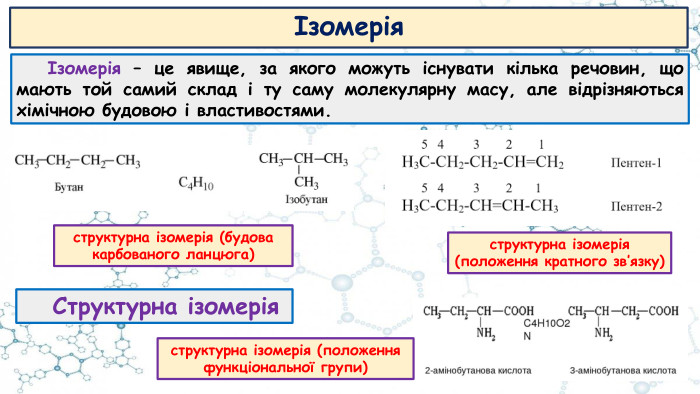
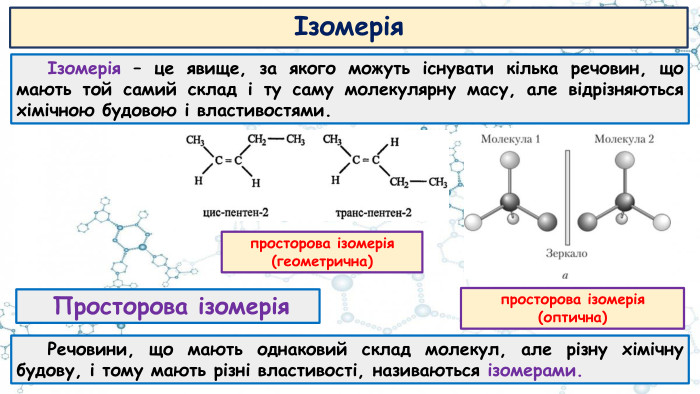
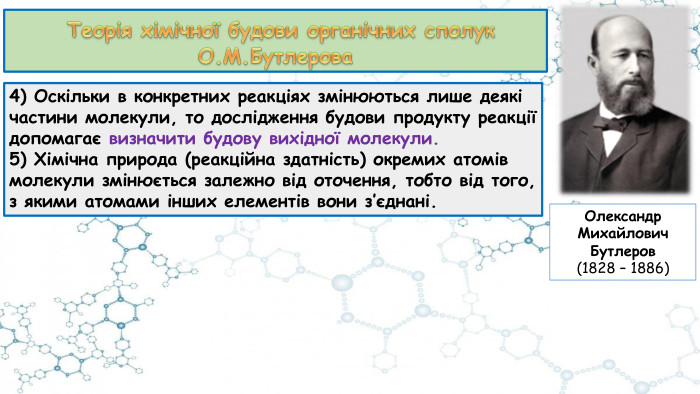
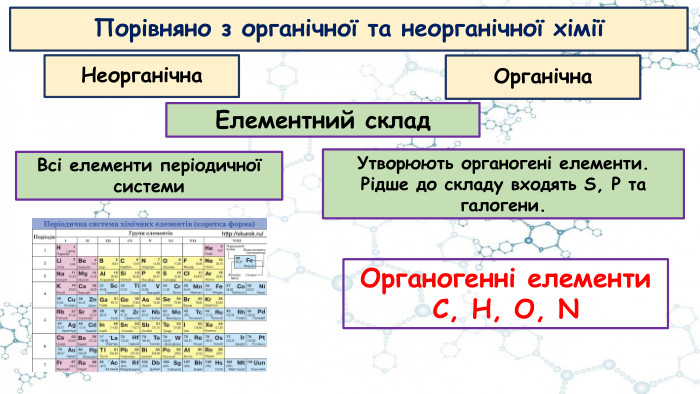
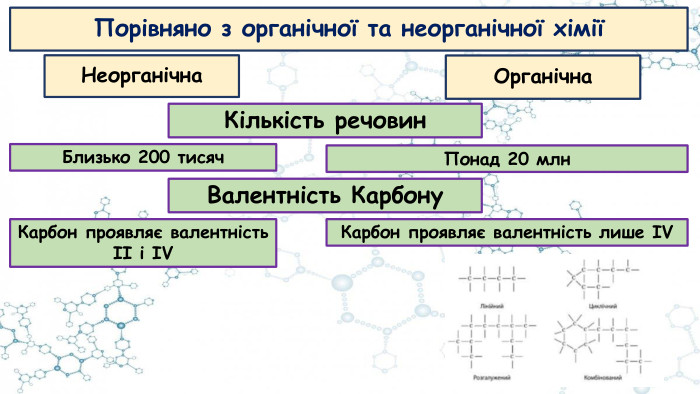
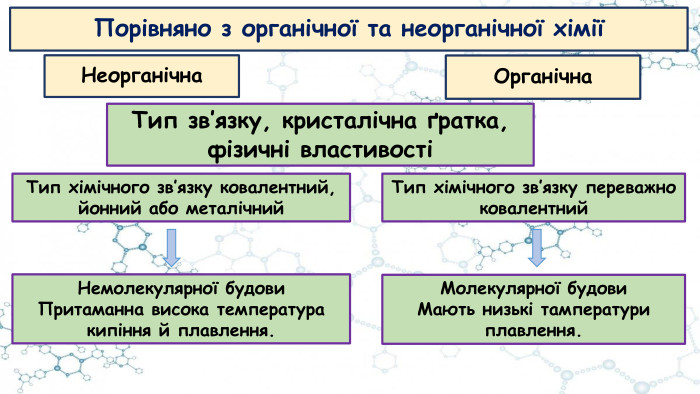
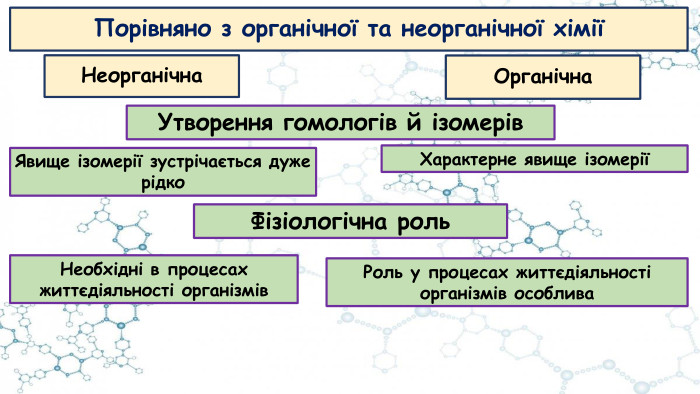
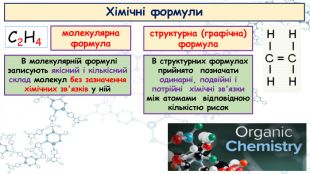
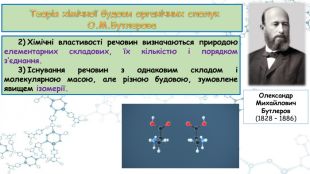
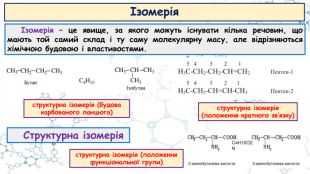
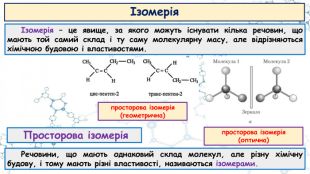
Презентація до відео-уроку "Особливості органічних сполук (порівняно з неорганічними). Елементи-органогени"
Посилання на відео-урок: https://youtu.be/REo_omQheBU Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку