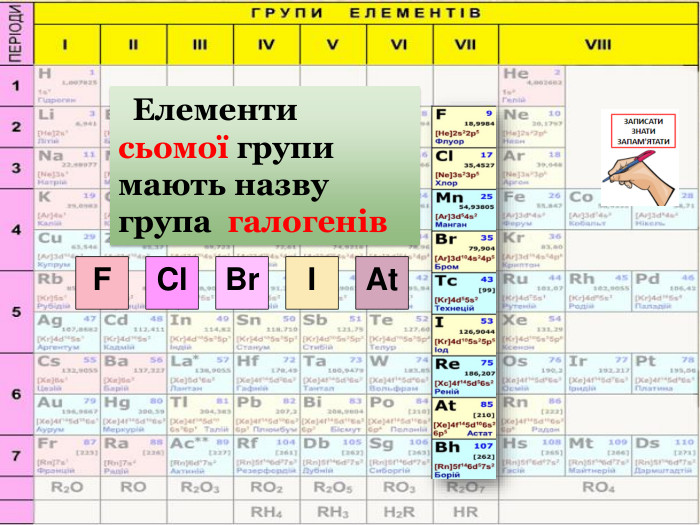
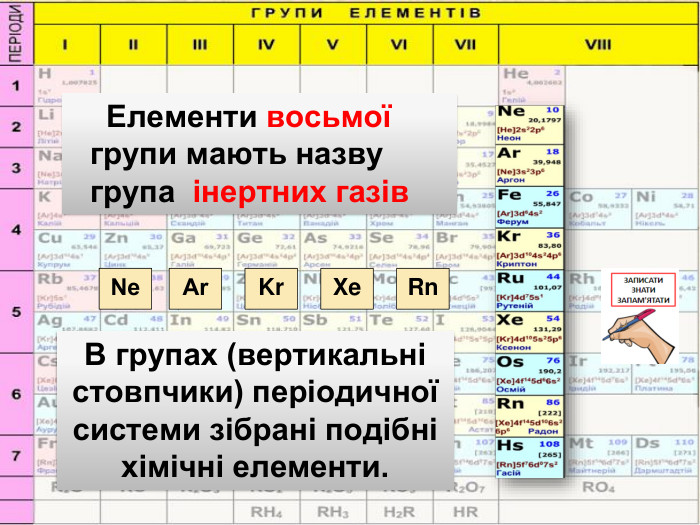
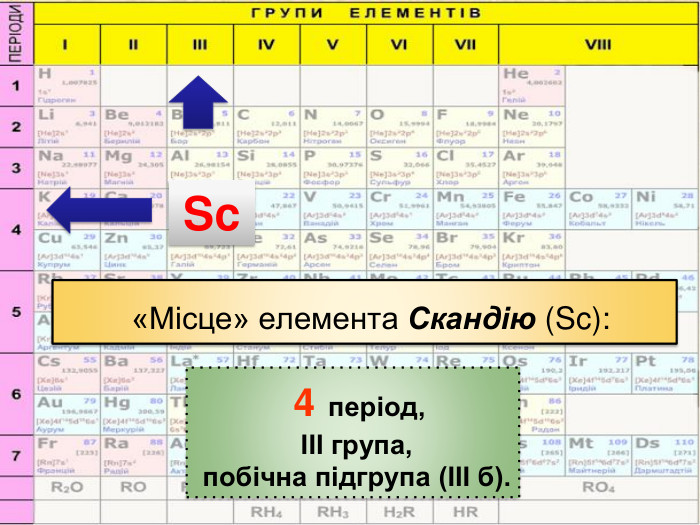
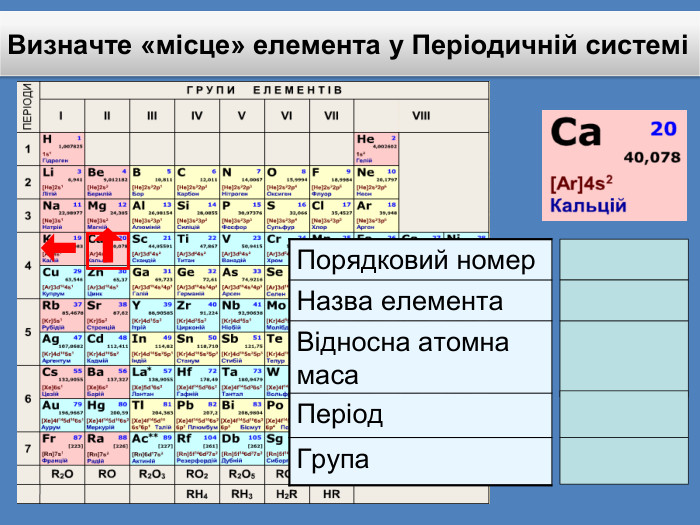
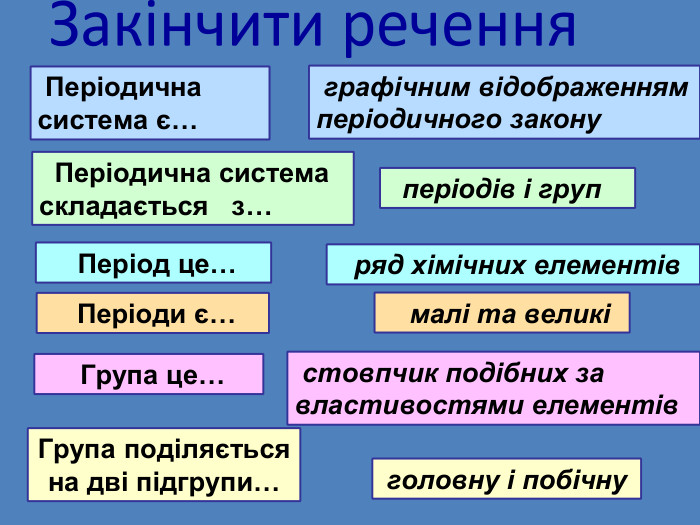
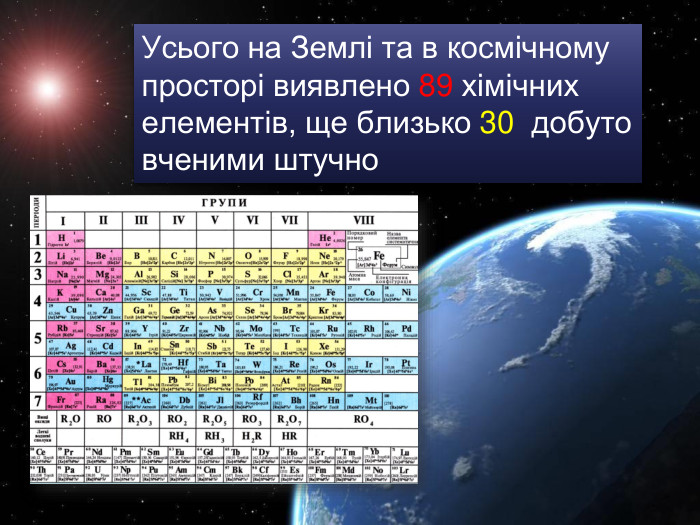
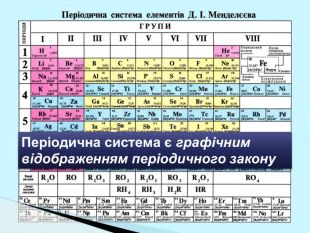
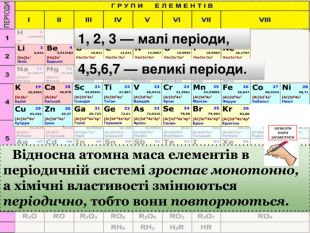
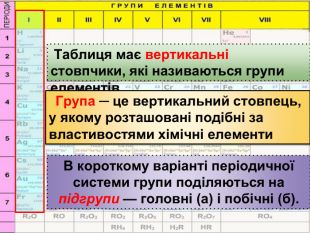
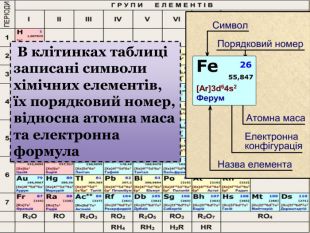
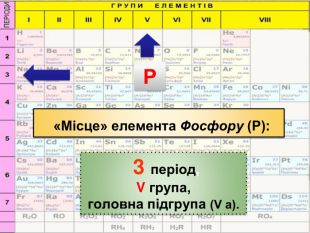
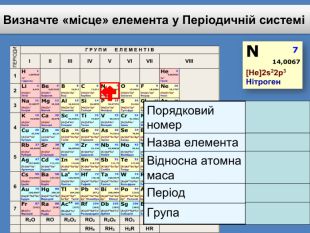
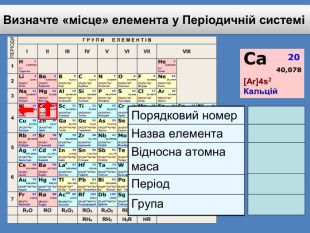
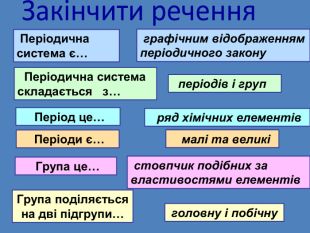
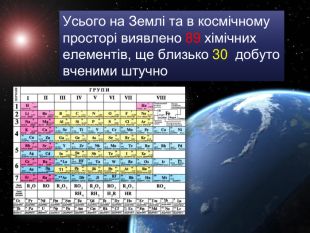
Періодичний закон та Періодична система хімічних елементів Д. І. Менделєєва. Поняття про лужні, інертні елементи, галогени.
Про матеріал
Презентація до уроку "Періодичний закон та Періодична система хімічних елементів Д. І. Менделєєва. Поняття про лужні, інертні елементи, галогени"
Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку