Практична робота з хімії "Хімічні властивості оцтової кислоти"
реалізація знань про властивості оцтової кислоти в практичній діяльності учнів.
формувати вміння знаходити спільні і важливі ознаки і властивості, застосовувати набуті знання на практиці, формулювати узагальнюючі висновки та оцінювати результати виконаних дій.
допомогти вихованню дбайливого відношення до праці, ініціативності, наполегливості в досягненні мети.
Практична робота № 4 . Властивості етанової кислоти
Мета: Дидактична: реалізація знань про властивості оцтової кислоти в практичній діяльності учнів.
Розвиваюча: формувати вміння знаходити спільні і важливі ознаки і властивості, застосовувати набуті знання на практиці, формулювати узагальнюючі висновки та оцінювати результати виконаних дій.
Виховна: допомогти вихованню дбайливого відношення до праці, ініціативності, наполегливості в досягненні мети.
Тип уроку: урок застосування знань, умінь та навичок
Форма: практична робота
Реактиви та обладнання: магній, магній оксид ( порошок), розчини оцтової кислоти, натрій гідроксиду, натрій карбонату, індикатор , пробірки, шпатель.
Структура уроку
І. Оголошення теми уроку...............................1хв
ІІ. Мотивація навчальної діяльності учнів....................2хв
ІІІ. Актуалізація опорних знань та практичного досвіду учнів.................5хв
ІV. Виконання практичної роботи..........................33хв
V. Домашнє завдання..................................2хв
VІ. Підведення підсумків уроку...........................2хв
Хід уроку
І. Оголошення теми
Записується дата уроку та тема уроку: «Хімічні властивості оцтової кислоти».
ІІ. Мотивація навчальної діяльності учнів
- При виконанні роботи ви покажете свої знання про властивості карбонових кислот. Ці вміння згодяться вам при подальшому вивченні хімії, у побуті і можливо у майбутній професії.
- За виконання дослідів, оформлення звіту кожний учень отримує оцінку.
- Спробуємо збагатити досвід про застосування оцтової кислоти в побуті.
- З карбоновими кислотами пов’язано багато цікавих історій Ось одна з них.
«…Вона вийняла з вуха одну з тих величезних перлин…і …занурила перлину в оцет. Запанувала тиша. Вражені гості, завмерши спостерігали, як незрівнянна перлина повільно розчинялася у мідному оцті. Ось від неї не залишилося й сліду, і тоді Клеопатра підняла кубок і випила весь напій до останньої краплини».
Г.р.Хаггард, «Клеопатра»
 А що сталося далі, ви самі зможете прочитати у цьому творі, а з реакцією ми познайомимося на уроці. Дуже смілива Клеопатра! Завдяки нашим правилам техніки безпеки праці, ми не будемо випивати напій
А що сталося далі, ви самі зможете прочитати у цьому творі, а з реакцією ми познайомимося на уроці. Дуже смілива Клеопатра! Завдяки нашим правилам техніки безпеки праці, ми не будемо випивати напій
Джіованні Баттиста Тьєполо «Бенкет Клеопатри»
ІІІ. Актуалізація опорних знань та практичного досвіду учнів
Бесіда, у ході якої визначається ступінь підготовки учнів до практичної роботи. Проведення інструктажу з техніки безпеки при виконанні даної роботи.
Учитель. При виконанні практичної роботи, кому загрожує небезпека? Вам. Уявіть собі, що перед вами терези, на одній шальці яких ви бачите цікавість, на другій – ваша відповідальність. Тільки додержуючись правил техніки безпеки ви можете виробляти ці риси характеру. Будьте обачливі! Обирайте безпечне життя.
При виконанні відповідних завдань Ви повинні економити речовини, а також час, адже по цих показниках ціниться робота виробничих підприємств. Отже, з Вами поруч: економія, бережливість, порядок в роботі, ваше відношення до праці.
Будьте уважні, зосереджені, зацікавлені в набутті знань, умінь і навичок! Я покладаюсь на ваші здібності, ваш розум, ваше мислення.
ІV. Виконання практичної робота. Узагальнення та систематизація знань
Практична робота виконується групами по два учні. Учням видаються дидактичні картки. ( підручник на с. 189)
Починаєте роботу над кожним дослідом з відповіді на питання, прогнозування виконання досліду та його результатів. Свої дії та спостереження записуйте в запропоновану таблицю.
ПРАКТИЧНА РОБОТА № 4
ВЛАСТИВОСТІ ОЦТОВОЇ (ЕТАНОВОЇ ) КИСЛОТИ
Мета: дослідити хімічні властивості оцтової кислоти, спільні з хімічними властивостями інших кислот; перевірити на практиці набуті знання з теми «Карбонові кислоти»
Обладнання: штатив для пробирок, спиртівка.
Реактиви: індикаторні папірці, розчини NaOH, Na2CO3, CH3COOH, Mg, MgO
Інструктаж з правил безпеки:
- акуратно брати розчини в потрібних кількостях речовин;
- проявляти особливу обережність при роботі з розчинами кислот і лугів;
- обережно поводитися зі скляним посудом
- обережно проводити нагрівання
З правилами техніки безпеки ознайомлен (а) _______(підпис)
ХІД РОБОТИ
|
№ |
Назва досліду |
спостереження |
Рівняння реакцій, висновки |
|
1 |
Дія оцтової кислоти на універсальний індикатор
|
Скляною паличкою наносимо краплю кислоти. Індикатор показав ( яке середовище?) |
Запис рівняння електролітичної дисоціації CH3COOH↔ Оцтова кислота – слабкий електроліт, дисоціює, утворюючи гідроген – йони, тому змінює колір індикаторів. |
|
|
Взаємодія оцтової кислоти з основами (лугами) |
У чисту пробірку наливаю 1 мл розчину NaOH, додаю метилоранж, який набуває ____ забарвлення Після доливання розчину оцтової кислоти забарвлення _______
|
CH3COOH+NaOH→ Тип цієї реакції ________ Скласти повне та скорочене йонне рівняння
Оцтова кислота реагує з лугами, утворюючи сіль і воду.
|
|
2 |
Взаємодія оцтової кислоти з металами |
В пробірку з порошком Mg доливаю 1 мл CH3COOH. Внаслідок реакції виділяється газ ____________ |
CH3COOH+Mg→ Тип цієї реакції________ Оцтова кислота реагує з металами, що в ряді напруг стоять до Гідрогену, утворюючи сіль і водень. |
|
3 |
Взаємодія оцтової кислоти з основними оксидами |
В пробірку з білим порошком MgО доливаю 1 мл CH3COOH. Відбувається розчинення порошку |
CH3COOH+MgО→ Тип цієї реакції________ Утворюються речовини______ |
|
4 |
Взаємодія оцтової кислоти з солями |
В пробірку з розчином CH3COOH. наливаю 1 мл Na2CO3 Внаслідок реакції виділяється газ ____
|
CH3COOH+ Na2CO3 → Тип цієї реакції ________ Скласти повне та скорочене йонне рівняння Оцтова кислота реагує солями, якщо при цьому утворюється осад, газ або малодисоційована речовина. |
ВИСНОВКИ: Відповісти на запитання: якими спільними з неорганічними кислотами володіє оцтова кислота.
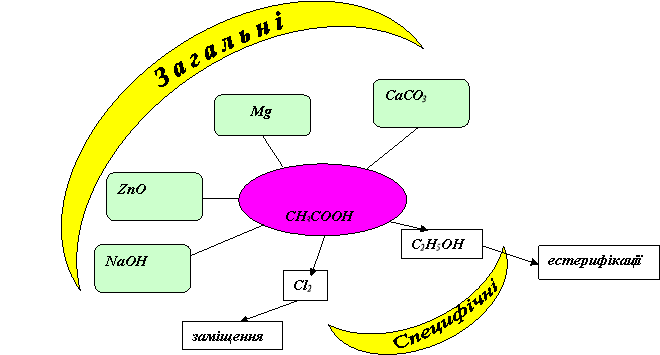
Органічні кислоти (на прикладі оцтової CH3COOH) мають, як загальні, так і специфічні властивості. У карбонових кислотах під впливом карбоксильної групи збільшується рухливість атомів Гідрогену, які стоять біля атома Карбону сусіднього з карбоксильною групою. Тому вони можуть легко заміщуватися атомами Cl2,Br2
Подібність властивостей органічних і неорганічних кислот, характеризують такі властивості етанової кислоти:
- змінює колір індикаторів;
- реагує з металами, що стоять у ряді активності металів до водню;
- реагує з основними оксидами;
- реагує з солями слабших за неї кислот (наприклад, з карбонатами).
Додаткові завдання:
- У стародавньому Римі дію оцтової кислоти на свинець використовували для виготовлення солодкого густого напою. Скисле вино наливали у свинцеві горнятка і витримували певний час. Римські аристократи ласували цим напоєм. Солодкого смаку йому надавав так званий свинцевий цукор, продукт взаємодії оцтової кислоти та свинцю. Треба сказати, що ця речовина досить отруйна, тому аристократи, самі того не знаючи, істотно вкорочували собі життя. Напишіть рівняння реакції, що відбувалася в горнятках.
2. Вапняний наліт на кранах, накип у чайнику — це кальцій карбонат. Як можна позбавитись накипу або вапняного нальоту, використовуючи властивості етанової кислоти? Запишіть рівняння реакції в молекулярній та йонно-молекулярній формах. Які ще органічні кислоти можна використовувати для видалення вапняного нальоту й накипу?
3.Бабуся висипала соду (натрій карбонат) і кухонну сіль в банки, і заплуталась, куди що висипала. Як, застосовуючи властивості оцтової кислоти, можна допомогти визначити де яка речовина?
Отож вважайте себе щасливими, бо, як сказав відомий психолог і педагог Ян Амос Коменський: « Вважаю нещасливий той день або час, коли ти не засвоїв нового і нічого не додав до своєї освіти»
V. Домашнє завдання. Повторити §33, впр. 403,405. Навчальний проект № 13
«Екотрофологія- наука про екологічно безпечне харчування
VІ. Підведення підсумків уроку
Учні висловлюються щодо досягнення мети уроку, вражень, які вони отримали від роботи.
-
Окреме "дякую" за додаткові питання.


про публікацію авторської розробки
Додати розробку
