Презентація "Багатоатомні спирти"


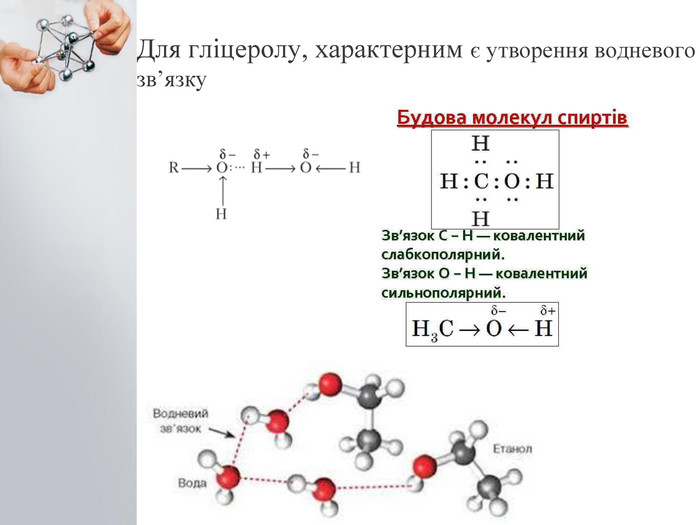

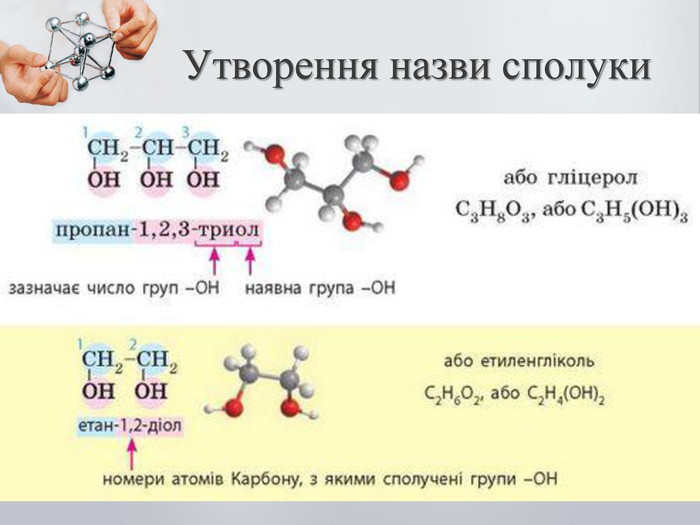
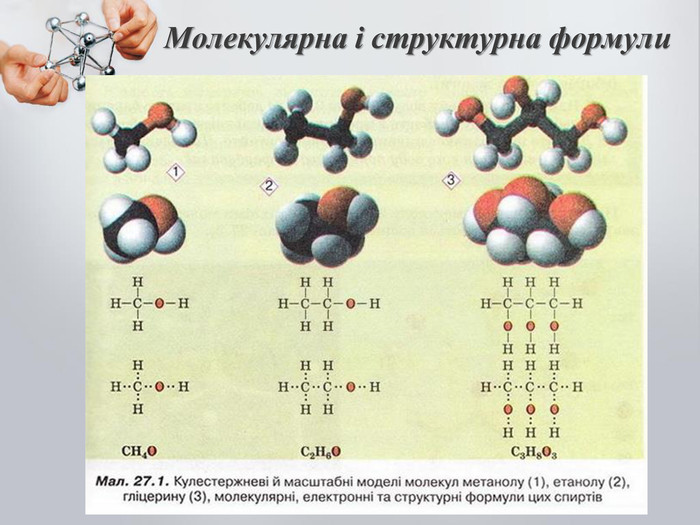

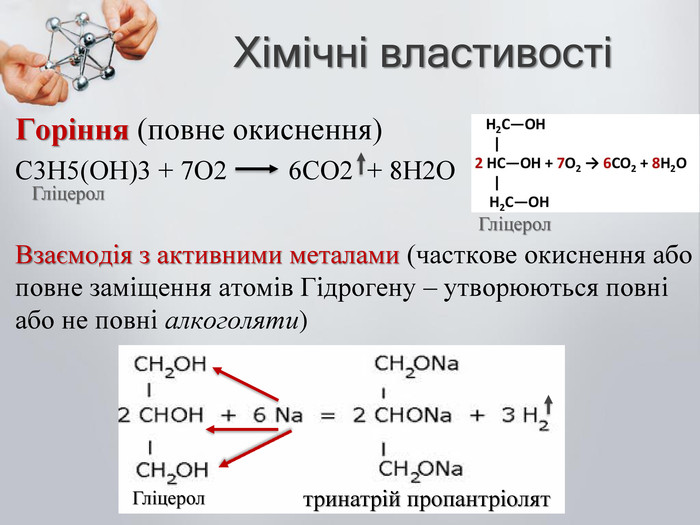


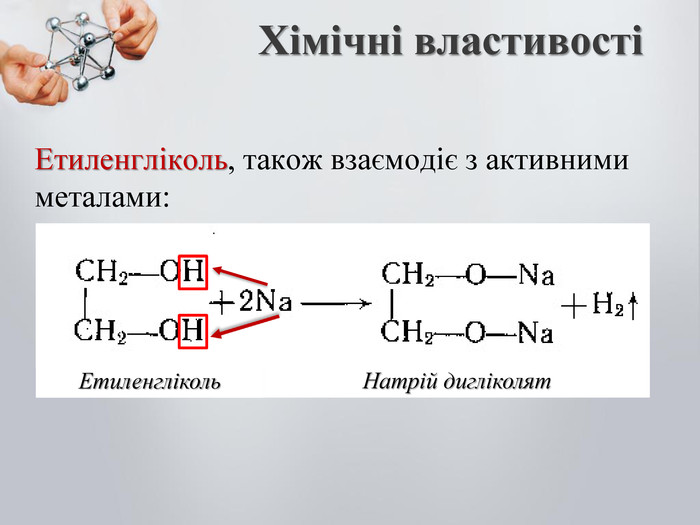
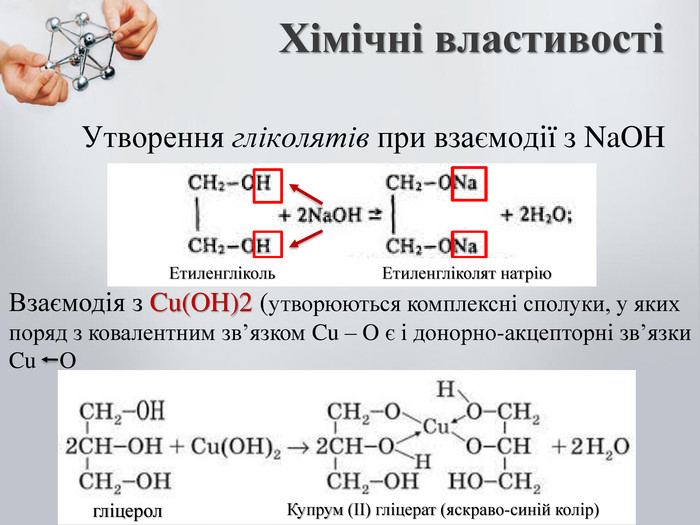

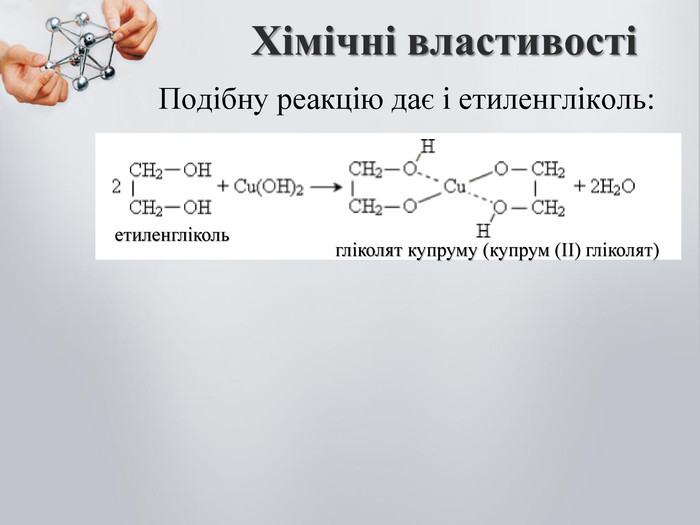
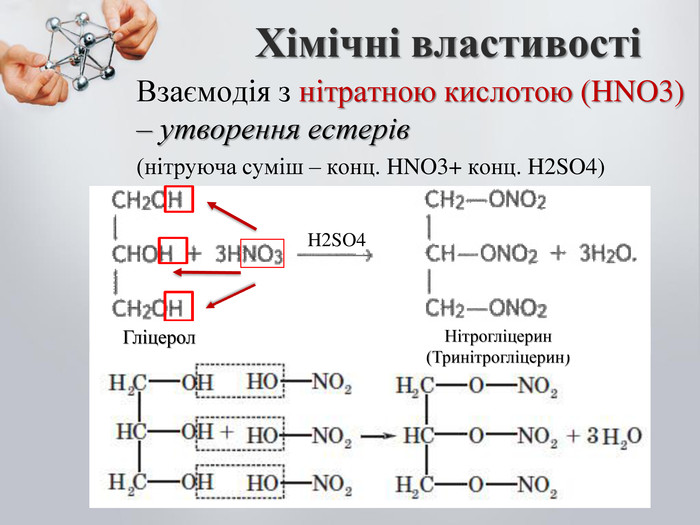
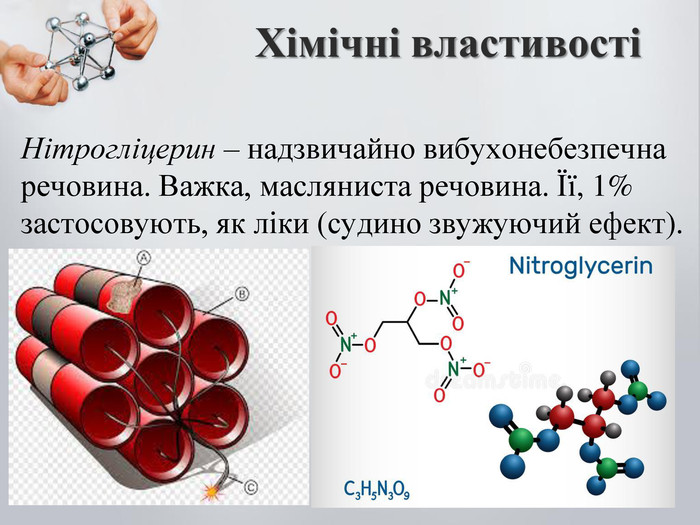


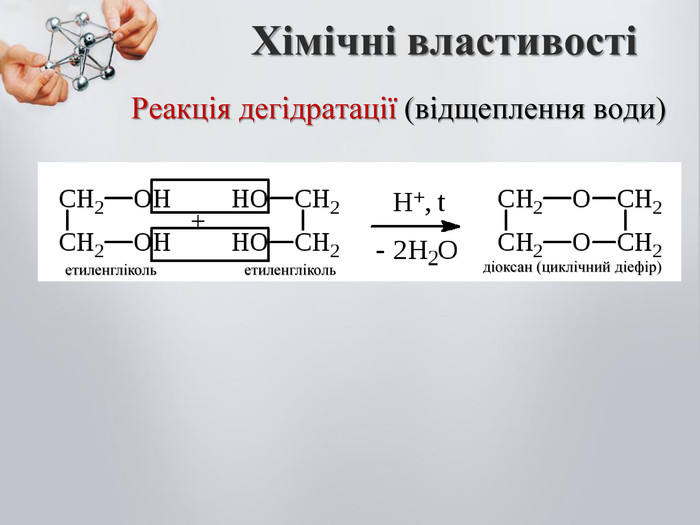







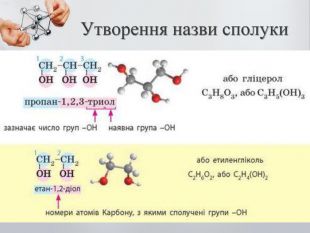
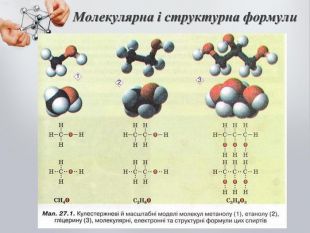
До бгатоатомних спиртів належать спирти із двома і більше гідроксильними групами (ОН). Загальна формула: CnH2n(OH)2 – двохатомний спирт CnH2n(OH)3 – трьохатомний спирт Номенклатура: Двохатомні спирти називають – діолами або гліколятами; Триатомні спирти називають – тріолами або гліцеролами; Ізомерія: Карбонового скелета; Положення функціональної групи (ОН) Багатоатомні насичені спирти
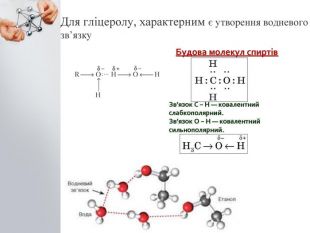
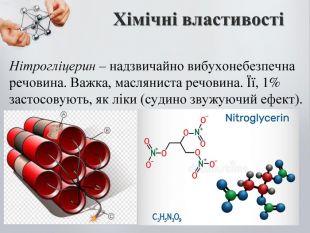
Фізичні властивості Етиленгліколь: Безбарвна, в’язка рідина; Солодкий на смак; Температура плавлення – 11,5℃; Температура кипіння – 197,8℃; Добро розчинний у воді. Отруйний. Гліцерин: Безбарвна, в’язка, гігроскопічна рідина; Солодка на смак; Змішується з водою у будь-якому співвідношенні; Температура плавлення - 18℃; Температура кипіння - 290℃.
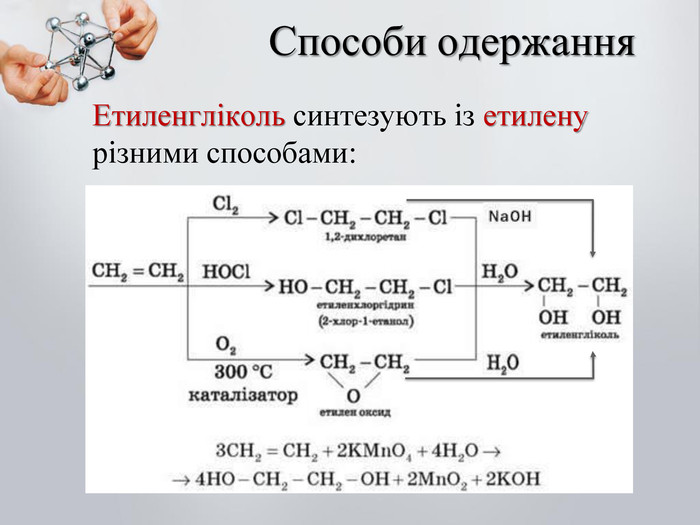
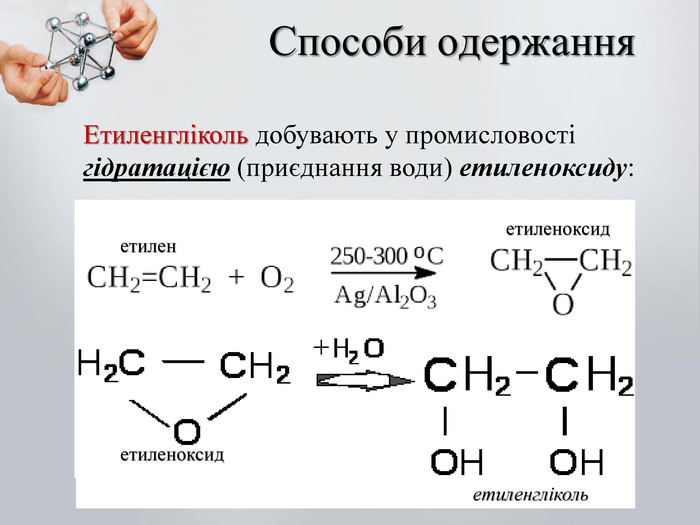
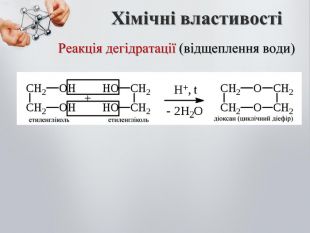
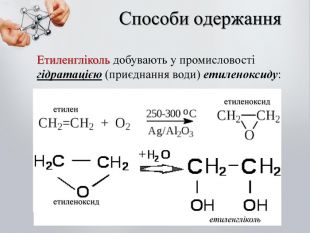
Гліцерол добувають синтетично з пропілену (C3H6) за такою схемою: CH2═CH – CH3 →CH2═CH – CH2OH → CH2OH – CHOH – CH2OH Пропілен Аліловий спирт Гліцерол Етиленгліколь утворюється під час пропускання етилену крізь розчин перманганату калію (KMnO4), при цьому відбуваються окислення і гідратація етилену: 1,2-етандіол (Етиленгліколь) Етан
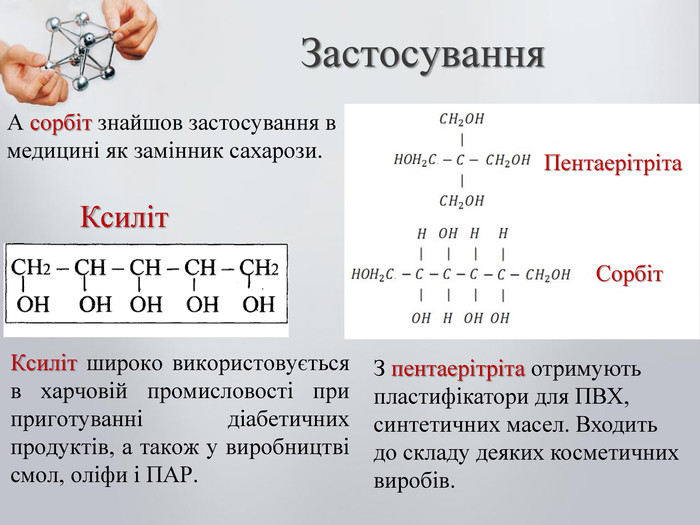
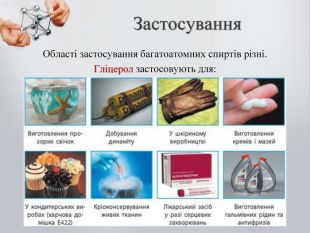
Ксиліт широко використовується в харчовій промисловості при приготуванні діабетичних продуктів, а також у виробництві смол, оліфи і ПАР. Ксиліт З пентаерітріта отримують пластифікатори для ПВХ, синтетичних масел. Входить до складу деяких косметичних виробів. А сорбіт знайшов застосування в медицині як замінник сахарози. Застосування Пентаерітріта Сорбіт


про публікацію авторської розробки
Додати розробку








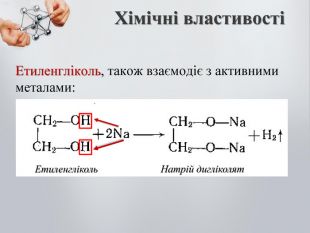
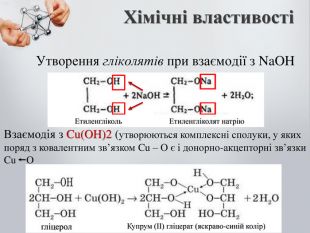

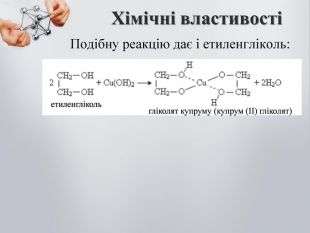
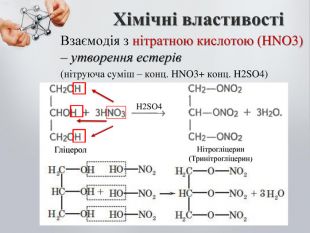










-

Колесник Наталія Іванівна
08.12.2024 в 10:28
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Велика Наталія Миколаївна
22.11.2022 в 23:04
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Климась Елена
08.11.2022 в 06:52
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

коверко ірина
30.01.2022 в 13:47
Дякую. Як би було прикріплено і відео, було б просто супер!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Труш Олена Олександрівна
28.11.2021 в 15:40
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Беловарі Магдалина
13.12.2020 в 16:34
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Yacenko Olena
30.11.2020 в 12:30
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 4 відгука