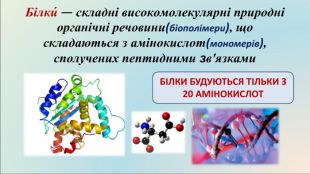
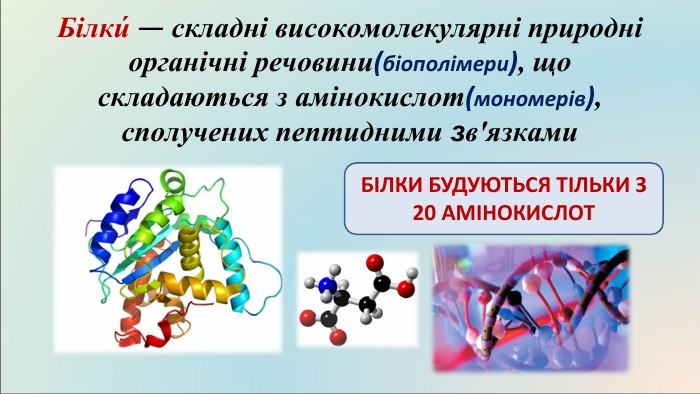
Презентація "Білки: склад, будова і властивості. Біологічна роль білків"


















Історія дослідження білку Антуан Франсуа де Фуркруа,французький хімік основоположник дослідження білків. Герман Еміль Фішер,німецький учений Білки були виділені в окремий клас біологічних молекул у XVIII столітті в результаті робіт французького хіміка Антуана де Фуркруа та інших учених, в яких було відмічено властивість білків коагулювати при нагріванні або під дією кислот. У той час були досліджені такі білки, як альбумін з яєчних білків, фібрин з крові і глютен із зерна пшениці. Герман Фішер у 1902 р. отримав Нобелівську премію за дослідження здатності амінокислот сполучатися між собою та проведення синтезу пептиду з вісімнадцяти α –амінокислот.
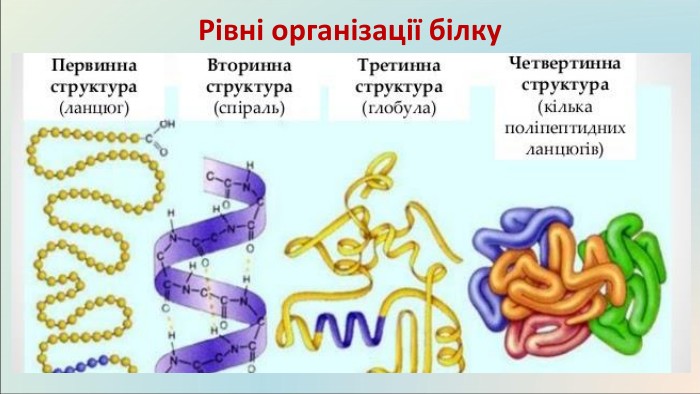
У 1934 р. Лайнус Полінг разом з А. Е. Мірскі сформулював теорію будови та функцій білка. В 1936 р. він почав вивчати атомні та молекулярні структури білків та амінокислот із використанням рентгенівської кристалографії. Голландський хімік Герріт Мульдер провів аналіз складу білків і виявив, що практично всі білки мають однакову емпіричну формулу. Мульдер також визначив продукти руйнування білків — амінокислоти — і для однієї з них (лейцину) майже точно визначив молекулярну масу — 131 дальтон. Історія дослідження білку Наш співвітчизник Іван Якович Горбачевський один із серед перших учених висловив думку про утворення білкових молекул з α-амінокислот
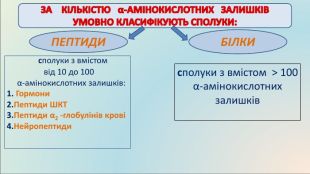
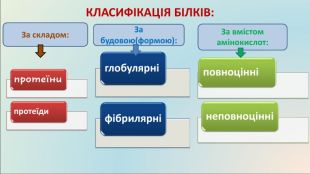
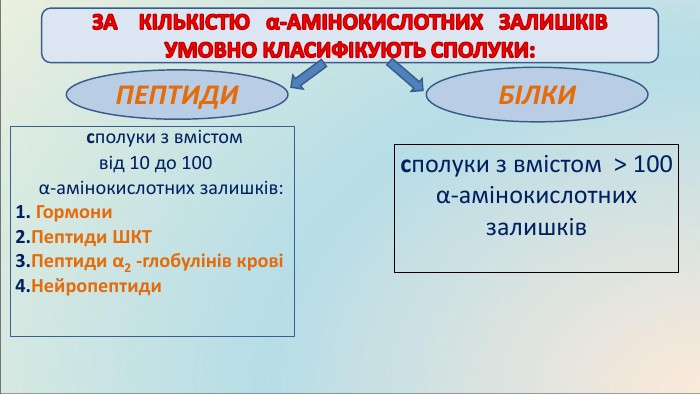
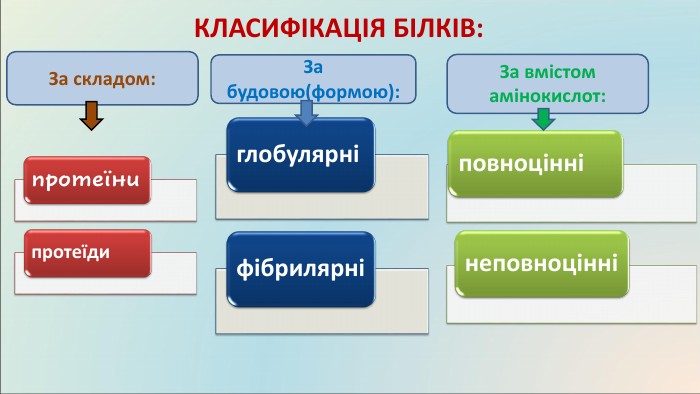
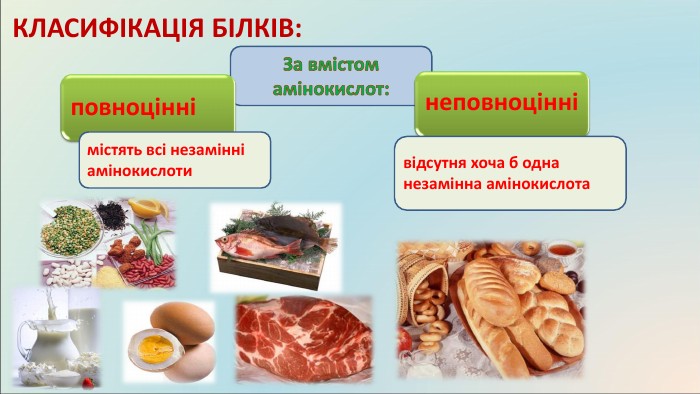
КЛАСИФІКАЦІЯ БІЛКІВ: За складом:прості білки, складаються із залишків амінокислот, утворюючи поліпептидний ланцюг: Альбуміни добре розчиняються у воді. Зустрічаються в молоці, яєчному білку і крові. Глобуліни у воді не розчиняються, але розчиняються в розбавлених розчинах солей. До глобулінів належать глобуліни крові і м’язовий білок міозин. Глутеліни розчиняються лише в розбавлених розчинах лугів. Зустрічаються в рослинах. Склеропротеїни – нерозчинні білки. До склеропротеїнів відносяться кератин волосся, білок шкіри і сполучних тканин колаген, білок натурального шовку фіброїн. ПІД ЧАС РУЙНУВАННЯ УТВОРЮЮТЬСЯ α – АМІНОКИСЛОТИ (амінокислоти, у яких аміногрупа розташована біля першого після карбоксильної групи атома Карбону)складні білки, крім залишків амінокислот містять залишки речовин небілкової природи: Глікопротеїди –містять вуглеводи (входять до складу мембран клітин, імуноглобуліни, муцин слини). Ліпопротеїди –містять ліпіди, транспортують холестерин та інші стероїди. Входять до складу хрящів, рогів, слини. Фосфопротеїди – містять залишки фосфорної кислоти (казеїн молока). Нуклеопротеїди – комплекс білка з нуклеїновими кислотами (хромосоми, рибосоми). Нуклеопротеїди є важливою складовою частиною вірусів – збудників багатьох хвороб. Хромопротеїди – містять забарвлену групу, беруть участь у фотосинтезі і клітинному диханні (каталаза, цитохром). Металопротеїди - містять іони металів (гемоглобін – йони Феруму,що надає забарвлення червоним кров’яним тільцям; ферменти). ПІД ЧАС РУЙНУВАННЯ УТВОРЮЮТЬСЯ α - і β - АМІНОКИСЛОТИ
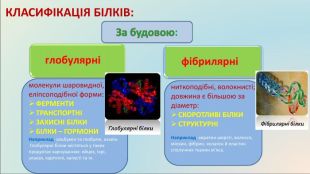
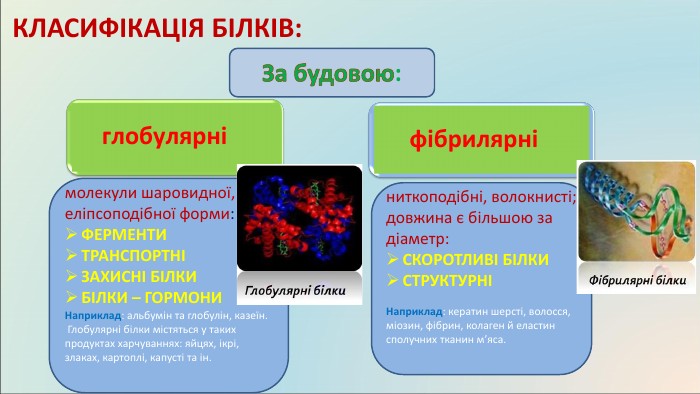
КЛАСИФІКАЦІЯ БІЛКІВ: За будовою: глобулярні фібрилярнімолекули шаровидної, еліпсоподібної форми: ФЕРМЕНТИТРАНСПОРТНІЗАХИСНІ БІЛКИБІЛКИ – ГОРМОНИНаприклад: альбумін та глобулін, казеїн. Глобулярні білки містяться у таких продуктах харчуваннях: яйцях, ікрі, злаках, картоплі, капусті та ін.ниткоподібні, волокнисті; довжина є більшою за діаметр: СКОРОТЛИВІ БІЛКИСТРУКТУРНІНаприклад: кератин шерсті, волосся, міозин, фібрин, колаген й еластин сполучних тканин м’яса.
Функції білків{5 C22544 A-7 EE6-4342-B048-85 BDC9 FD1 C3 A}Функції білківЇї суть. Приклади білків. Будівельна. Будівельний матеріал клітин і тканин. Колаген, мембранні білки. Транспортна. Переносять різноманітні речовини. Гемоглобін, що переносить кисень до тканин і вуглекислий газ від них. Міоглобін – накопичує кисень у м’язах. Захисна. Знешкоджують чужорідні речовини. Гамма-глобулін сироватки кровіЕнергетична Постачають енергію в організм. При розщепленні 1г білка вивільняється 17,6 к. Дж енергіїКаталітична. Прискорюють хімічні реакції в організміУсі ферменти за своєю природою є білками, наприклад рибонуклеаза. Рушійна. Забезпечують усі види руху, що виконують клітини та органи і організми. Міозін (білок м’язів)Регуляторна. Регулюють обмінні процеси. Гормони, наприклад інсулін. Білки відіграють велику роль у процесах росту, розмноження, передачі організмом спадкових властивостей
Хімічні властивості білків 1. Гідроліз (кислотно-основний, ферментативний), у лабораторних умовах можна здійснити , вдавшись до нагрівання білка із сильними кислотами або лугами, що призводить до розщеплення поліпептидних зв'язків з утворенням вільних амінокислот: У клітинах живих організмів відбувається гідроліз білків за участі каталізаторів (ферментів), більшість із яких – білкового походження. ферментибілок + n. H2 O суміш α-амінокислот
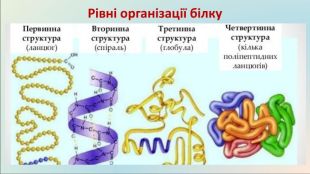
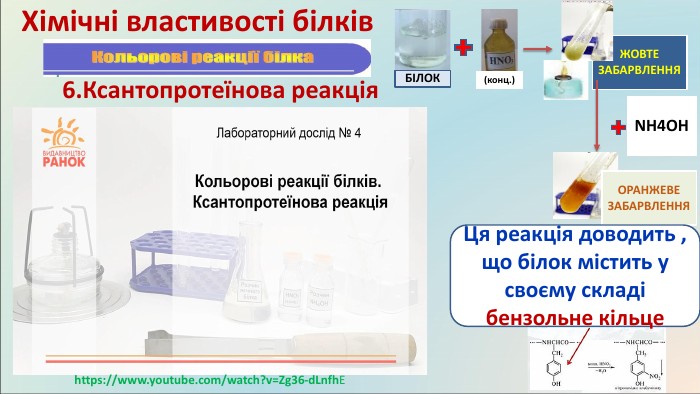
2. Денатурація білків – порушення природної структури білка під дією нагрівання і хімічних реагентів: а) висока або низька температура; б) механічний вплив; в) опромінення; г) отрути; д) дія спирту; є) дія солей важких металів(Pb, Hg та ін.) Під час приготування яєчні, смаження м’яса чи риби первинна структура білкових молекул зберігається, тоді як інші структури руйнуються. Більшість білків не витримує високого нагрівання. Ось чому під час різних захворювань людини, температура тіла, що перевищує 400 С , НЕБЕЗПЕЧНА ДЛЯ ЖИТТЯ3. Ренатурація білків – часткове руйнування природної структури білка, яке відновлюється при зміні умов існування 4. Деструкція білків – необоротний процес руйнування первинної структури білків
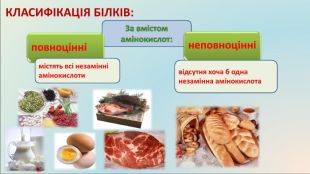
Значення білків: Насамперед білки — це харчові продукти. Цінним продуктом, що забезпечує організм білком, є курячі яйця. До білка курячих яєць входять усі вісім незамінних амінокислот:валін, метіонін, триптофан, лізин, фенілаланін, ізолейцин, лейцин, треонін. За дієтичного харчування норма вживання білків становить 90-120 г на добу. Дієтичне харчування зі збалансованою кількістю білків у раціоні має велике значення для зміцнення імунітету людини, бо створює протидію хвороботворним бактеріям.
Значення білків: Білки та білкові препарати застосовують як лікувальні засоби. Велике значення для зміцнення імунної системи має застосування гамма-глобуліну. Фармацевтичний препарат гамма-глобуліну створює тимчасовий імунітет проти багатьох інфекційних захворювань. Зокрема, його використовують для профілактики та лікування кору та кашлюку в дітей.
Значення білків У промисловості білки є цінною сировиною для різних виробництв. З шерсті й шовку виготовляють тканини. Із панцерів черепах і рогів тварин виробляють дрібні речі — гребінці, ґудзики, прикраси для інтер'єрів. Білки кісток, хрящів і обрізків шкіри при кип'ятінні з водою утворюють клей.
Висновки:7. Білки є насамперед незамінним пластичним матеріалом, потрібним для побудови клітини і тканини.8. Білки відіграють велику роль у процесах росту, розмноженням, передачі організмом спадкових властивостей. 9. Білки входять до складу ферментів і гормонів. 10. Білки, як і жири та вуглеводи, є важливим джерелом енергії в організмі.
-
 Фертак Наталя Володимирівна 09.04.2025 в 23:00Загальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0
Фертак Наталя Володимирівна 09.04.2025 в 23:00Загальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0


про публікацію авторської розробки
Додати розробку