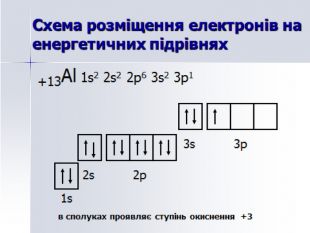
Презентація до уроку "Алюміній: фізичні та хімічні властивості"
Про матеріал
Презентація до уроку "Алюміній: фізичні та хімічні властивості"
Презентація містить експрес-тест для актуалізації опорних знань, основний та додатковий матеріал з теми, історичні відомості, міжпредметні зв'язки, цікаві факти, завдання для закріплення, домашнє завдання. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку