Презентація до уроку "Будова та властивості твердих тіл. Анізотропія кристалів. Рідкі кристали. "

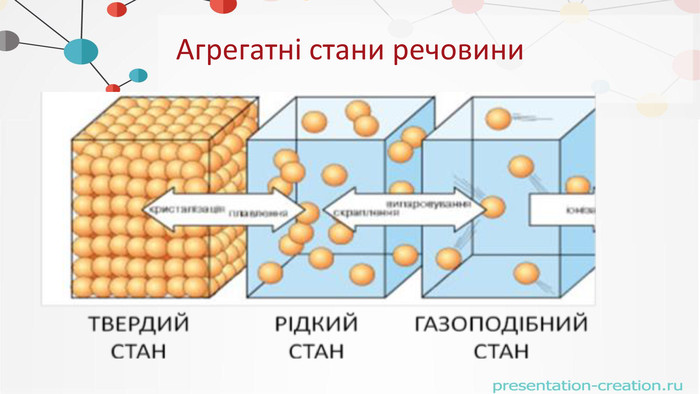




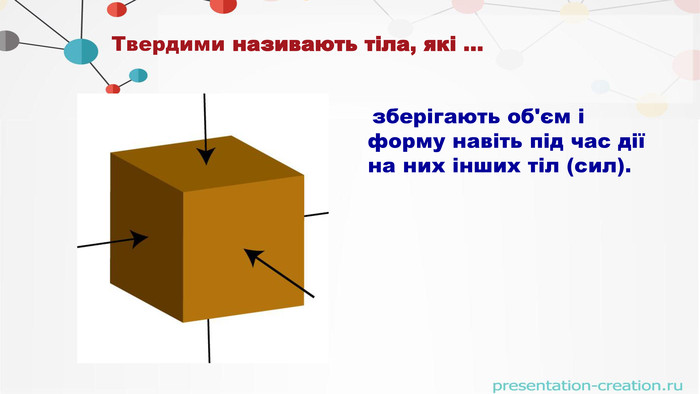

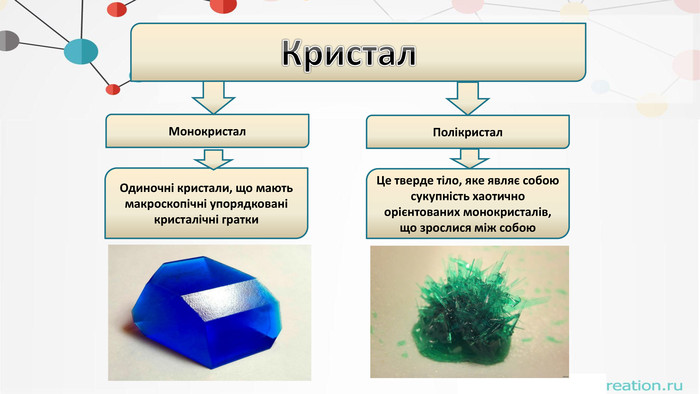





































. Що таке кристали?Кристали – це тверді тіла, атоми чи молекули яких, займають певне впорядковане положення в просторі У кристалічних речовинах частинки речовини розташовані в чітко визначеному порядку. Якщо з‘єднати центри положень рівноваги, то вийде правильна просторова гратка, яку називають кристалічною.
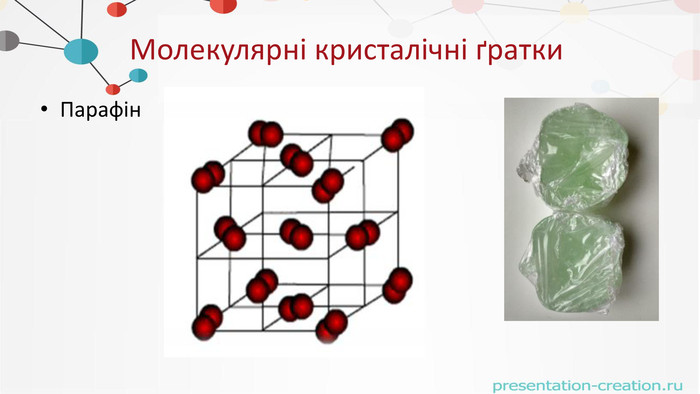
Типи кристалічних граток{21 E4 AEA4-8 DFA-4 A89-87 EB-49 C32662 AFE0}Тип кристалів. Що знаходиться у вузлах кристалічних решіток. Приклади кристалівІонніІони розміщуються почергово з протилезними зарядами. Сіль Na. Cl. АтомніНейтралні атоми, які утримуються ковалентними зв`язками квантово- механічного походження. Алмаз. МеталічніПозитивні іони (між вузлами електронний газ). Метали з високою електропровідністю. МолекулярніНейтронні молекули, які взаємодіють за рахунок зміщення електронних оболонок атомів. Парафін, Br2, CH4
Кристали утворюються в природних умовах і штучно. В природних умовах багато кристалів утворилось внаслідок охолодження рідкої речовини земної кори – магми, що є розплавом різних речовин. Багато мінералів виникли з перенасичених водних розчинів. Штучні кристали можна здобути із розплаву шляхом кристалізації з розчину і газу.
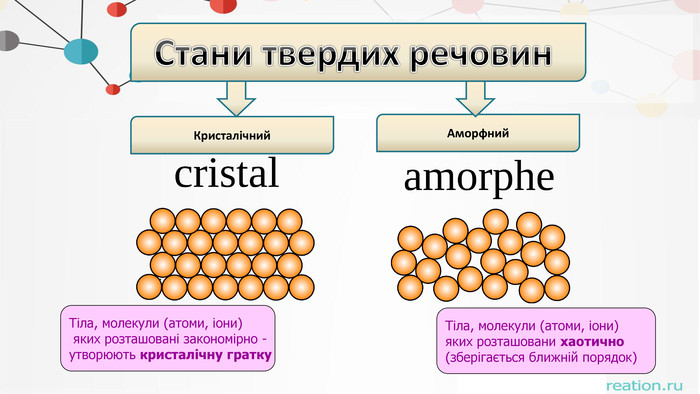
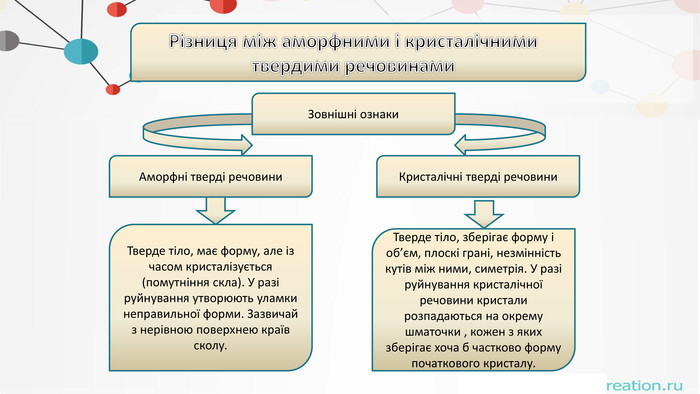
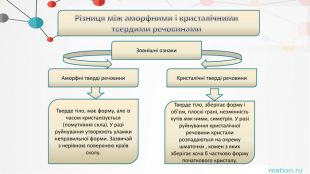
. Різниця між аморфними і кристалічнимитвердими речовинами. Зовнішні ознаки. Аморфні тверді речовини. Кристалічні тверді речовини. Тверде тіло, має форму, але із часом кристалізується (помутніння скла). У разі руйнування утворюють уламки неправильної форми. Зазвичай з нерівною поверхнею країв сколу. Тверде тіло, зберігає форму і об’єм, плоскі грані, незмінність кутів між ними, симетрія. У разі руйнування кристалічної речовини кристали розпадаються на окрему шматочки , кожен з яких зберігає хоча б частково форму початкового кристалу.
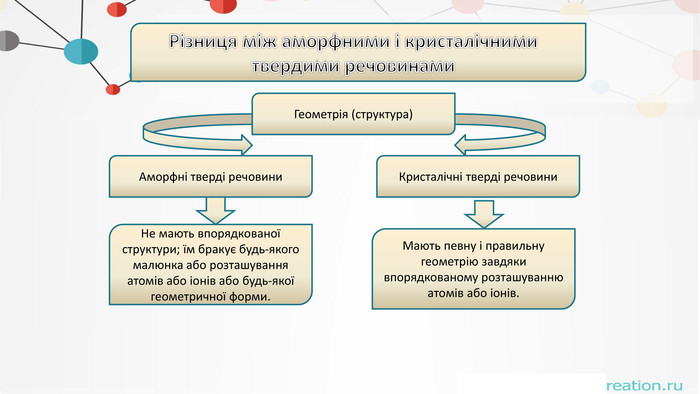
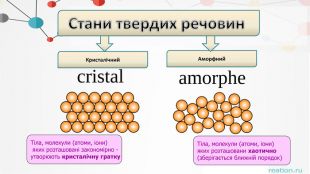
. Різниця між аморфними і кристалічнимитвердими речовинами. Геометрія (структура)Аморфні тверді речовини. Кристалічні тверді речовини. Не мають впорядкованої структури; їм бракує будь-якого малюнка або розташування атомів або іонів або будь-якої геометричної форми. Мають певну і правильну геометрію завдяки впорядкованому розташуванню атомів або іонів.
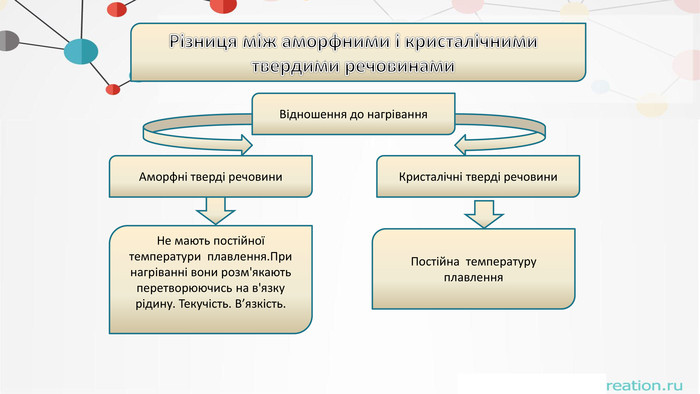
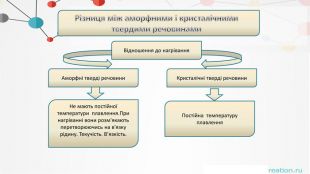
. Різниця між аморфними і кристалічнимитвердими речовинами. Відношення до нагрівання. Аморфні тверді речовини. Кристалічні тверді речовини. Не мають постійної температури плавлення. При нагріванні вони розм'якають перетворюючись на в'язку рідину. Текучість. В’язкість. Постійна температуру плавлення
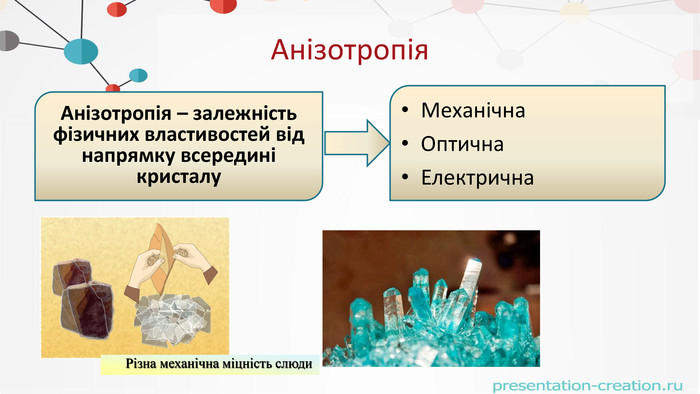
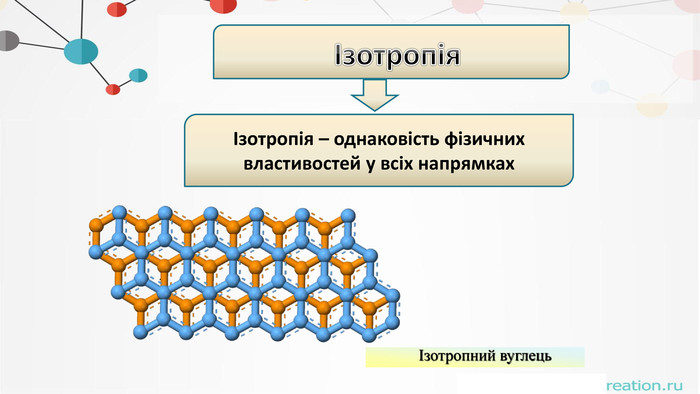
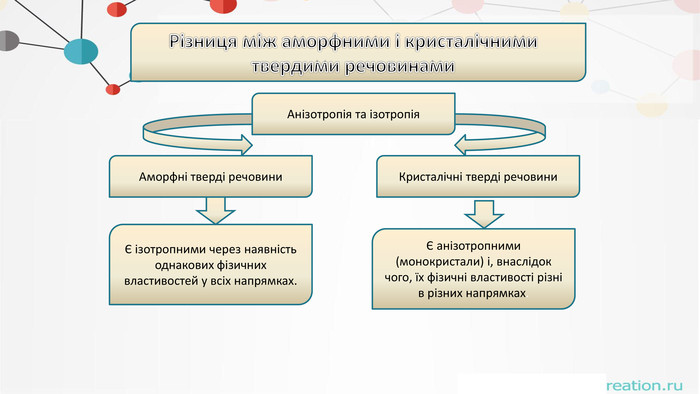
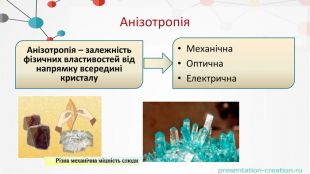
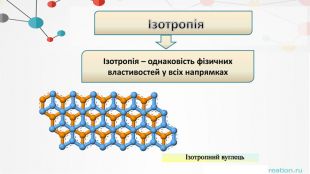
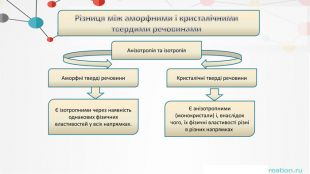
. Різниця між аморфними і кристалічнимитвердими речовинами. Анізотропія та ізотропія. Аморфні тверді речовини. Кристалічні тверді речовиниЄ ізотропними через наявність однакових фізичних властивостей у всіх напрямках.Є анізотропними (монокристали) і, внаслідок чого, їх фізичні властивості різні в різних напрямках.
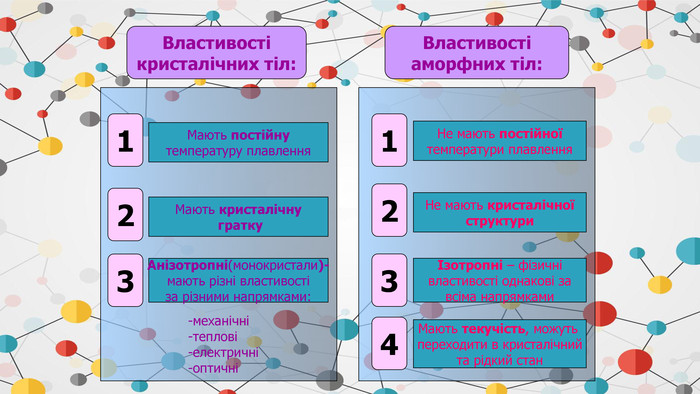
Властивостікристалічних тіл: Властивостіаморфних тіл:1231 Мають постійнутемпературу плавлення23 Мають кристалічну гратку. Анізотропні(монокристали)-мають різні властивостіза різними напрямками: Не мають постійноїтемператури плавлення. Не мають кристалічноїструктуриІзотропні – фізичнівластивості однакові завсіма напрямками-механічні-теплові-електричні-оптичні4 Мають текучість, можуть переходити в кристалічнийта рідкий стан
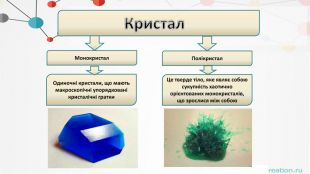
Отже ….1. Що називають кристалами?2. Які види кристалів ви знаєте?3. Що називають монокристалами? Наведіть приклади.4. Що називають полікристалами? Наведіть приклади.5. Що називають анізотропією? Ізотропією?6. Що таке аморфні тіла?Наведіть приклади.7. Які кристали називаються рідкими? Де вони використовуються
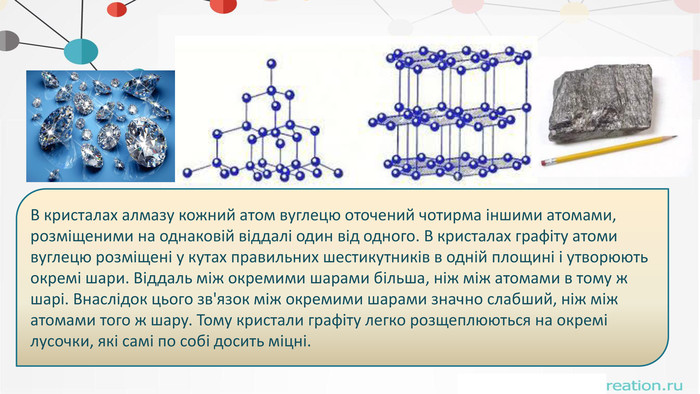
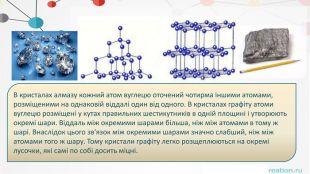
. В кристалах алмазу кожний атом вуглецю оточений чотирма іншими атомами, розміщеними на однаковій віддалі один від одного. В кристалах графіту атоми вуглецю розміщені у кутах правильних шестикутників в одній площині і утворюють окремі шари. Віддаль між окремими шарами більша, ніж між атомами в тому ж шарі. Внаслідок цього зв'язок між окремими шарами значно слабший, ніж між атомами того ж шару. Тому кристали графіту легко розщеплюються на окремі лусочки, які самі по собі досить міцні.
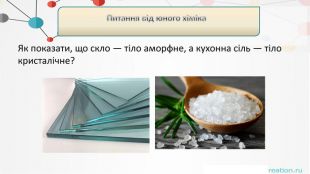
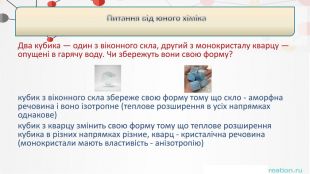
Два кубика — один з віконного скла, другий з монокристалу кварцу — опущені в гарячу воду. Чи збережуть вони свою форму? кубик з віконного скла збереже свою форму тому що скло - аморфна речовина і воно ізотропне (теплове розширення в усіх напрямках однакове) кубик з кварцу змінить свою форму тому що теплове розширення кубика в різних напрямках різние, кварц - кристалічна речовина (монокристали мають властивість - анізотропію) Питання від юного хіміка
Домашнє завдання: Опрацювати параграф §34 Підготувати повідомлення з тем: “Виготовлення штучних алмазів”“Як працює ЖК монітор?”Розпочати роботу над проектом по вирощуванню кристалів в домашніх умовах , створити презентацію проекту https://naurok.com.ua/prezentaciya-proekt-viroschuvannya-kristaliv-soley-154327.html http://www.myshared.ru/slide/1408072/https://www.youtube.com/watch?v=9t. WRw. Rvgg-M


про публікацію авторської розробки
Додати розробку















































-

Рохманова Людмила Федорівна
02.02.2026 в 21:40
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Клепікова Ольга Анатоліївна
22.02.2025 в 14:29
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Ковальчук Наталія
04.03.2024 в 22:45
Дуже розгорнуто і цікаво.
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

сусь надія
22.10.2023 в 13:35
Щиро дякую
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 1 відгук