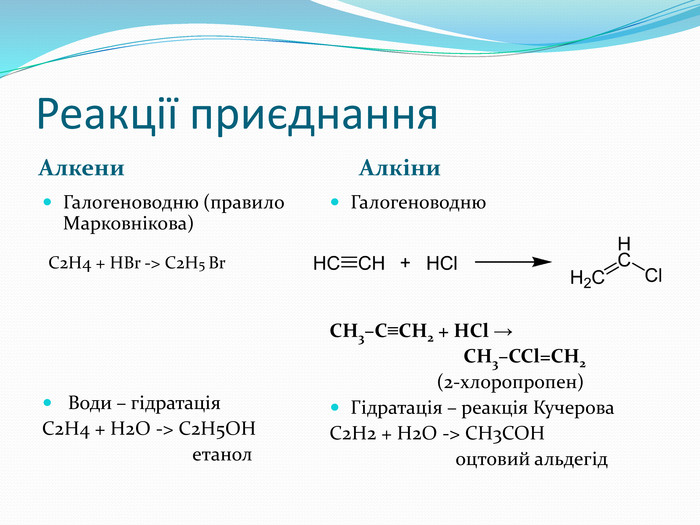
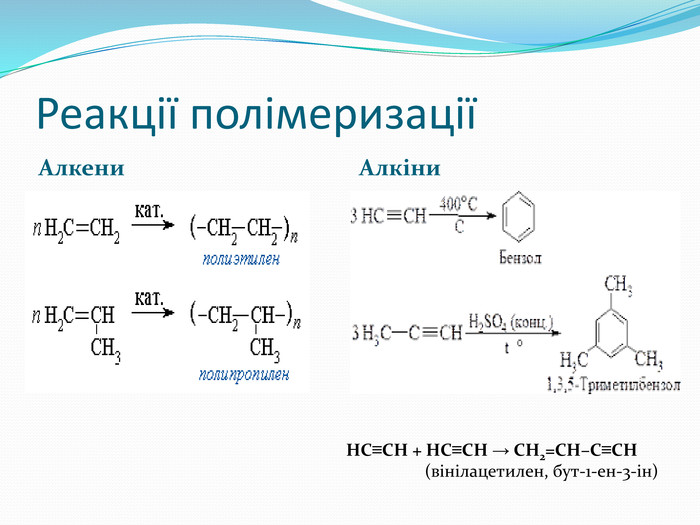
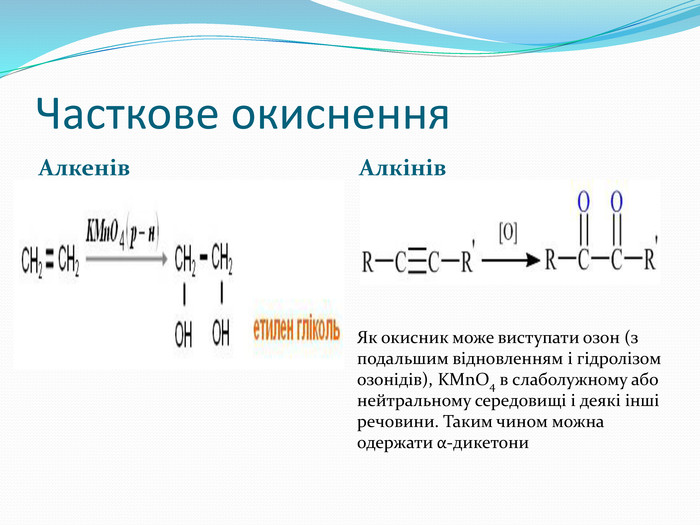
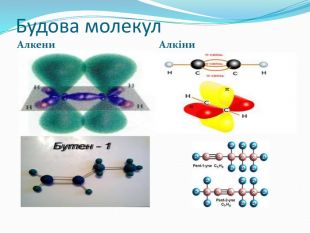
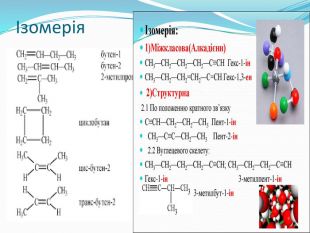
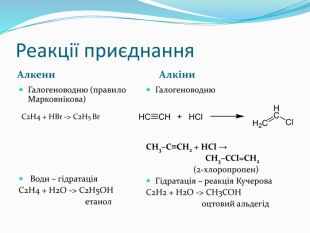
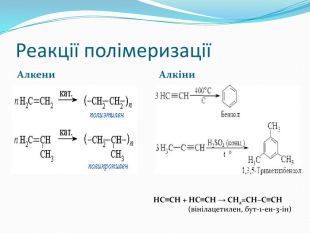
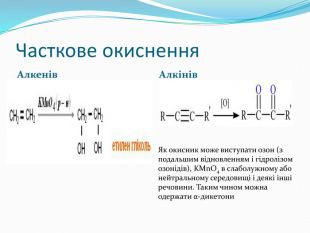
Презентація до уроку хімії 10 клас "Ненасичені вуглеводні"
Про матеріал
Презентація до уроку хімії в 10 класі за новою програмою на тему "Ненасичені вуглеводні". Завдання, на які посилається презентація в розділі закріплення знань та домашнє завдання з підручника "Хімія-10 клас" (рівень стандарту), П.П.Попель, Л.С.Крикля - Київ: ВЦ "Академія" , 2018. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку