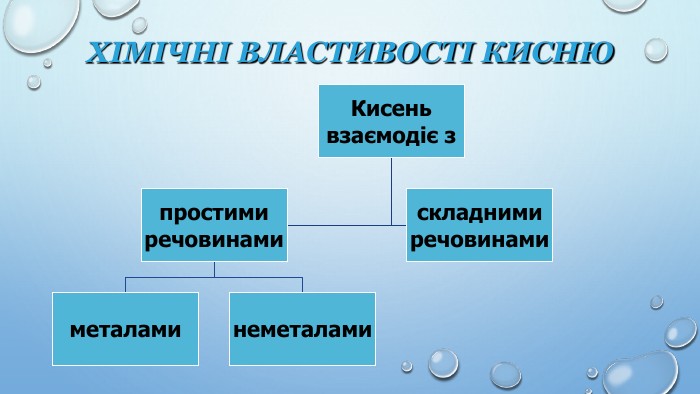
Презентація до уроку "Хімічні властивості Оксигену: взаємодія з простими речовинами"
Про матеріал
Презентація до уроку "Хімічні властивості Оксигену: взаємодія з простими речовинами" містить добірку відеодослідів на підтвердження хімічних властивостей Оксигену, добірку завдань на складання формул оксидів, рівнянь реакцій. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку