Презентація до уроку "Класифікація вуглеводів. Глюкоза: молекулярна формула та її відкрита форма, фізичні властивості. Хімічні властивості глюкози. Способи одержання глюкози та її"
















Тема уроку: Класифікація вуглеводів. Глюкоза: молекулярна формула та її відкрита форма, фізичні властивості. Хімічні властивості глюкози. Способи одержання глюкози та її застосування. Тема уроку: Класифікація вуглеводів. Глюкоза: молекулярна формула та її відкрита форма, фізичні властивості. Хімічні властивості глюкози. Способи одержання глюкози та її застосування.
Девіз уроку: Вивчай усе не заради марнославства, а заради практичної користі Г. Ліхтенберг«З давніх-давен люди вживали в харчування натуральний оцет, добутий з цукристих речовин та «кваснину»: квашені огірки, помідори, капусту, яблука, гриби. І не хворіли! На вашу думку, чому? Відповідь отримаємо в кінці уроку. Тож будьте уважні та зосереджені»
Творчі та дослідницькі завдання на урок1 учень. Дана речовина міститься в медові, спілих фруктах та ягодах, її розчин використовують для внутрівенного харчування хворих під час критичних ситуацій та в післяопераційний період. Вона дає якісні реакції на багатоатомні спирти та на альдегіди. Встановлено, що дана сполука містить w%(С) = 40%; w%(Н) = 6,67%; w%(О) = 53,33%; має молярну масу 180г/моль. Встановіть формулу речовини.2 учень. Скласти протягом уроку «портрет» глюкози в вигляді ессе.3 учень. Отримує наклейки з написами ( вуглеводів, моносахариди, полісахариди, глюкоза, класифікація, дисахариди, крохмаль, сахароза,фруктоза, лактоза, целюлоза). Біля дошки скласти схему «Класифікація вуглеводів» 4 учень. Досліджує фізичні властивості глюкози: колір, запах, агрегатний стан за певної температури, розчинність у воді, легкоплавкість та робить висновок про кристалічну гратку речовини, описує відомий йому з життя смак глюкози.
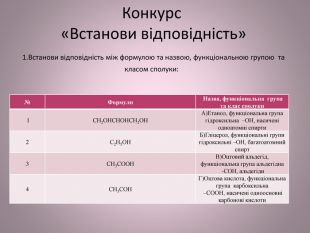
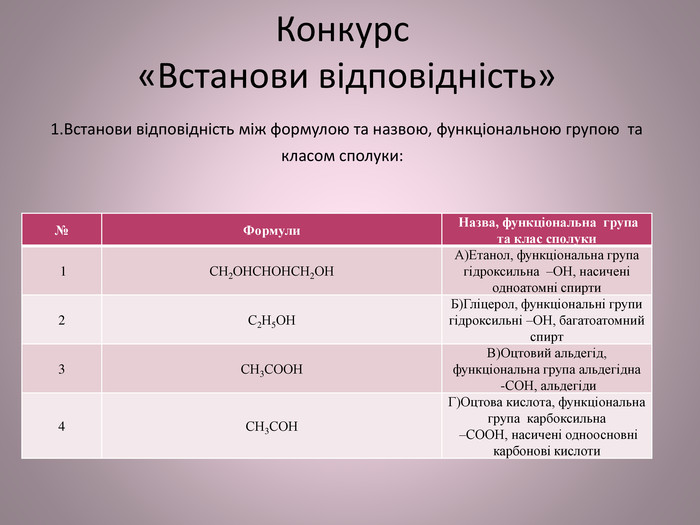
Конкурс «Встанови відповідність» 1. Встанови відповідність між формулою та назвою, функціональною групою та класом сполуки:{5 C22544 A-7 EE6-4342-B048-85 BDC9 FD1 C3 A}№Формули Назва, функціональна група та клас сполуки 1 СН2 ОНСНОНСН2 ОНА)Етанол, функціональна група гідроксильна –ОН, насичені одноатомні спирти2 С2 Н5 ОНБ)Гліцерол, функціональні групи гідроксильні –ОН, багатоатомний спирт3 СН3 СООНВ)Оцтовий альдегід, функціональна група альдегідна -СОН, альдегіди4 СН3 СОН Г)Оцтова кислота, функціональна група карбоксильна –СООН, насичені одноосновні карбонові кислоти
2. Встанови відповідність між класом сполук, функціональною групою та якісною реакцією на неї:{5 C22544 A-7 EE6-4342-B048-85 BDC9 FD1 C3 A}№Формули Назва, функціональна група та клас сполуки 1 СН2 ОНСНОНСН2 ОНГліцерол, функціональні групи гідроксильні –ОН, багатоатомний спирта) За допомогою свіжоосадженого купрум(ІІ) гідроксиду Cu(OH)2 при нагріванні або за допомогою реакції «срібного дзеркала». У разі окиснення купрум(ІІ) гідроксидом при нагріванні утворюється червоний осад Cu2 O.2 СН3 СОН Оцтовий альдегід, функціональна група альдегідна -СОН, альдегідиб)За допомогою свіжоосадженого купрум(ІІ) гідроксиду Cu(OH)2 без нагрівання. У результаті реакції до розчину даної речовини утворюється прозорий темно-синій розчин
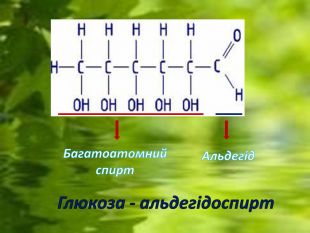
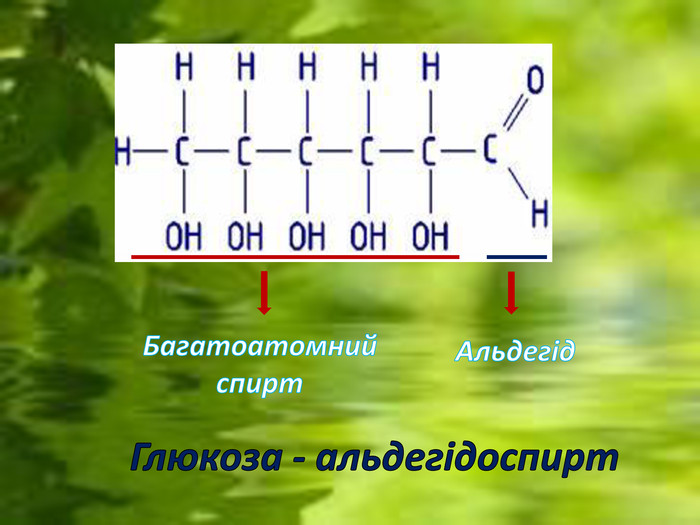
Проблемне питання: А чи може одна й та сама речовина давати якісну реакцію на багатоатомні спирти та альдегіди? Якщо так, то які функціональні групи будуть визначати її властивості? Яку будову вона матиме? Крім цього, дана речовина приєднує 5 моль карбонової кислоти. Тоді скільки гідроксильних груп вона матиме? Спробуймо і ми вирішити на уроці дане питання!
Перевірка завдань. Класифікація вуглеводів Cn(H2 O)m{5 C22544 A-7 EE6-4342-B048-85 BDC9 FD1 C3 A}Моносахариди. Дисахариди. Полісахариди Пенто́зи (від грец. πέντε — п'ять), C5 H10 O5 — органічні сполуки з групи моносахаридів, у молекулі яких є п'ять вуглецевих атомів. Кристалічні речовини, солодкі на смак, добре розчинні у воді. Входять до складу деяких глікозидів та полісахаридів рослин (арабіноза, ксилоза) а також нуклеїнових кислот (рибоза, дезоксирибоза). Залежно від наявності в молекулі альдегідної або кетонної групи їх поділяють на альдо- та кето- пентози. Використовують ухарчовій промисловості. Дисахариди — вуглеводи, які при нагріванні з водою в присутності мінеральних кислот чи під дією ферментів піддаються гідролізу, розкладаються на дві молекули моносахаридів. Буряковий та тростинний цукор (сахароза), С12 Н22 О11 — найважливіший із дисахаридів. Його добувають із цукрового буряку (в ньому знаходиться до 28 % сахарози від сухої речовини) або із цукрової тростини. Він є також у соках берези, клену й деяких фруктах. Сахароза — цінний харчовий продукт. Під час гідролізу вона розпадається з утворенням молекули глюкози й молекули фруктози. Мальтоза — це солодовий цукор, він складається з двох залишків глюкози. Дисахариди мають солодкий присмак. Вони, як і моносахариди, добре розчинні у воді. Полісахариди — це вуглеводи, які багато в чому відрізняються від моносахаридів і дисахаридів, не мають солодкого смаку і майже не розчинні у воді. Вони являють собою складні високомолекулярні сполуки, які під каталітичним впливом кислот чи ферментів піддаються гідролізу з утворенням простіших поліцукридів, потім дицукридів, і, зрештою, багато (сотні і тисячі) молекул моноцукридів. Важливі представники поліцукридів — крохмаль і целюлоза. Їх молекули побудовані з ланок -С6 Н10 О5-, є залишками шестичленних циклічних форм молекул глюкози, що втратили молекулу води, тому склад крохмалю й целюлози виражається однією формулою (С6 Н10 О5)X. Різниця у властивостях цих поліцукридів обумовлена просторовою ізомерією моноцукридних молекул: крохмаль побудований із ланок α-форми глюкози, а целюлоза — β-форми. Гексо́зи (від грец. ἕξ — шість), C6 H12 O6 — вуглеводи групи моносахаридів, молекули яких містять шість вуглецевих атомів. Є в тканинах рослин, тварин і людини у вільному стані, або входять до складу глікозидів і полісахаридів. Залежно від характеру карбонільної групи, гексози поділяють на альдогексози (наприклад, глюкоза, маноза, галактоза) і кетогексози (наприклад, фруктоза). Гексози — безбарвні або білі кристали, добре розчинні у воді. Вступають у реакції, характерні для карбонільних сполук (так, альдогексози дають реакцію срібного дзеркала — при нагріванні з реактивом Толленса утворюється металеве срібло). Одержують їх гідролізом полісахаридів (наприклад, крохмалю), а також синтетично. Застосовують у мікробіологічній і харчовій промисловості, в медицині.
Задача на виведення формули речовини. Дана речовина міститься в медові, спілих фруктах та ягодах, її розчин використовують для внутрівенного харчування хворих під час критичних ситуацій та в післяопераційний період. Вона дає якісні реакції на багатоатомні спирти та на альдегіди. Встановлено, що дана сполука містить w%(С) = 40%; w%(Н) = 6,67%; w%(О) = 53,33%; має молярну масу 180г/моль. Встановіть формулу речовини.
Визначення функціональних груп у молекулі глюкози. ЛАБОРАТОРНИЙ ДОСЛІД № 2. Окиснення глюкози купрум(ІІ) гідроксидом.Інструктаж за інструкцією. Виконання: У пробірку налийте 2—3 мл розчину натрій гідроксиду і додайте 3—4 краплі розчину купрум(ІІ) сульфату. До осаду купрум(ІІ) гідроксиду, що утворився, долийте 2—3 мл розчину глюкози і добре перемішайте суміш. Що спостерігаєте? Вміст пробірки обережно нагрійте. Про що свідчить поява осаду і зміна його забарвлення? Зробіть відповідні висновки.
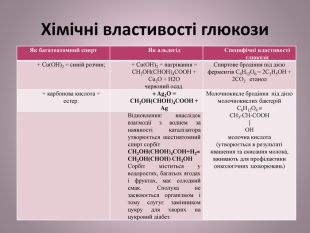
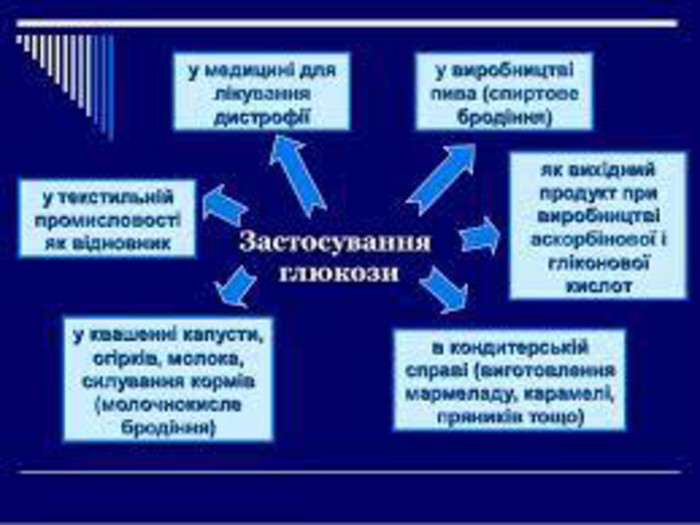
Хімічні властивості глюкози{5 C22544 A-7 EE6-4342-B048-85 BDC9 FD1 C3 A}Як багатоатомний спирт. Як альдегід. Специфічні властивості глюкози+ Сu(ОН)2 = синій розчин;+ Сu(ОН)2 + нагрівання = СН2 ОН(СНОН)4 СООН + Сu2 О + Н2 О червоний осад. Спиртове бродіння під дією ферментів С6 Н12 О6 = 2 С2 Н5 ОН + 2 СО2 етанол+ карбонова кислота = естер.+ Ag2 О = СН2 ОН(СНОН)4 СООН + Ag Молочнокисле бродіння під дією молочнокислих бактерій. С6 Н12 О6 =СН3-СН-СООН|ОНмолочна кислота(утворюється в результаті квашення та скисання молока, вживають для профілактики онкологічних захворювань)Відновлення: внаслідок взаємодії з воднем за наявності каталізатора утворюється шестиатомний спирт сорбіт. СН2 ОН(СНОН)4 СОН+Н2=СН2 ОН(СНОН) СН2 ОН Сорбіт міститься у водоростях, багатьох ягодах і фруктах, має солодкий смак. Сполука не засвоюється організмом і тому слугує замінником цукру для хворих на цукровий діабет.


про публікацію авторської розробки
Додати розробку