Презентація до уроку: "Кристалічні ґратки. Атомні, молекулярні та йонні кристали"



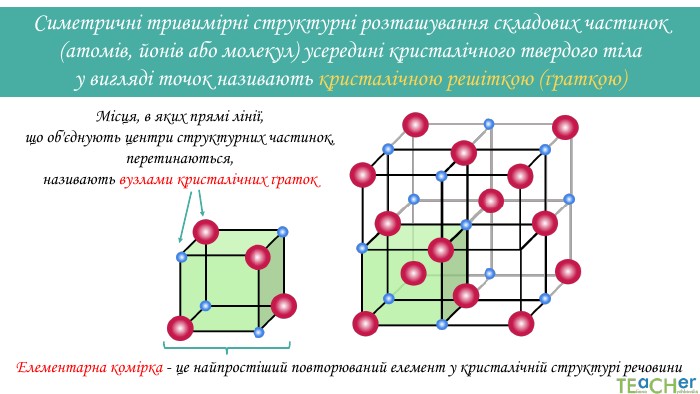



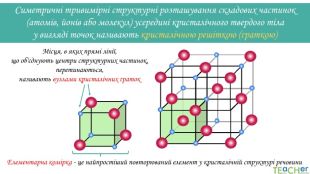
Симетричні тривимірні структурні розташування складових частинок (атомів, йонів або молекул) усередині кристалічного твердого тіла у вигляді точок називають кристалічною решіткою (ґраткою) Місця, в яких прямі лінії, що об'єднують центри структурних частинок, перетинаються, називають вузлами кристалічних ґраток. Елементарна комірка - це найпростіший повторюваний елемент у кристалічній структурі речовини
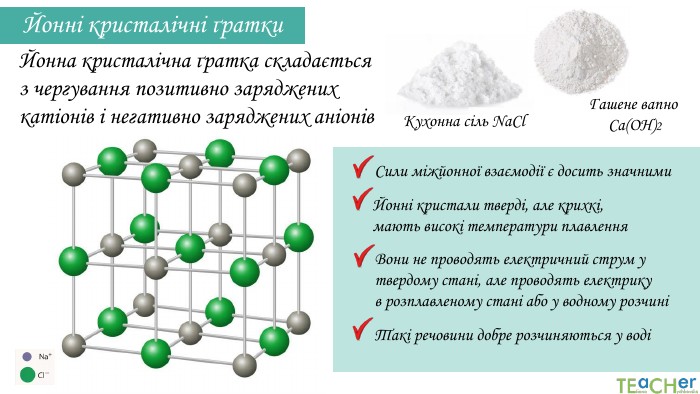
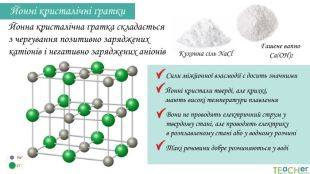
Йонні кристалічні ґратки. Йонна кристалічна ґратка складається з чергування позитивно заряджених катіонів і негативно заряджених аніонів. Сили міжйонної взаємодії є досить значними Йонні кристали тверді, але крихкі, мають високі температури плавлення. Вони не проводять електричний струм у твердому стані, але проводять електрику в розплавленому стані або у водному розчиніТакі речовини добре розчиняються у водіКухонна сіль Na. Cl Гашене вапно Са(ОН)2
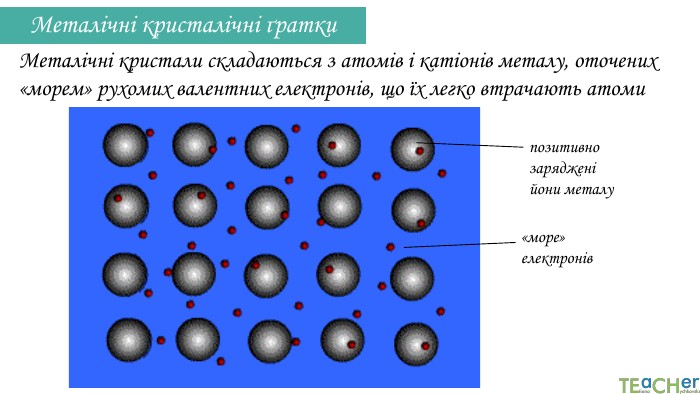
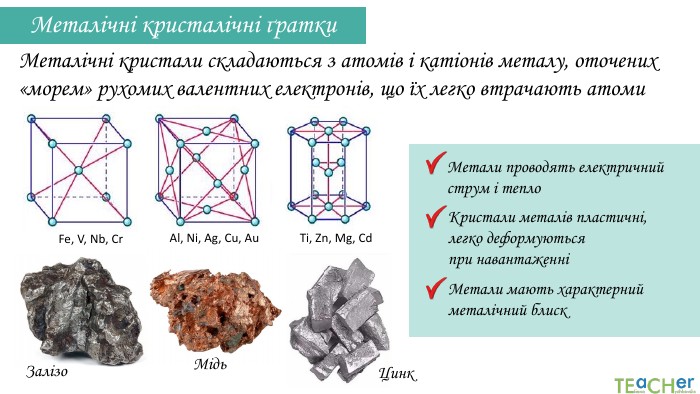
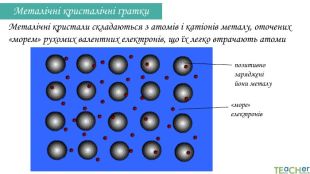
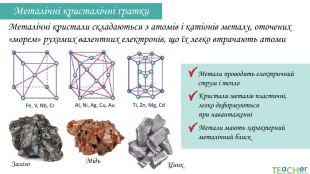
Металічні кристалічні ґратки. Метали проводять електричний струм і тепло Кристали металів пластичні, легко деформуються при навантаженніМетали мають характерний металічний блиск. Металічні кристали складаються з атомів і катіонів металу, оточених «морем» рухомих валентних електронів, що їх легко втрачають атоми. Fe, V, Nb, Cr. Al, Ni, Ag, Cu, Au. Ti, Zn, Mg, Cd. Залізо Мідь. Цинк
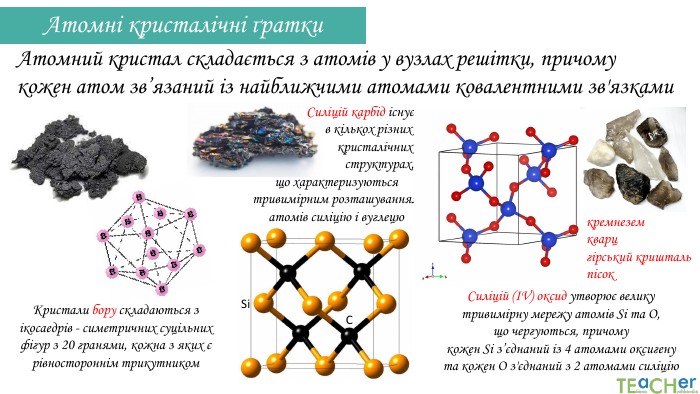
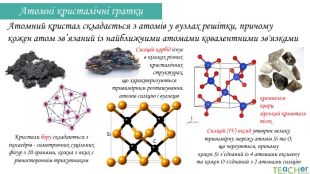
Атомні кристалічні ґратки. Атомний кристал складається з атомів у вузлах решітки, причому кожен атом зв’язаний із найближчими атомами ковалентними зв'язками. Кристали бору складаються з ікосаедрів - симетричних суцільних фігур з 20 гранями, кожна з яких є рівностороннім трикутником Si. C Силіцій карбід існує в кількох різних кристалічних структурах, що характеризуються тривимірним розташуванням атомів силіцію і вуглецю Силіцій (IV) оксид утворює велику тривимірну мережу атомів Si та O, що чергуються, причому кожен Si з’єднаний із 4 атомами оксигену та кожен O з'єднаний з 2 атомами силіціюкремнеземкварцгірський криштальпісок
Атомні кристалічні ґратки. У кристалічній ґратці алмазу кожен атом карбону утворює чотири зв'язки із сусідніми атомами. Атомні кристали тверді та крихкіУ речовин з атомною кристалічною ґраткою дуже високі температури плавлення і кипіння Атомні кристали практично нерозчинні, не проводять електрику в жодному агрегатному стані Температура плавлення кремнезему - 1710 °СТемпература плавлення графіту - 3900 °САтомний кристал складається з атомів у вузлах решітки, причому кожен атом зв’язаний із найближчими атомами ковалентними зв'язками
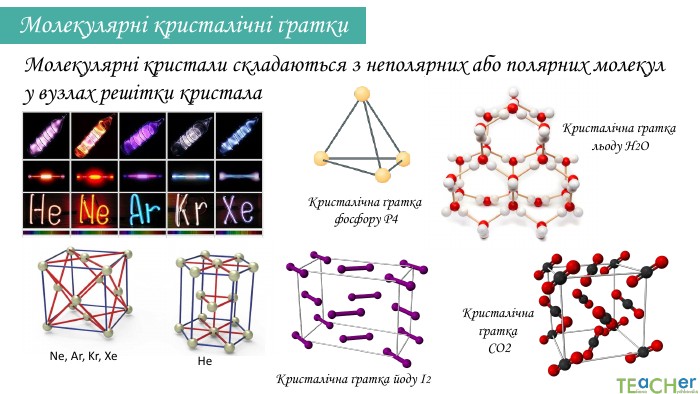
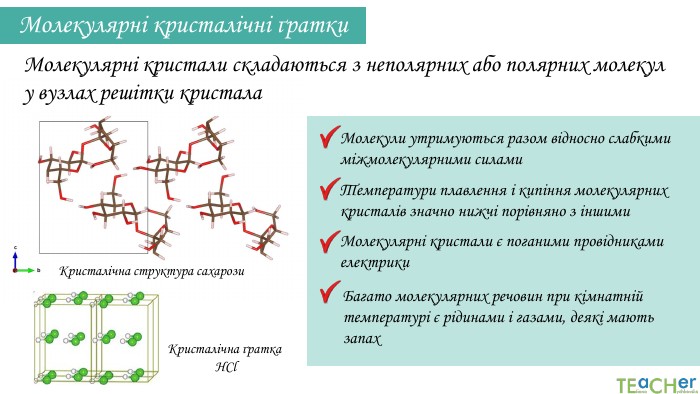
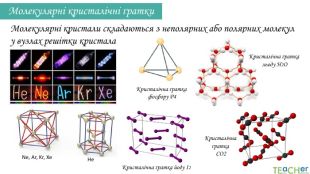
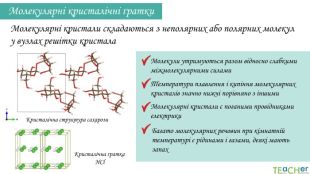
Кристалічна структура сахарози. Молекулярні кристалічні ґратки. Молекулярні кристали складаються з неполярних або полярних молекул у вузлах решітки кристала Кристалічна ґратка HCl. Молекули утримуються разом відносно слабкими міжмолекулярними силами Температури плавлення і кипіння молекулярних кристалів значно нижчі порівняно з іншими. Молекулярні кристали є поганими провідниками електрики. Багато молекулярних речовин при кімнатній температурі є рідинами і газами, деякі мають запах
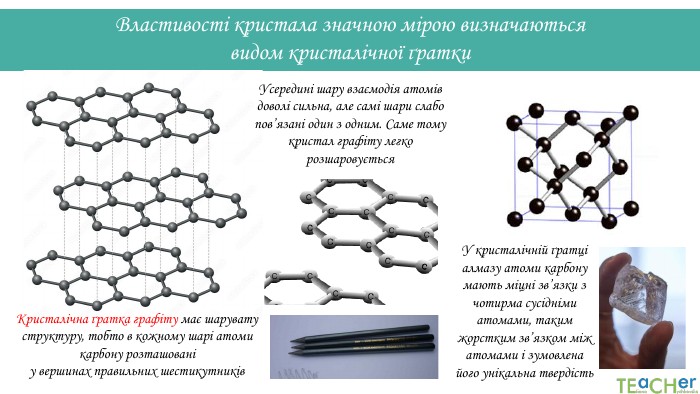
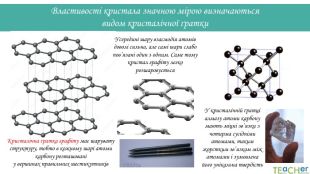
У кристалічній ґратці алмазу атоми карбону мають міцні зв’язки з чотирма сусідніми атомами, таким жорстким зв’язком між атомами і зумовлена його унікальна твердість Властивості кристала значною мірою визначаються видом кристалічної ґратки. Кристалічна ґратка графіту має шарувату структуру, тобто в кожному шарі атоми карбону розташовані у вершинах правильних шестикутників. Усередині шару взаємодія атомів доволі сильна, але самі шари слабо пов’язані один з одним. Саме тому кристал графіту легко розшаровується
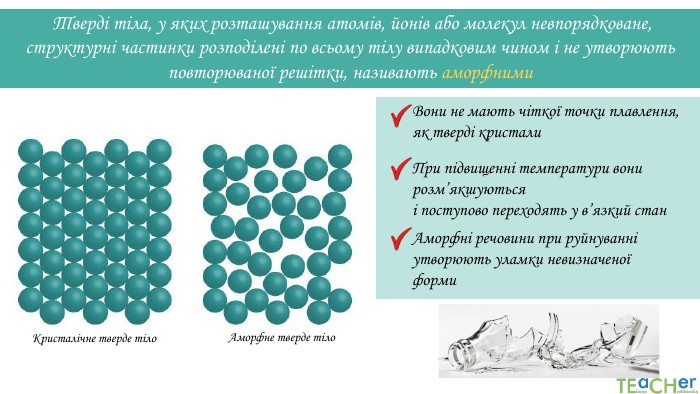
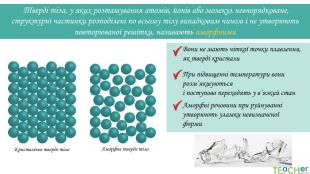
Тверді тіла, у яких розташування атомів, йонів або молекул невпорядковане, структурні частинки розподілені по всьому тілу випадковим чином і не утворюють повторюваної решітки, називають аморфними. Вони не мають чіткої точки плавлення, як тверді кристали. При підвищенні температури вони розм’якшуються і поступово переходять у в’язкий стан Аморфні речовини при руйнуванні утворюють уламки невизначеної форми. Кристалічне тверде тіло. Аморфне тверде тіло
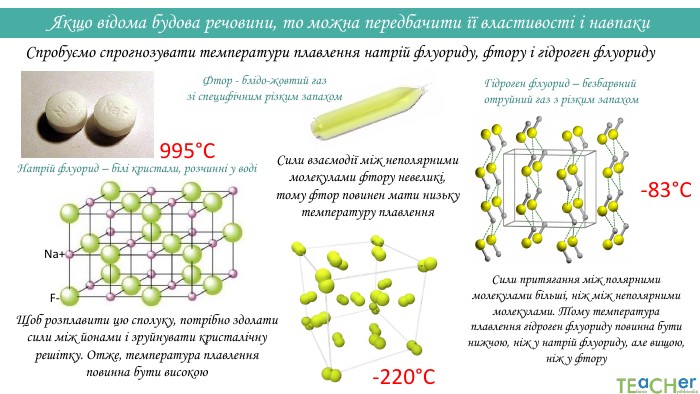
Якщо відома будова речовини, то можна передбачити її властивості і навпаки. Спробуємо спрогнозувати температури плавлення натрій флуориду, фтору і гідроген флуориду. F-Na+Натрій флуорид – білі кристали, розчинні у водіЩоб розплавити цю сполуку, потрібно здолати сили між йонами і зруйнувати кристалічну решітку. Отже, температура плавлення повинна бути високою Фтор - блідо-жовтий газ зі специфічним різким запахом. Сили взаємодії між неполярними молекулами фтору невеликі, тому фтор повинен мати низьку температуру плавлення. Гідроген флуорид – безбарвний отруйний газ з різким запахом Сили притягання між полярними молекулами більші, ніж між неполярними молекулами. Тому температура плавлення гідроген флуориду повинна бути нижчою, ніж у натрій флуориду, але вищою, ніж у фтору 995°C-220°C-83°C
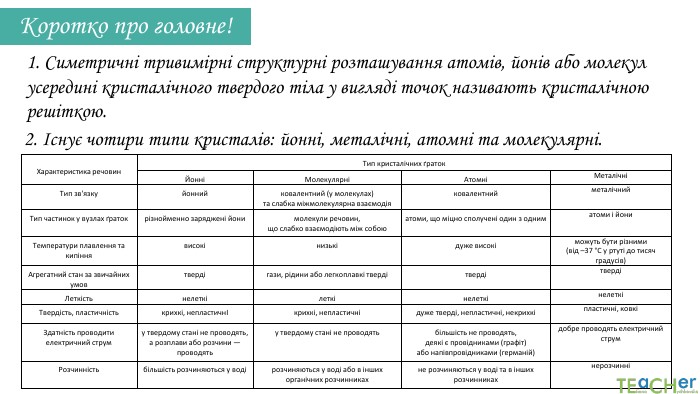
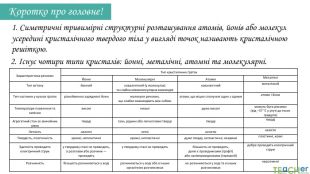
Коротко про головне!1. Симетричні тривимірні структурні розташування атомів, йонів або молекул усередині кристалічного твердого тіла у вигляді точок називають кристалічною решіткою.2. Існує чотири типи кристалів: йонні, металічні, атомні та молекулярні.{5940675 A-B579-460 E-94 D1-54222 C63 F5 DA}Характеристика речовин. Тип кристалічних ґраток. ЙонніМолекулярніАтомніМеталічні Тип зв'язкуйоннийковалентний (у молекулах) та слабка міжмолекулярна взаємодіяковалентнийметалічний. Тип частинок у вузлах ґратокрізнойменно заряджені йонимолекули речовин, що слабко взаємодіють між собоюатоми, що міцно сполучені один з одниматоми і йони. Температури плавлення та кипіннявисокінизькідуже високіможуть бути різними (від –37 °С у ртуті до тисяч градусів)Агрегатний стан за звичайних умовтвердігази, рідини або легкоплавкі твердітвердітвердіЛеткістьнелеткілеткінелеткінелеткіТвердість, пластичністькрихкі, непластичнІкрихкі, непластичнідуже тверді, непластичні, некрихкіпластичні, ковкіЗдатність проводити електричний струму твердому стані не проводять, а розплави або розчини — проводятьу твердому стані не проводятьбільшість не проводять, деякі є провідниками (графіт) або напівпровідниками (германій)добре проводять електричний струм. Розчинністьбільшість розчиняються у водірозчиняються у воді або в інших органічних розчинникахне розчиняються у воді та в інших розчинникахнерозчинні


про публікацію авторської розробки
Додати розробку








-

Прищенко Тетяна Іванівна
15.01.2025 в 15:34
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Потапова Галина Іванівна
18.11.2024 в 23:23
дякую!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Шатовський Валентин Олександрович
17.11.2024 в 10:28
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Виноградова Оксана Михайлівна
12.12.2023 в 09:34
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Переверзева Інна Євгенівна
21.11.2023 в 23:41
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Пашаєва Тетяна Миколаївна
13.11.2023 в 17:45
Дуже дякую!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Пашаєва Тетяна Миколаївна
13.11.2023 в 17:45
Дуже дякую!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 4 відгука