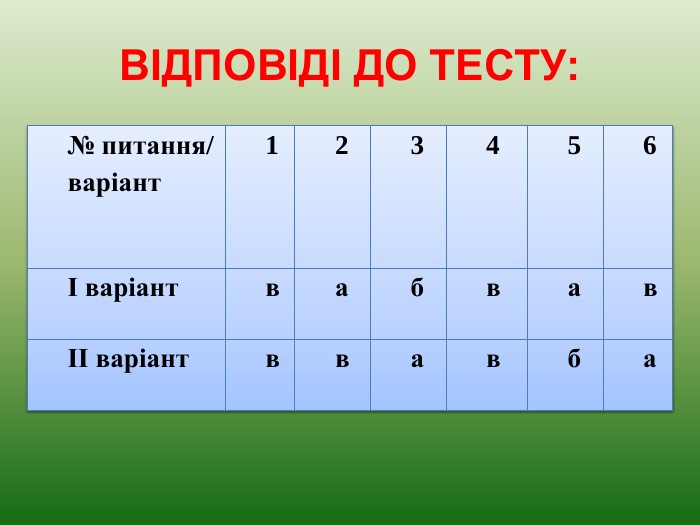
Презентація "Ферум. Залізо. Фізичні та хімічні властивості, взаємодія з киснем, сіркою. Поширеність Феруму в природі"
Про матеріал
Презентація до уроку "Ферум. Залізо. Фізичні та хімічні властивості, взаємодія з киснем, сіркою. Поширеність Феруму в природі" Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку