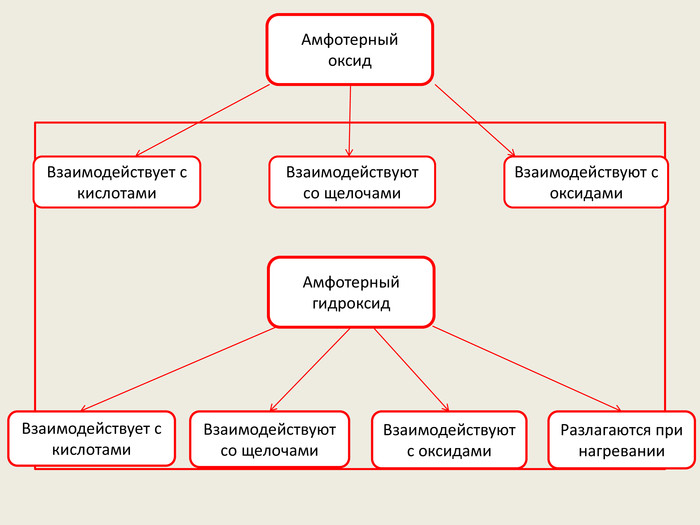
Презентація "Хімічні властивості амфотерних оксидів та гідроксидів "
Про матеріал
Презентація до уроку в 8-х класах на тему "Хімічні властивості амфотерних оксидів. Хімічні властивості амфотерних гідроксидів: взаємодія з кислотами, лугами (в розчині, при сплавлянні)." Перегляд файлу
Зміст слайдів
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку



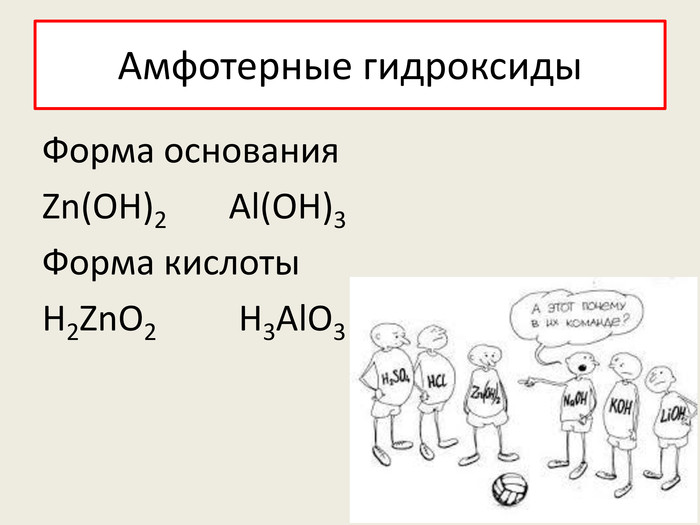

![При взаимодействии с растворимыми основаниями амфотерные гидроксиды проявляют кислотные свойства: В растворах взаимодействуют только со щелочами: Кислота + основание → соль + вода. Zn(OH)2 + 2 Na. OH = Na2 [Zn(ОН)4] натрий тетрагидроксоцинкат. Al(OH)3 + Na. OH = Na [Al(ОН)4] натрий тетрагидроксоалюминат. Al(OH)3 + 3 Na. OH = Na3 [Al(ОН)6] натрий гексагидроксоалюминат При взаимодействии с растворимыми основаниями амфотерные гидроксиды проявляют кислотные свойства: В растворах взаимодействуют только со щелочами: Кислота + основание → соль + вода. Zn(OH)2 + 2 Na. OH = Na2 [Zn(ОН)4] натрий тетрагидроксоцинкат. Al(OH)3 + Na. OH = Na [Al(ОН)4] натрий тетрагидроксоалюминат. Al(OH)3 + 3 Na. OH = Na3 [Al(ОН)6] натрий гексагидроксоалюминат](/uploads/files/743365/174329/186960_images/5.jpg)