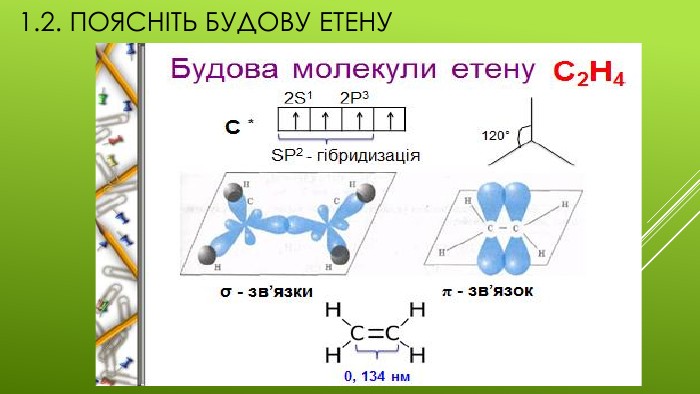
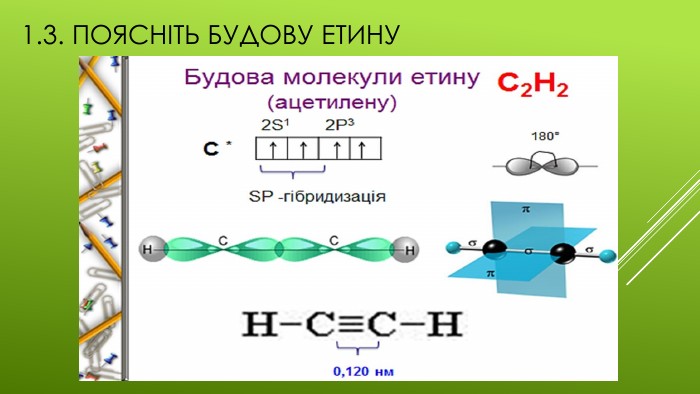
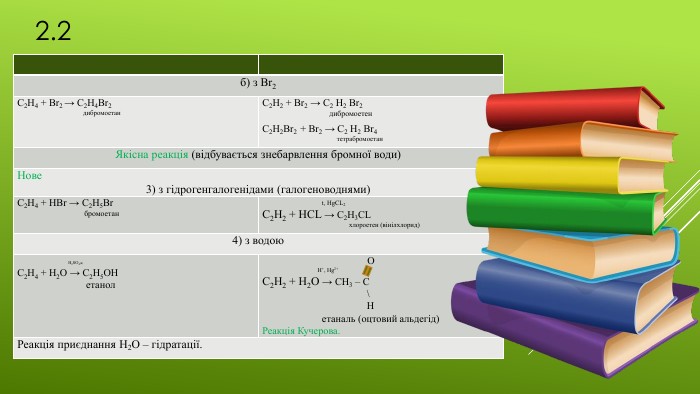
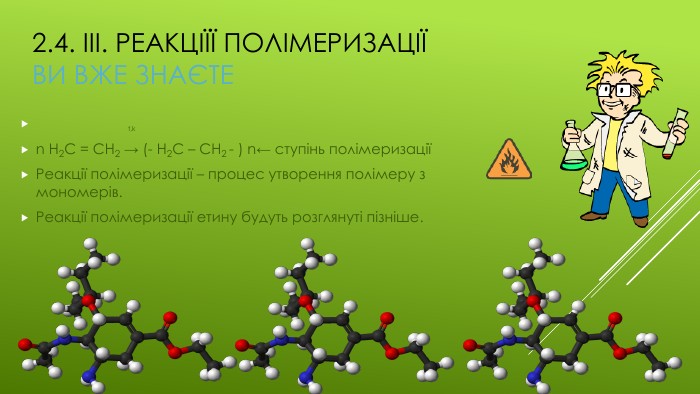
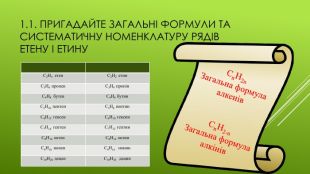
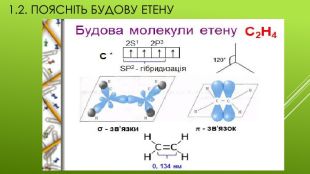
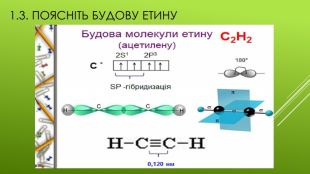
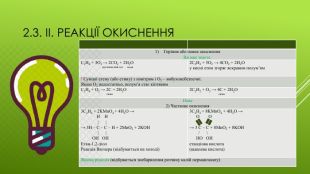
Презентація "Хімічні властивості етену та етину."
Про матеріал
Презентація на тему "Хімічні властивості етену та етину",яка є доповненням до конспекту уроку "Хімічні властивості етену та етину". Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку