Презентація "Хімічні властивості солей"
Про матеріал
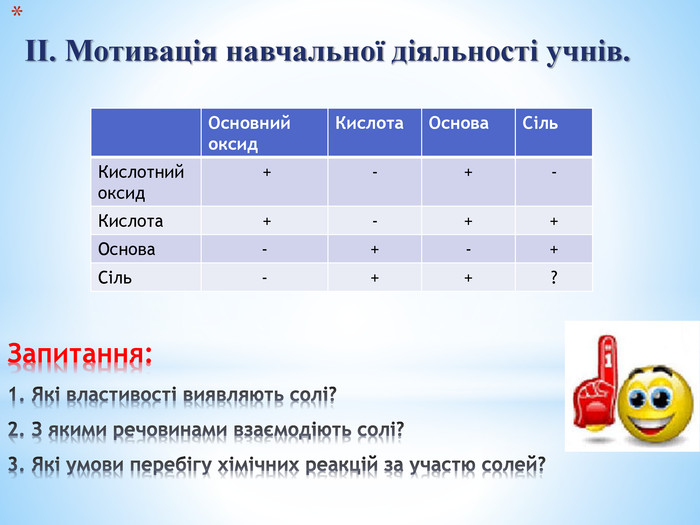
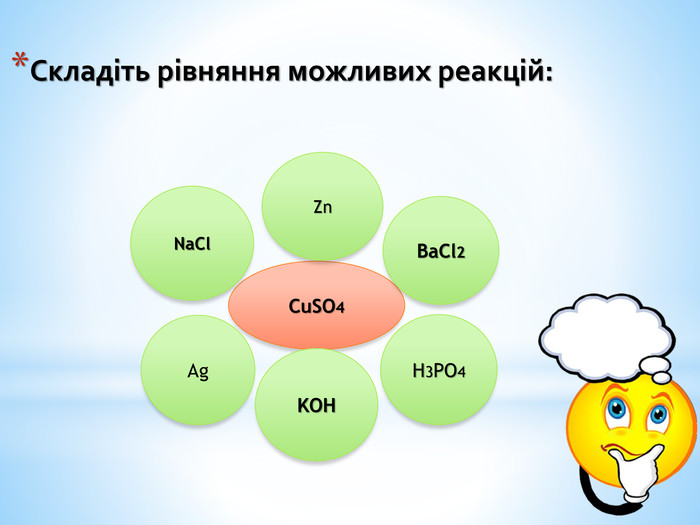
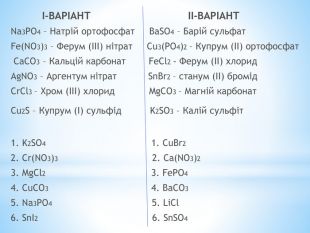
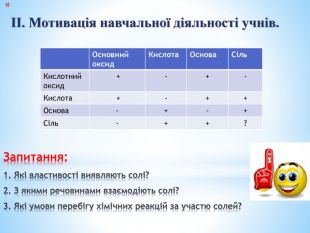
Презентація до уроку "Хімічні властивості середніх солей" для класу з вивченням хімії на рівні стандарту. Дана презентація містить перевірочну роботу, вивчення нового матеріалу та виконання лабораторних дослідів з вивчення хімічних кластивостей середніх солей: взаємодія з металами, кислотами, лугами, іншими солями. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку






















-

Сергєєнкова ірина Станіславівна
25.04.2023 в 20:51
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Костіна Неля Миколаївна
16.04.2023 в 13:10
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Тимчишин Іванна
03.05.2022 в 18:56
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Гуменюк Олена
15.03.2022 в 22:27
Дякую,гарна робота.
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 1 відгук