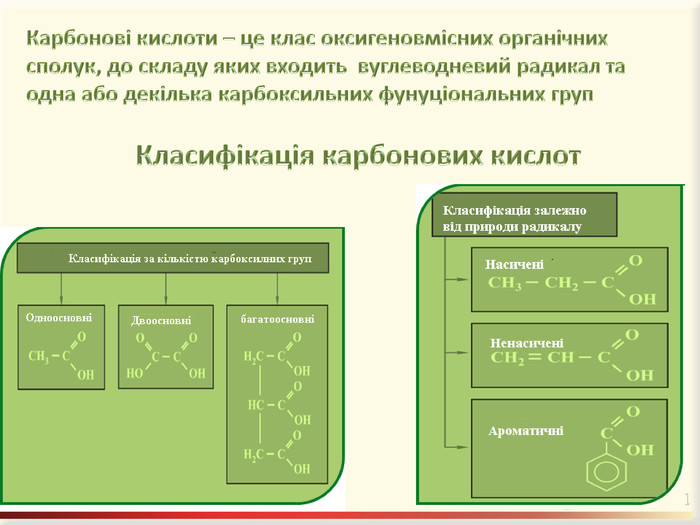
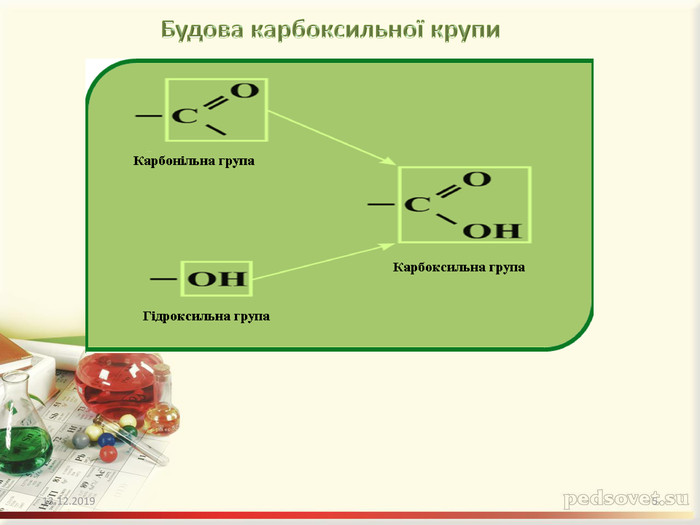
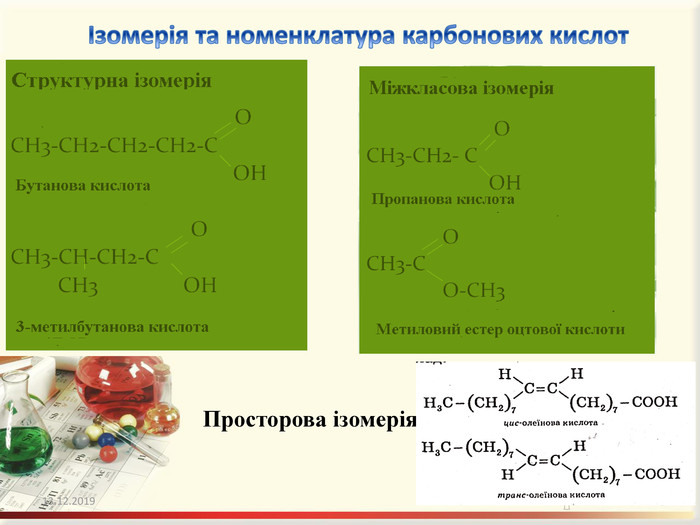
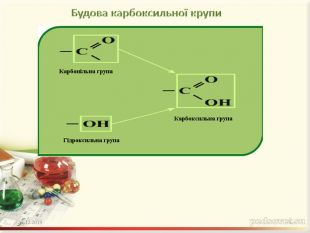
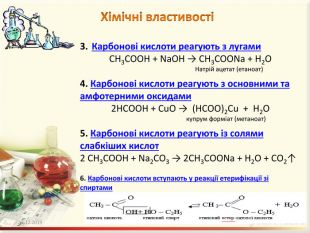
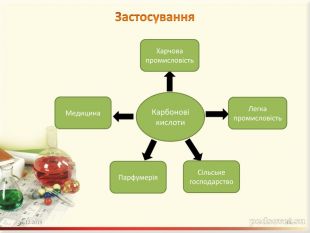
Презентація "Карбонові кислоти. Склад, будова, ізомерія, поширення, застосування, фізичні та хімічні властивості"
Про матеріал
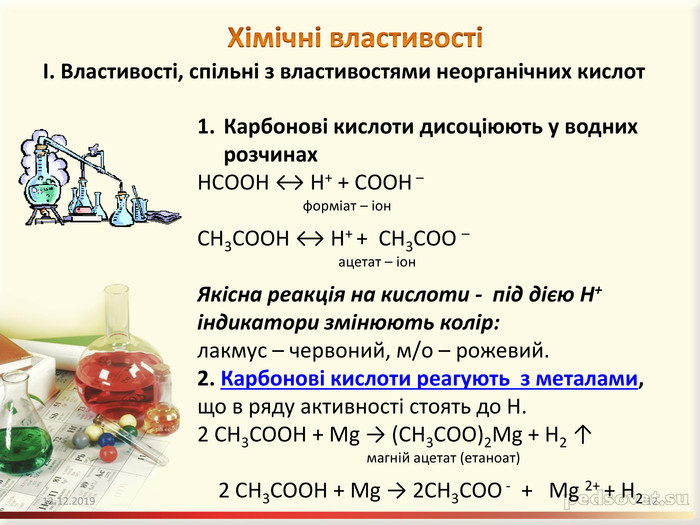
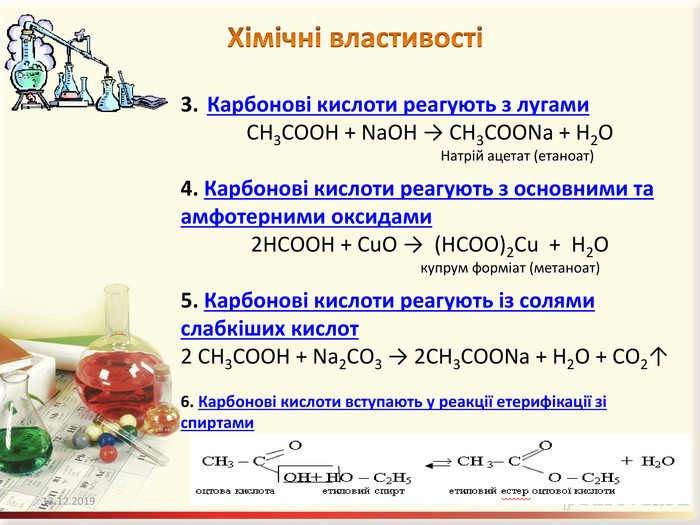
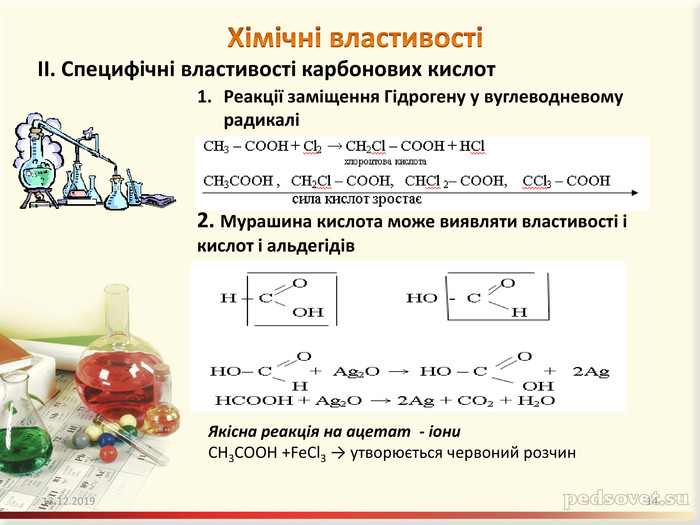
Містить відео десомонстрації хімічних властивостей карбонових кислот на прикладі оцтової кислоти Зміст архіву
Перегляд файлу
Зміст слайдів

Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку