Презентація: кисень та вода, типи реакцій, індикатори
 |

 Класифікація хімічних реакцій
Класифікація хімічних реакцій
 1.Реакція сполучення 2.Реакція розкладу 3.Реакція заміщення
1.Реакція сполучення 2.Реакція розкладу 3.Реакція заміщення
4.Реакція обміну
 1.Реакція сполучення
1.Реакція сполучення

 Реакція сполучення — реакція, під час якої з двох або кількох речовин утворюється одна нова речовина
Реакція сполучення — реакція, під час якої з двох або кількох речовин утворюється одна нова речовина
 A + B = С
A + B = С
Приклад: С+О 2= СО2
2.  Реакція розкладу
Реакція розкладу

 Реакція розкладу — реакція, під час якої з однієї речовини утворюється дві або кілька нових
Реакція розкладу — реакція, під час якої з однієї речовини утворюється дві або кілька нових
 С = А + В
С = А + В
Приклад: 2KCIO3 = 2KCI + O2
3.  Реакція заміщення
Реакція заміщення
Реакція заміщення — реакція між простою та складною речовиною, у процесі якої атоми простої речовини заміщують атоми одного з елементів у складній

 речовині, внаслідок чого утворюються нова проста і нова складна речовини
речовині, внаслідок чого утворюються нова проста і нова складна речовини
 АВ + С = СВ + А
АВ + С = СВ + А
Приклад: Fe +CuSO = FeSO + Cu4 4
4.  Реакція обміну
Реакція обміну

 Реакція обміну — реакція, у процесі якої дві складні речовини обмінюються своїми складовими частинами
Реакція обміну — реакція, у процесі якої дві складні речовини обмінюються своїми складовими частинами
 АВ + СD = AD + CB
АВ + СD = AD + CB
Приклад: KI + AgNO = AgI + KNO3 3
 Кисень
Кисень
Фізичні властивості

![]() безбарвний газ
безбарвний газ ![]() не має запаху та смаку
не має запаху та смаку ![]() при охолодженні до -183 °С перетворюється на блакитну рідину
при охолодженні до -183 °С перетворюється на блакитну рідину ![]() за температури -219 °С рідина твердне, утворюючи сині кристали.
за температури -219 °С рідина твердне, утворюючи сині кристали. ![]() кисень в 1,1 раза важчий за повітря
кисень в 1,1 раза важчий за повітря ![]() малорозчинний у воді (істоти у водоймах дихають розчиненим киснем)
малорозчинний у воді (істоти у водоймах дихають розчиненим киснем)
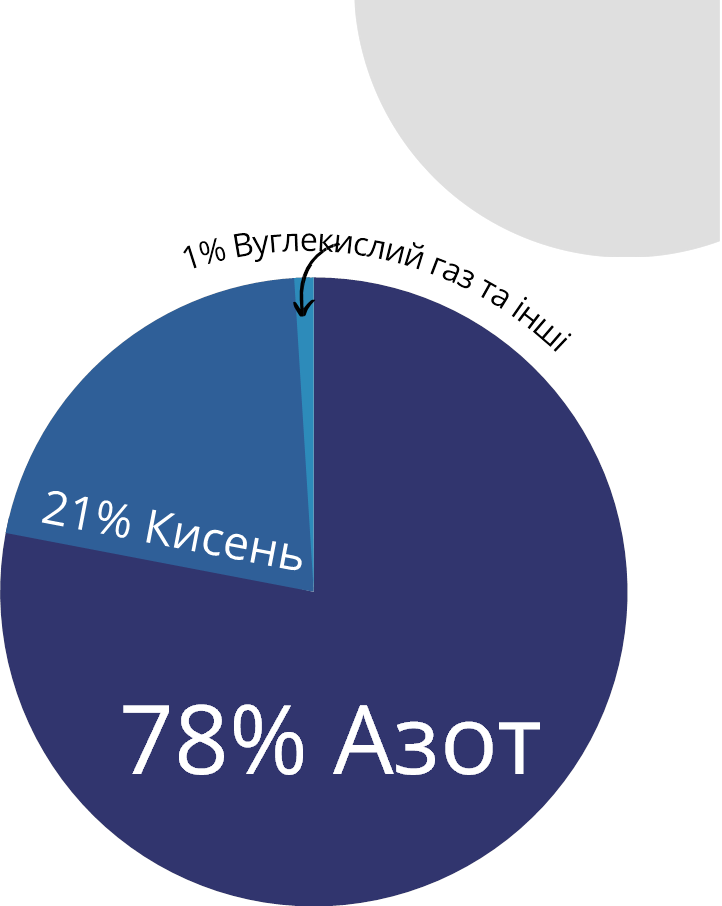
Повітря

Кисень
Хімічні властивості
Оксиди — сполуки утворені двома елементами, один з яких Оксиген.
Реакції кисню з простими речовинами


 Кисень взаємодіє (як правило при нагріванні) з більшістю неметалів та майже з усіма металами
Кисень взаємодіє (як правило при нагріванні) з більшістю неметалів та майже з усіма металами
Вугілля нагріте на повітрі до великої температури загораєтья
Реакція з сіркою
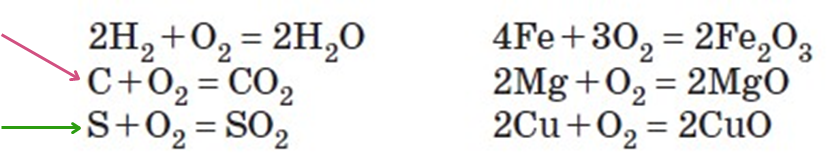 Коли запалюємо сірник
Коли запалюємо сірник
Реакції кисню зі складними речовинами
Реакції зі складними речовинами відбуваються наприклад, коли горить природний газ, етиловий спирт, ацетон тощо.
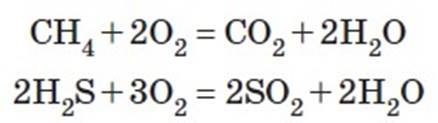



 Взаємодія води з оксидами
Взаємодія води з оксидами
Усі кислотні оксиди (за винятком силіцій(IV) оксиду SiO2) вступають у реакції сполучення з водою з утворенням кислот:
CO2 + H2O = H2CO3 (карбонатна кислота) Кислота
 |

 |
P2O5 + 3H2O = 2H3PO4 (ортофосфатна кислота)
 Більшість основних оксидів із водою НЕ взаємодіють.
Більшість основних оксидів із водою НЕ взаємодіють.
 Основні оксиди взаємодіють із водою лише в тому разі, якщо продуктом реакції є розчинна основа (луг), зокрема:
Основні оксиди взаємодіють із водою лише в тому разі, якщо продуктом реакції є розчинна основа (луг), зокрема:
Na2O + H2O = 2NaOH
CaO + H2O = Ca(OH)2




Дякую

 |
за увагу


про публікацію авторської розробки
Додати розробку
