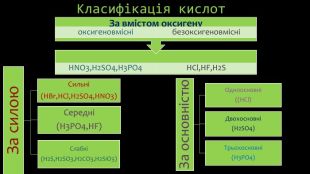
Презентація "Кислоти: фізичні властивості, поширеність"
Про матеріал
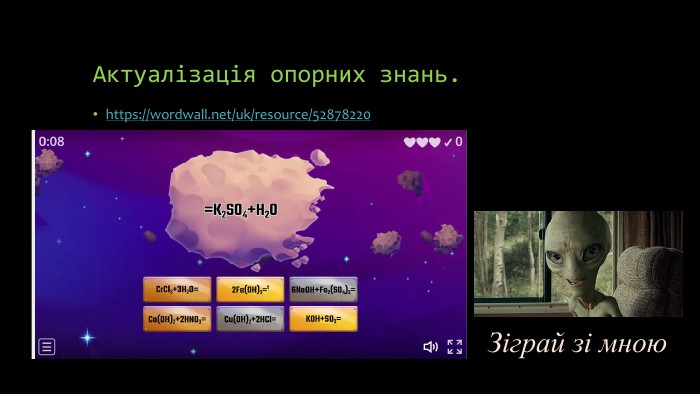
познайомити учнів з поширеністю кислот у природі, їх використанням; розвивати вміння логічно і творчо мислити та критично оцінювати отриману інформацію.
Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку