Презентація "Кислоти, їхні склад і назви"
Про матеріал
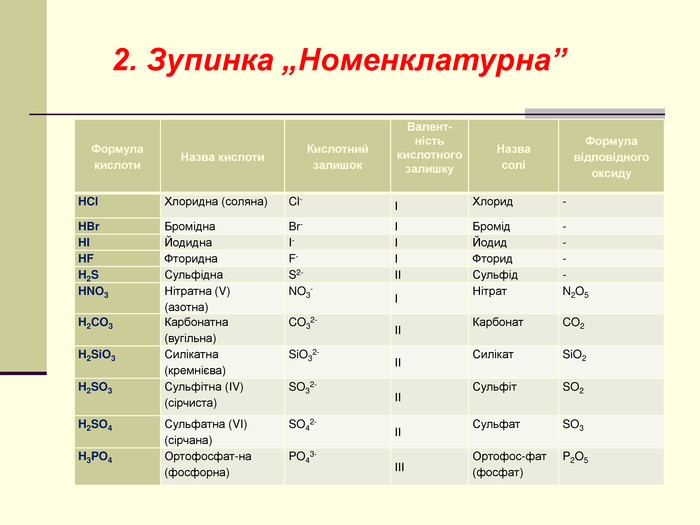
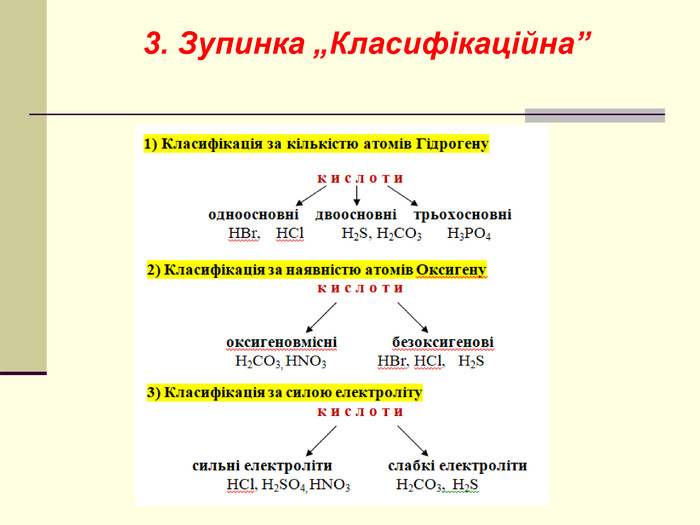
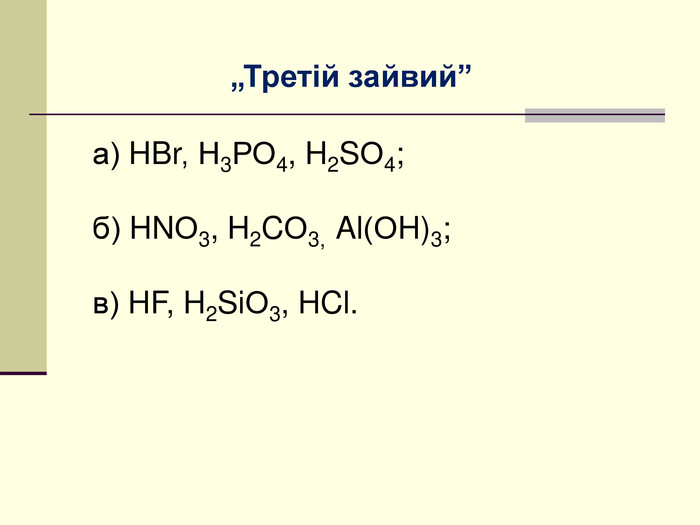
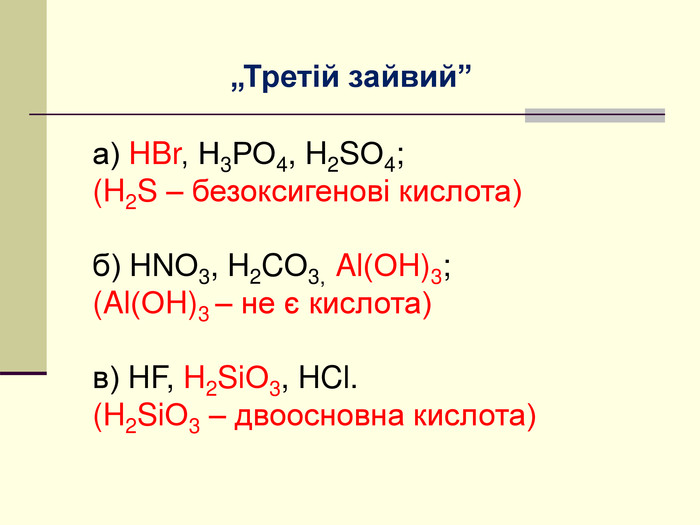
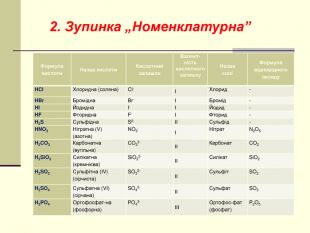
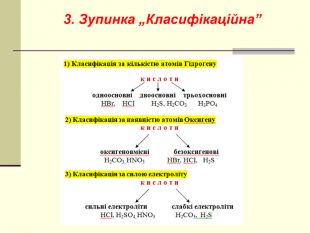
Мета: освітня – сприяти розширенню знань про класифікацію неорганічних речовин на прикладі кислот, ознайомити учнів із поняттям „кислота”, класифікацією кислот за складом та номенклатурою кислот;
розвиваюча – розвивати логічне мислення, пам’ять, вміння визначати та класифікувати кислоти, давати назви кислотам; розвивати інтелектуальну культуру учня;
виховна – виховувати науковий світогляд, вміння брати відповідальність за прийняте рішення.
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
Дякую! Оригінально та змістовно!


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку