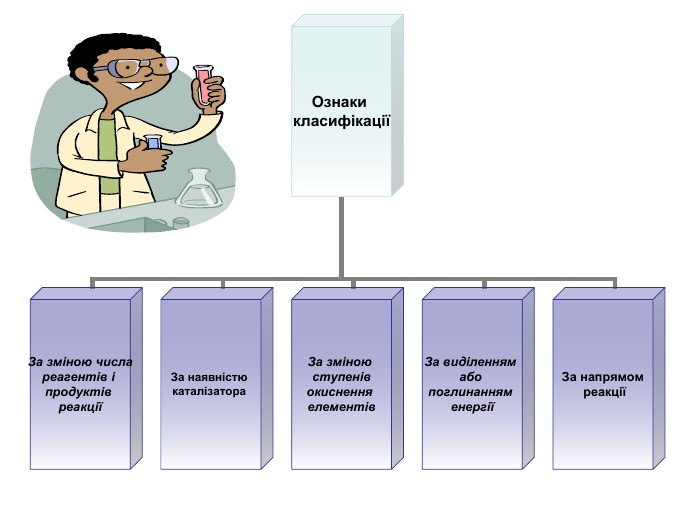
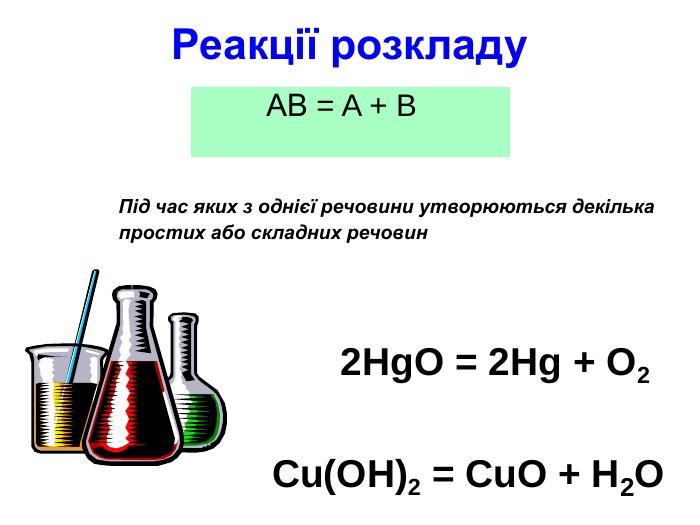
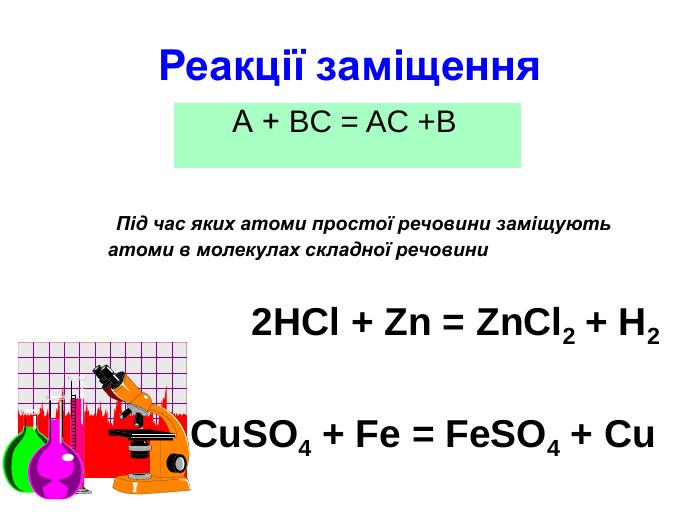
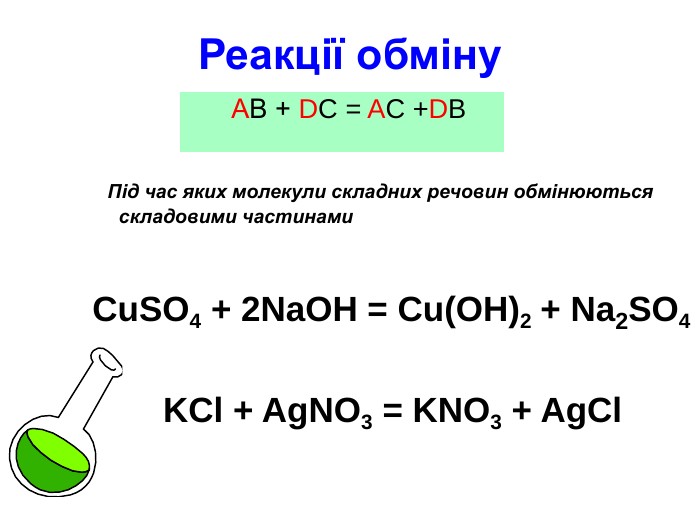
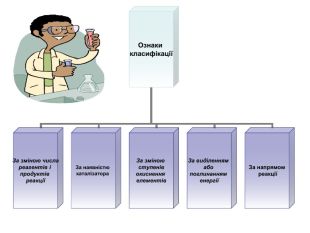
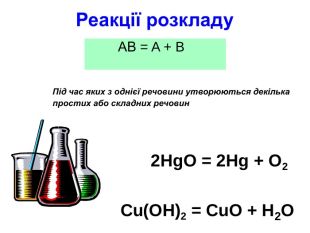
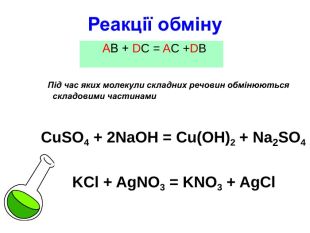
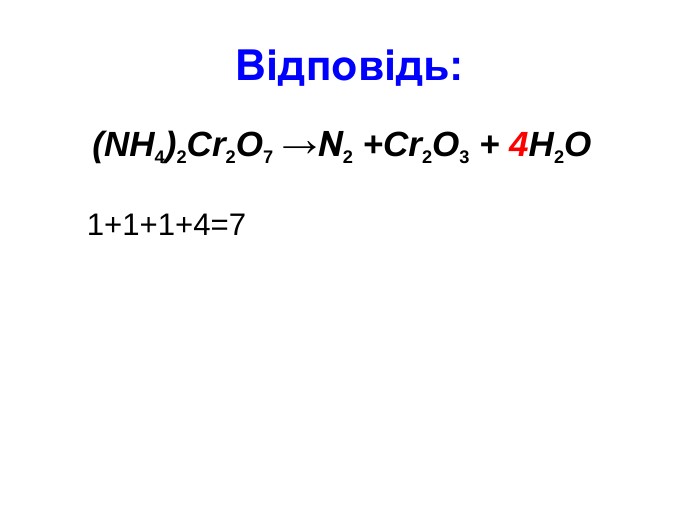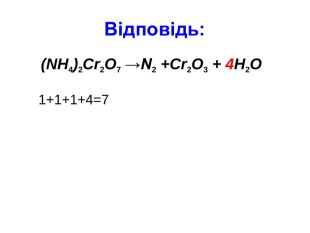Презентація " Класифікація хімічних реакцій"
Про матеріал
Презентація " Класифікація хімічних реакцій" для проведення уроку узагальнення і систематизації знань з хімії в 9 класі Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
-
дякую
-


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку