Презентація "Методика розв'язування задач"
Про матеріал
В даній презентації зібрані алгоритми:
-складання формулбінарних сполук за валентністю;
-визначення валентності за формуламибінарних сполук;
-складання хімічного рівняння з непарноюкількістю атомів;
-складання йонних рівнянь;
-складання назви насиченого вуглеводню;
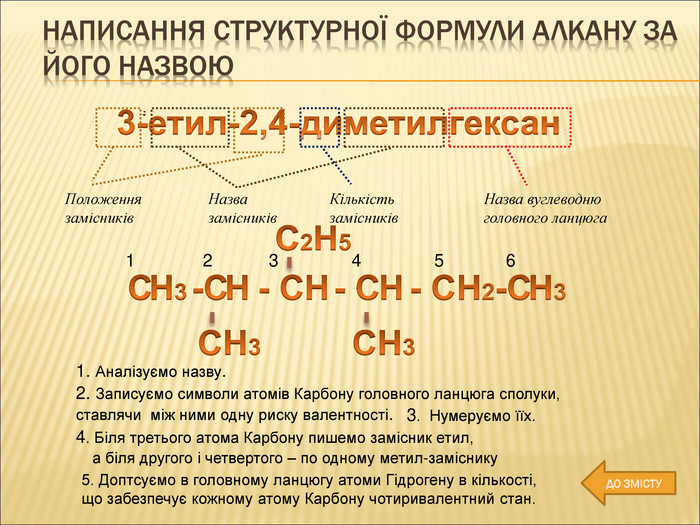
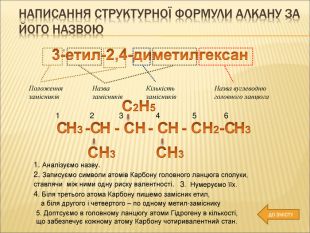
-написання структурної формули алкану за його назвою
Перегляд файлу
Зміст слайдів
ppt
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку