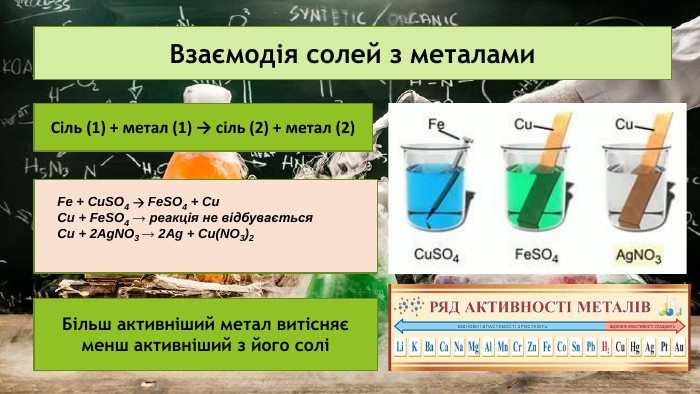
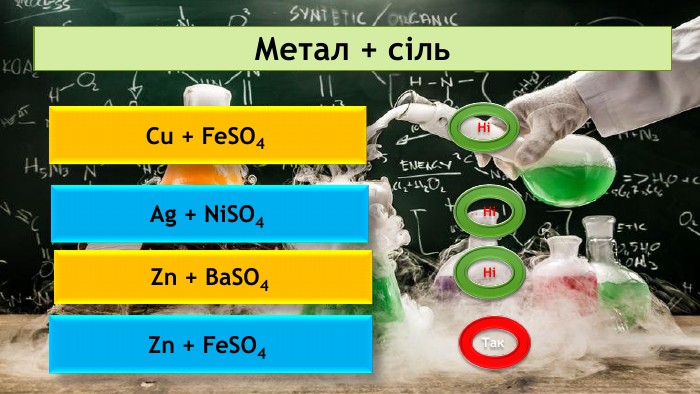
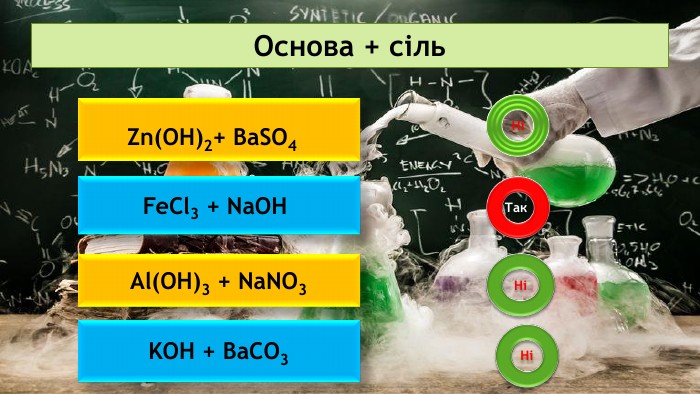
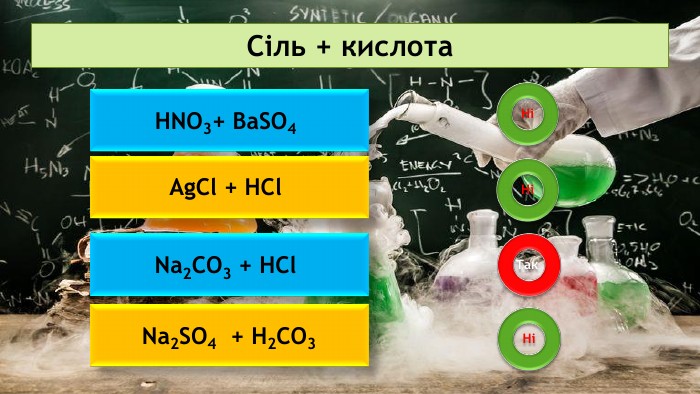
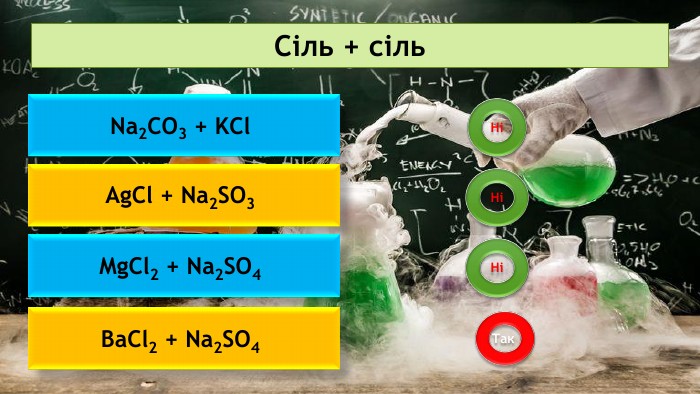
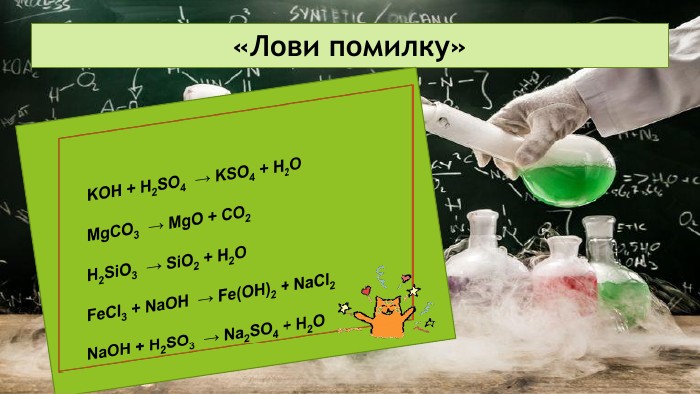
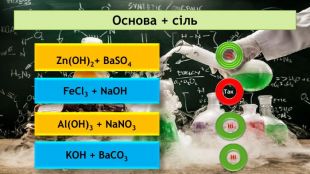
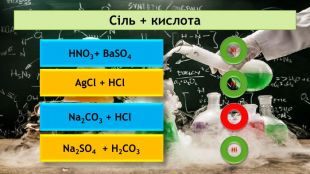
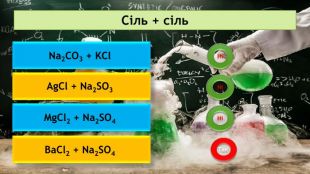
Презентація на тему: "Хімічні властивості середніх солей"
Про матеріал
Презентація на тему; Хімічні властивості середніх солей" може бути використана на уроках хімії у 8 класі при вивченні теми "Основні класи неорганічних сполук" також в 11 класі Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
Дякую!
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку