Презентація на тему Металічні і неметалічні елементи. Метали і неметали. Навчальне дослідження№3
Про матеріал
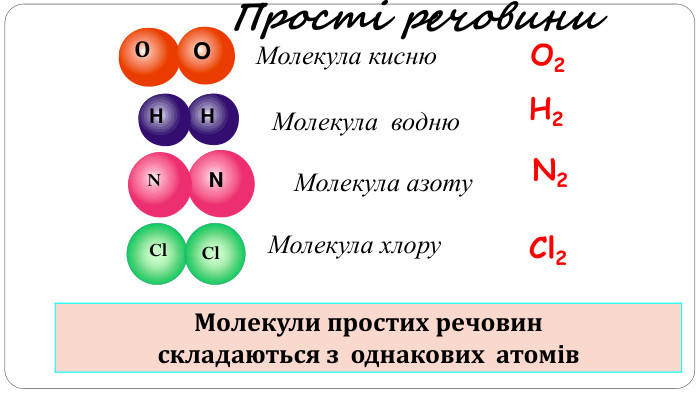
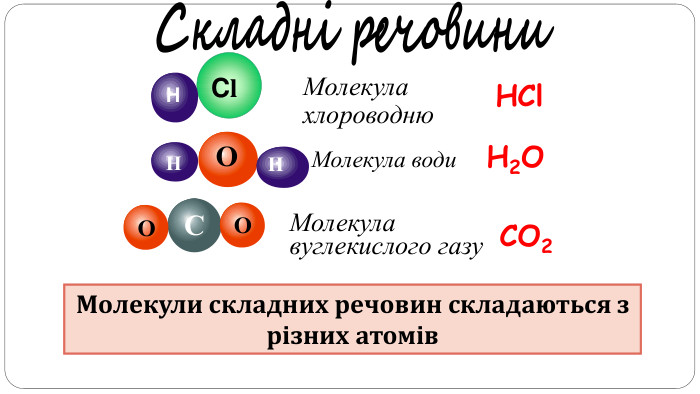
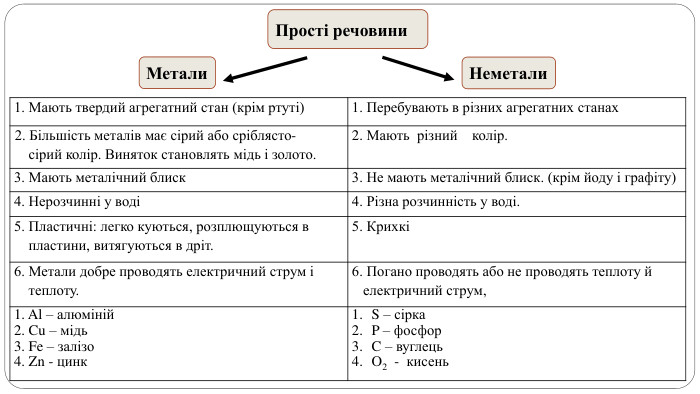
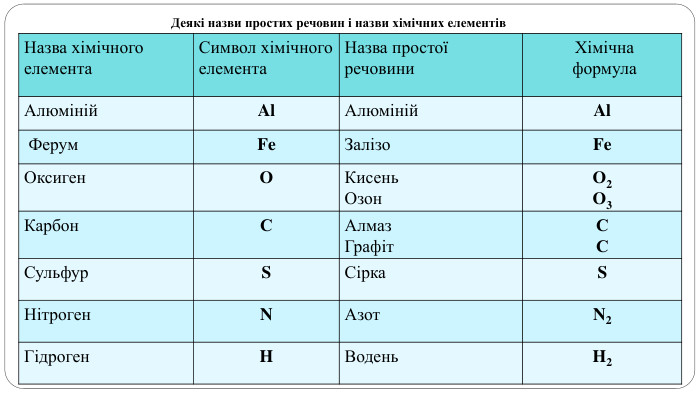
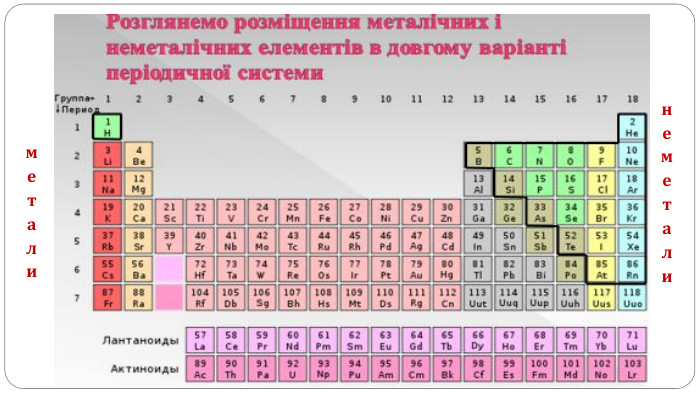
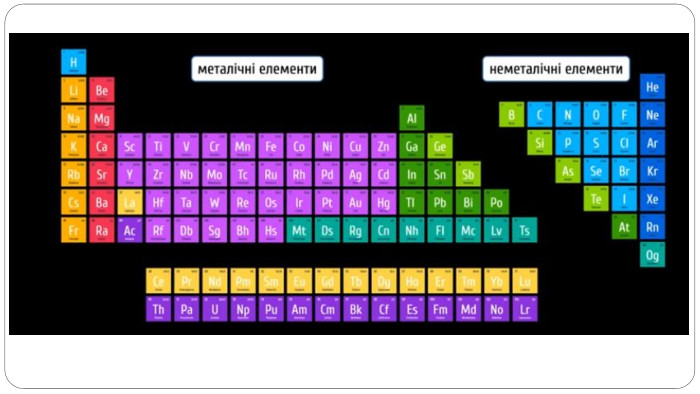
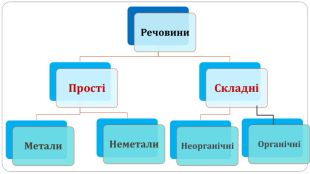
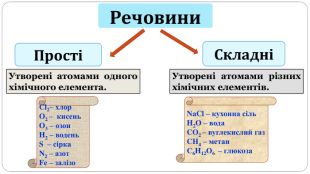
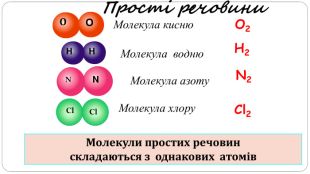
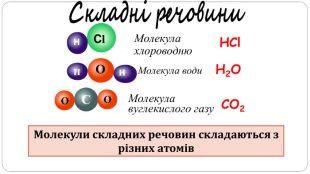
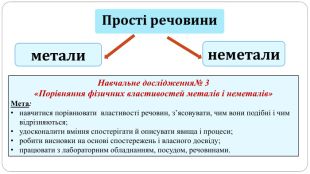
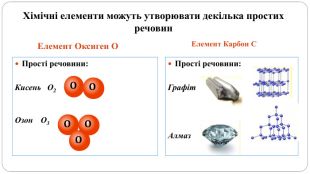
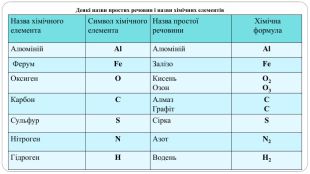
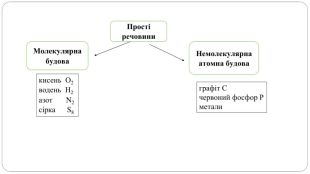
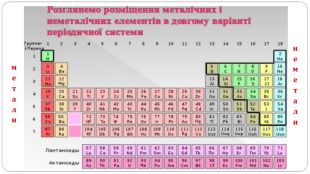
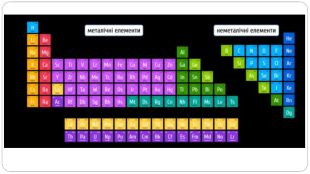
увести поняття про багатоатомність речовин, дати елементарну класифікацію елементів на металічні та неметалічні, навчити розрізняти металічні та неметалічні елементи за їх положенням у періодичній системі, показати суттєву відмінність фізичних властивостей металів і неметалів, розвивати вміння порівнювати метали і неметали за їх властивостями, робити логічні висновки, формувати інтерес до навчання, показувати важливість набутих знань.
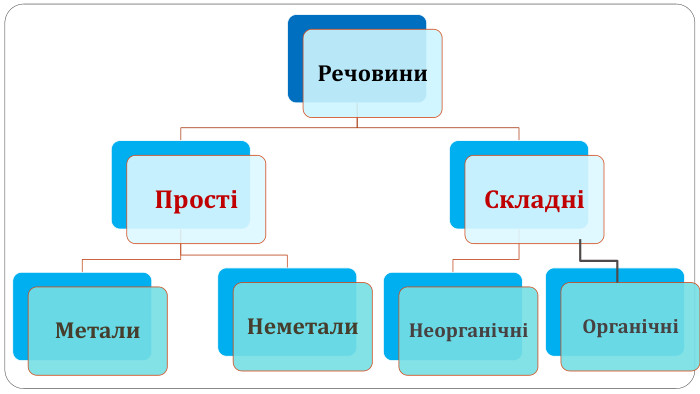
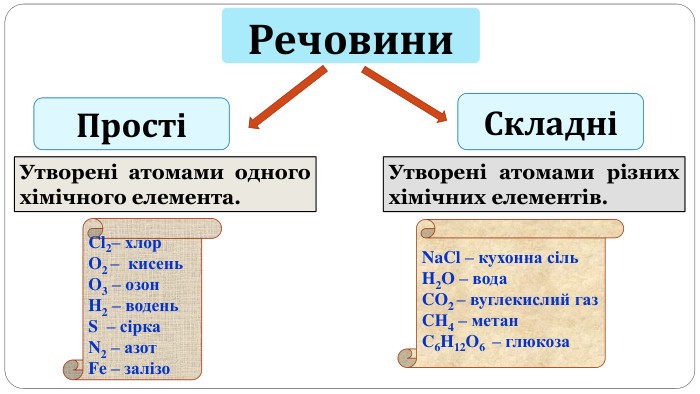
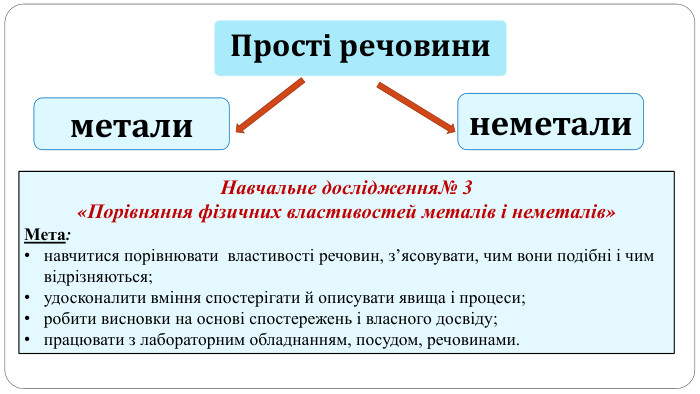
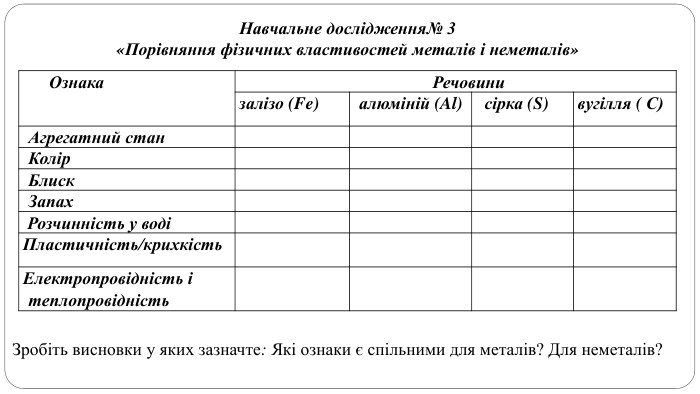
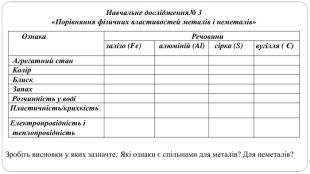
Поняття про метали й неметали учні /учениці використовують із початкової школи, але головна мета цього дослідження — самостійно дійти висновку, що ці групи речовин об’єднують спільні фізичні властивості.
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
-
Дякую!


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку