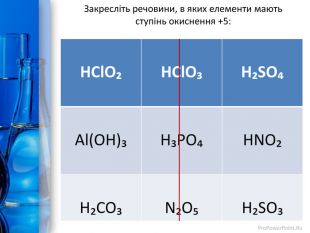
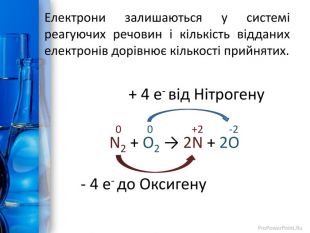
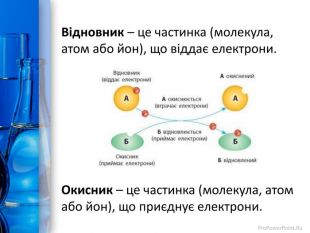
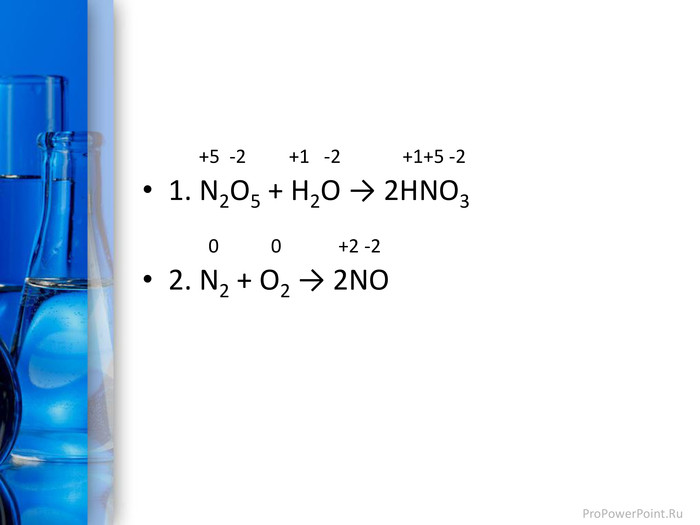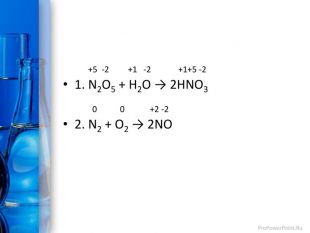Презентація "Окисно-відновні реакції"
Про матеріал
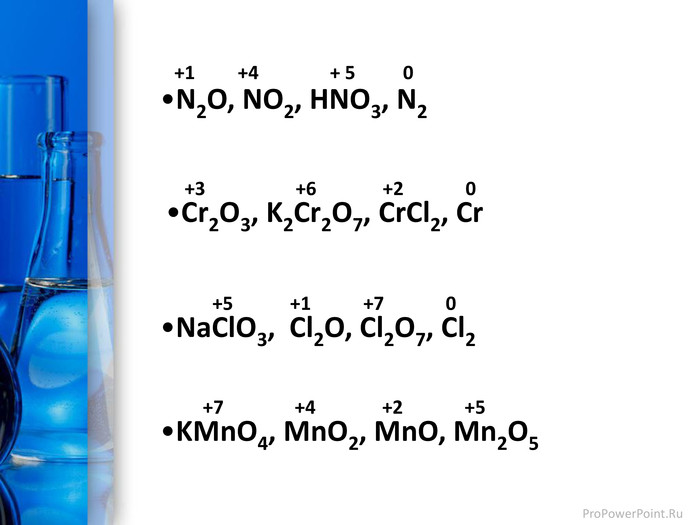
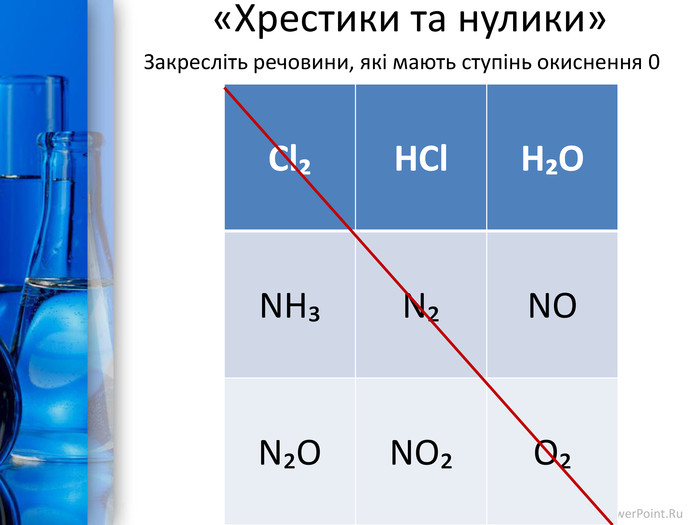
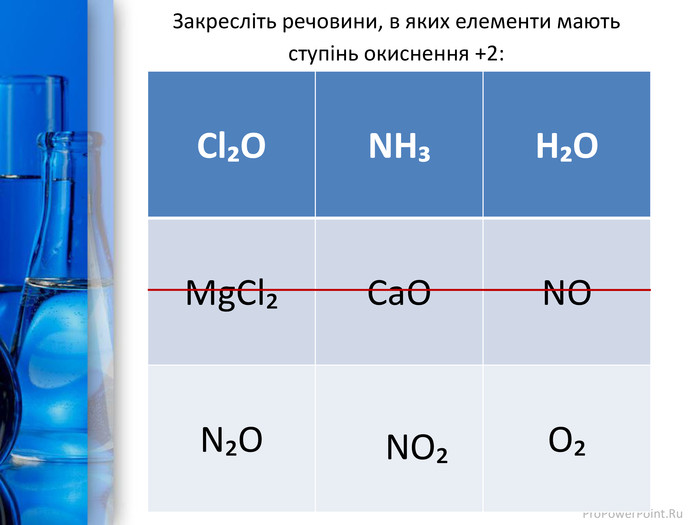
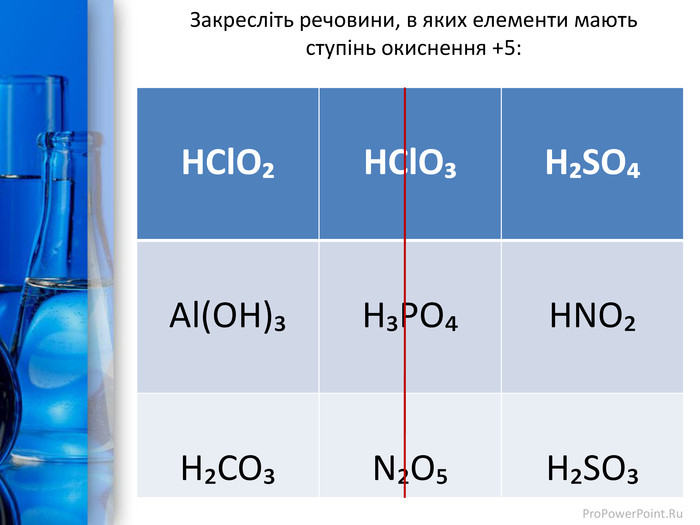
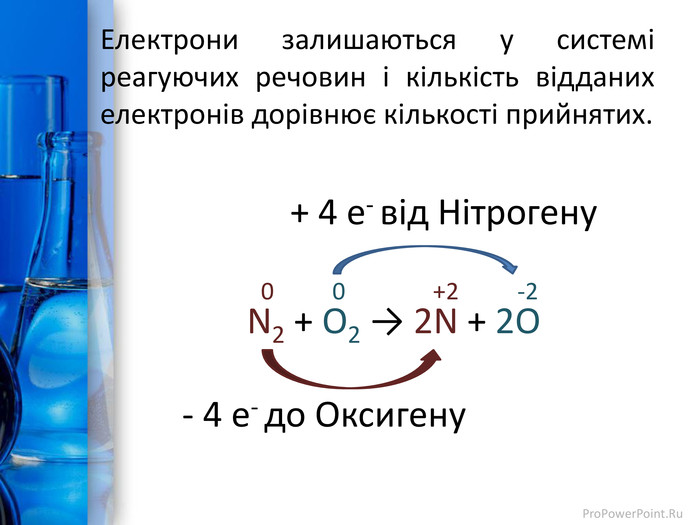
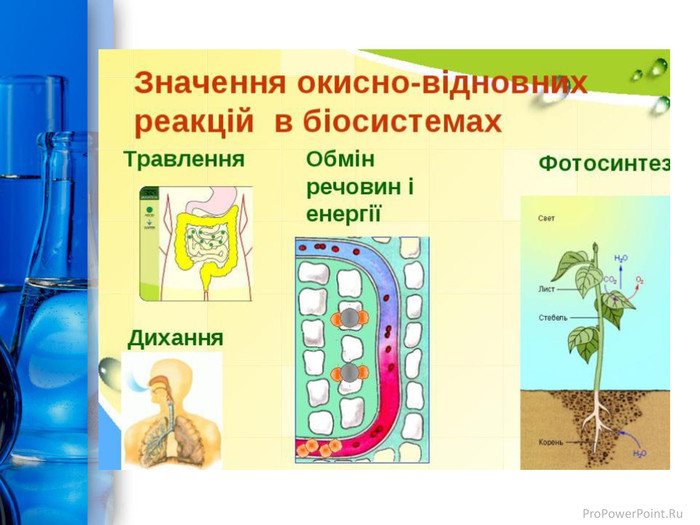
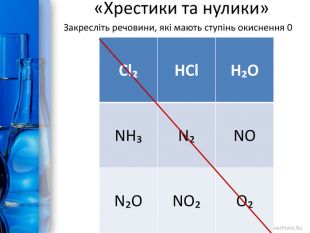
Презентація до уроку з теми "Окисно-відновні реакції. Процеси окиснення, відновлення; окисники, відновники". Перегляд файлу
Зміст слайдів
ppt
До підручника
Хімія 9 клас (Григорович О.В.)
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку