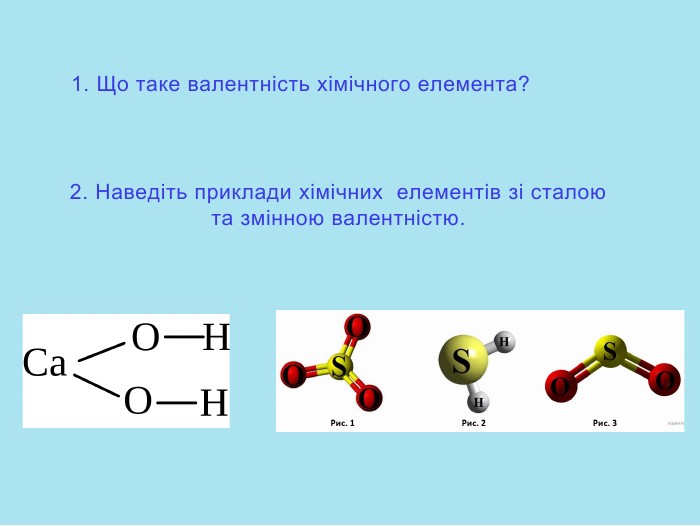
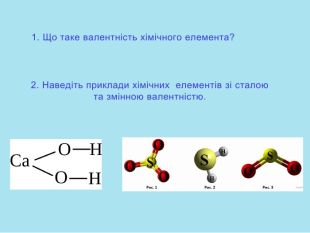
Презентація "Природа хімічного зв'язку".
Про матеріал
Презентація складається з розділів:
- Електронна природа хімічного зв'язку
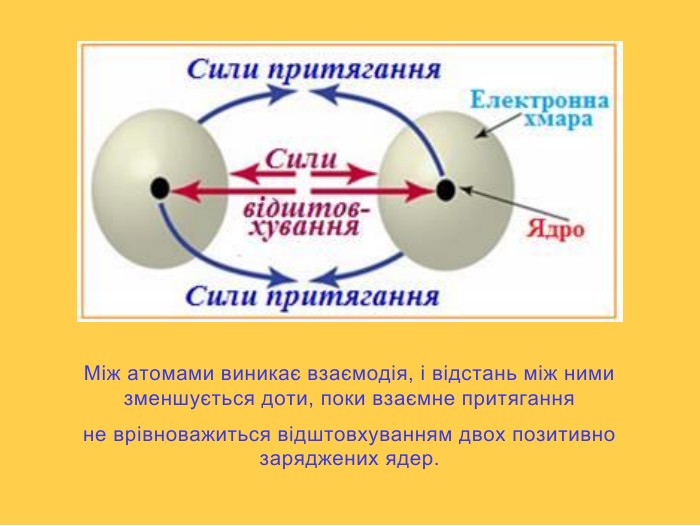
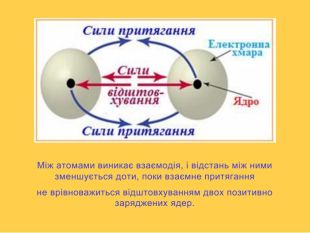
- Умови виникнення хімічного зв'язку
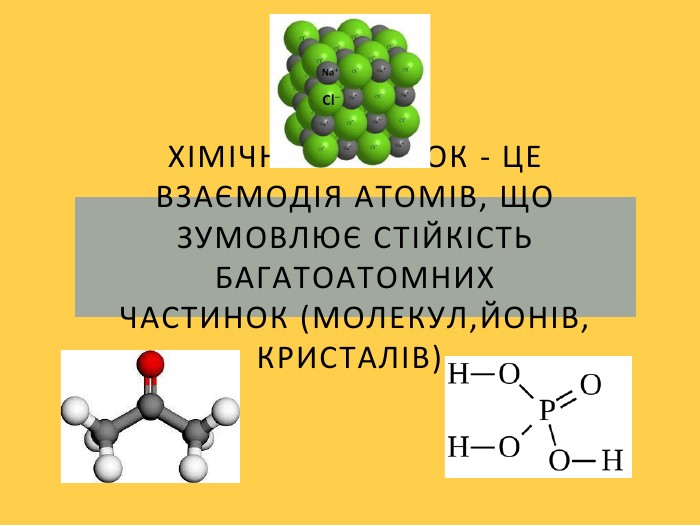
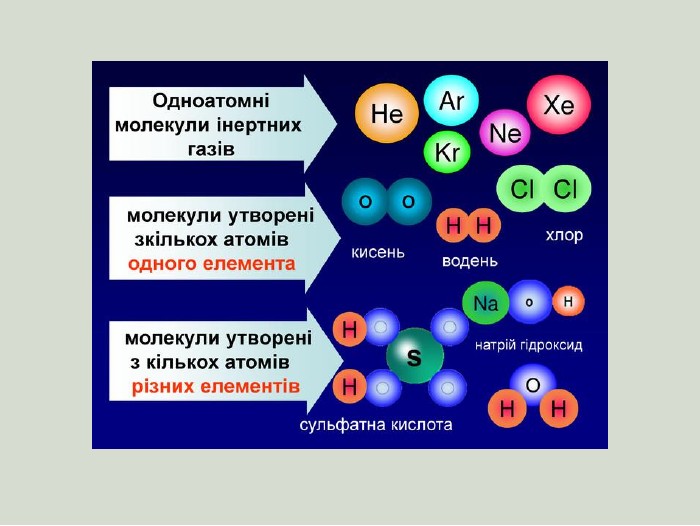
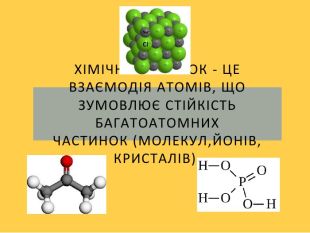
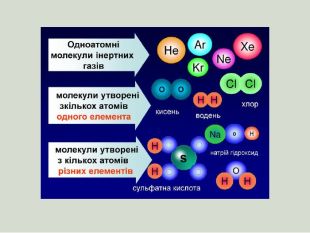
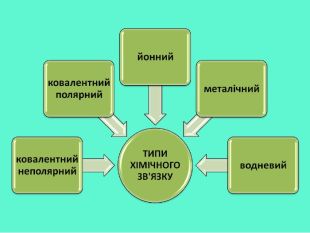
- Типи хімічного зв'язку.
Також презентація містить завдання з актуалізації знань та закріплення нового матеріалу. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку