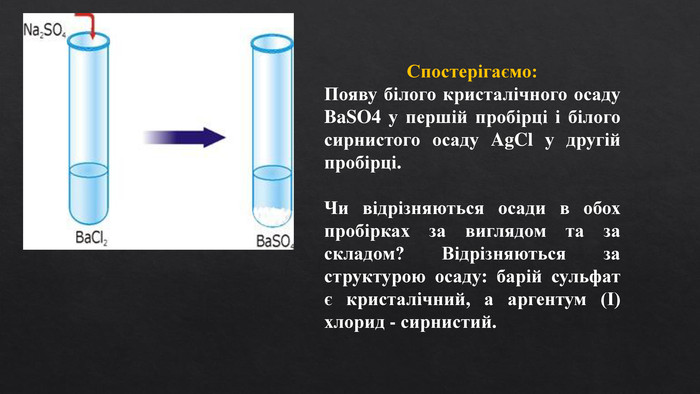
Презентація "Реакції обміну між електролітами у водних розчинах"
Про матеріал
Презентація містить інформацію про хід роботи, завдання до практичної роботи "Реакції обміну між електролітами у водних розчинах", є допоміжним матеріалом під час дистанційного навчання. Перегляд файлу
Зміст слайдів
pptx
До підручника
Хімія 9 клас (Григорович О.В.)
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку