Презентація "Реакції йонного обміну"
Про матеріал
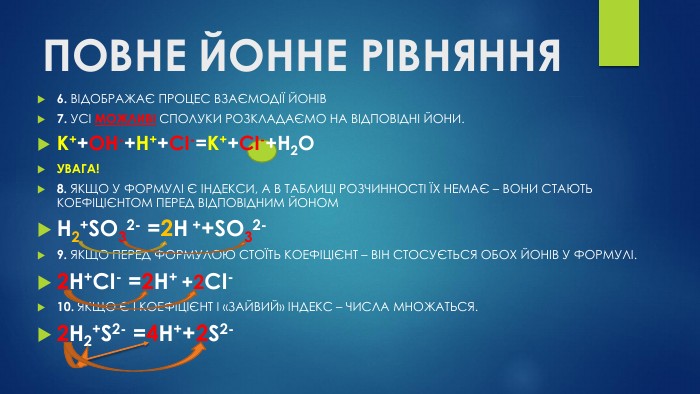
Матеріал презентації допоможе під час пояснення теми "Реакції йонного обміну" у 9 класі. Також стане в нагоді під час повторення теми в 11 класі. Перегляд файлу
Зміст слайдів
pptx
До підручника
Хімія 9 клас (Григорович О.В.)
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку