Презентація "Розрахункові задачі. Розрахунки за хімічними рівняннями маси, об’єму, кількості речовини реагентів та продуктів"
Про матеріал
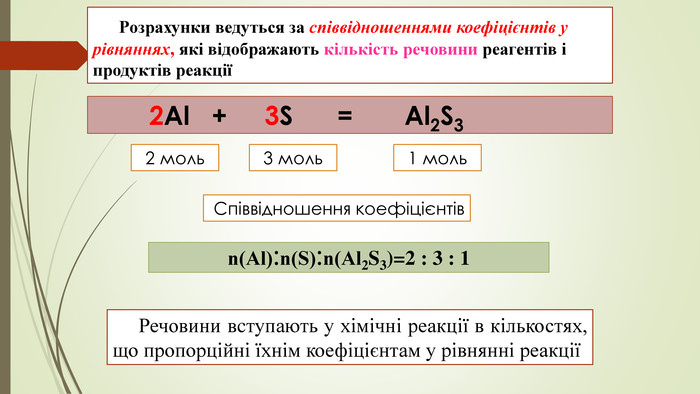
Презентація до уроку хімії 8 клас з теми "Розрахунки за хімічними рівняннями маси, об’єму, кількості речовини реагентів та продуктів". У матеріалі наводиться алгоритм розв'язування задач двома способами. Перегляд файлу
Зміст слайдів
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку