Презентація розробки проведення уроку "Методика організації проведення уроку"
Про матеріал
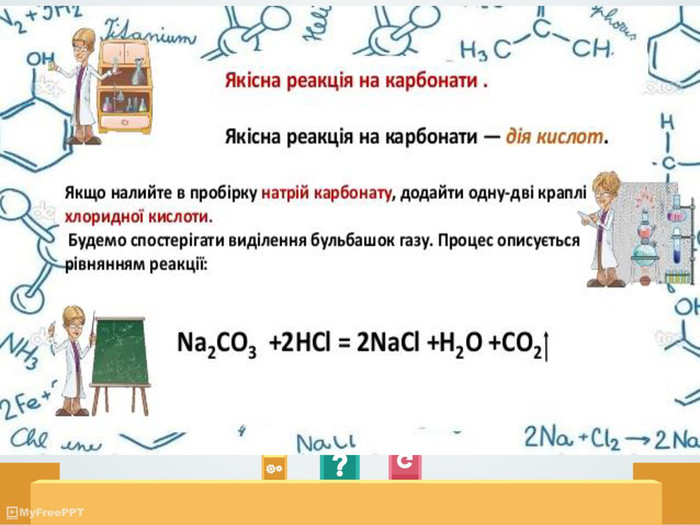
Конкурсна розробка презентації уроку , хімія , 9 клас на тему : “Якісні реакції на деякі йони. Застосування реакцій”
Методика організації дослідницько-пошукової роботи учнів на уроках хімії Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку