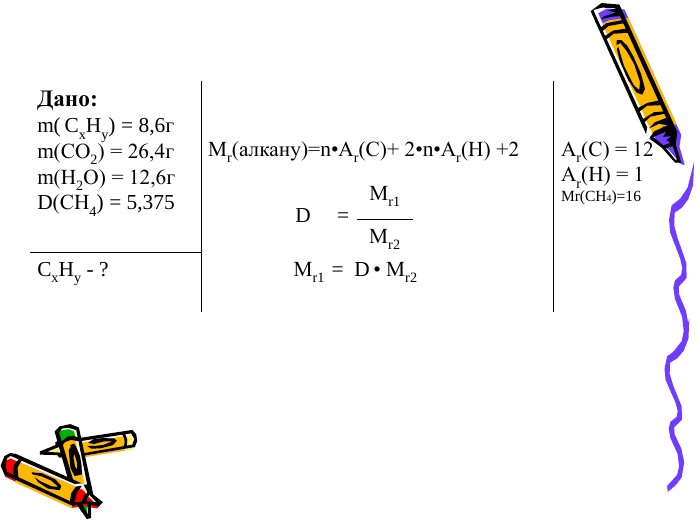
Презентація РОЗВ’ЯЗАННЯ ЗАДАЧ НА ЗНАХОДЖЕННЯ ФОРМУЛИ СПОЛУКИ, ЩО ЗГОРІЛА, ЗА ВІДОМИМИ МАСАМИ ЧИ ОБ’ЄМАМИ ПРОДУКТІВ РЕАКЦІЇ
Про матеріал
Основним завдання навчання є формування різнобічно розвиненої, комунікативної, компетентної особистості, здатної реалізувати набуті знання, вміти критично мислтити. Вміння розв"язуати хімічні задачі входить до математичної компетентності. Математична компетентність включає елементи логічної діяльності. Вона як раз і формується під час розв"язування задач. Перегляд файлу
Зміст слайдів
ppt
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку