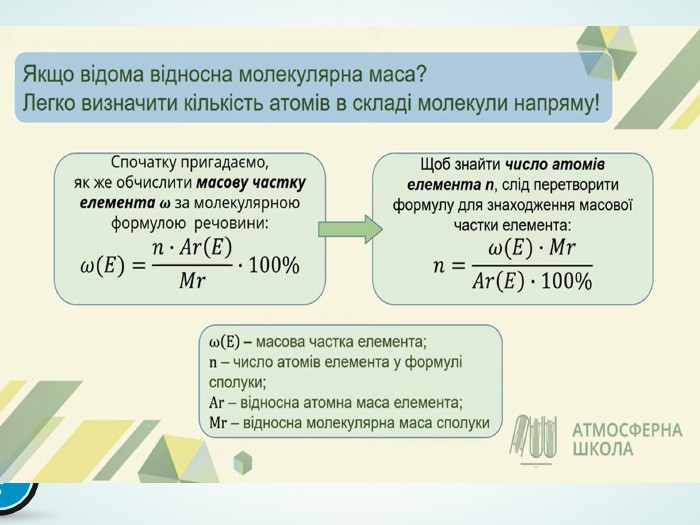
Презентація "Розв'язування задач з виведення молекулярної формули речовин за масовими частками елементів"
Про матеріал
Розглянуто алгоритм та приклади розв'язування задач різного рівня складності Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
-
Задача про вибухівку - супер!


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку