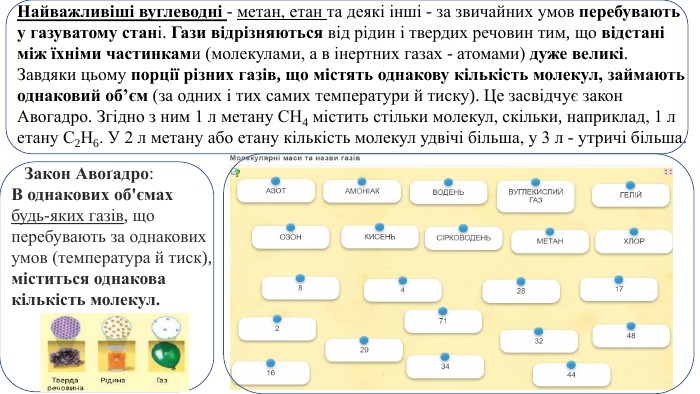
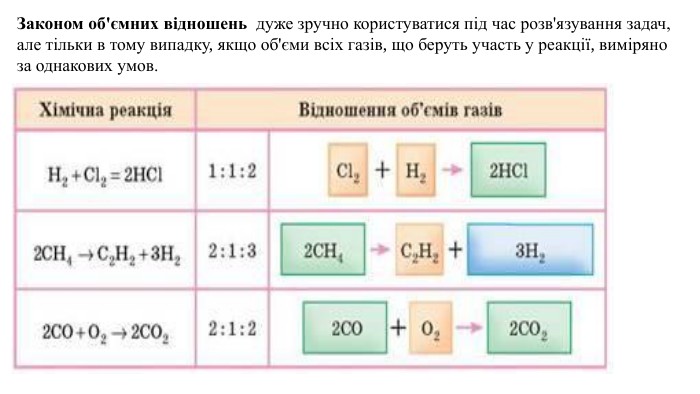
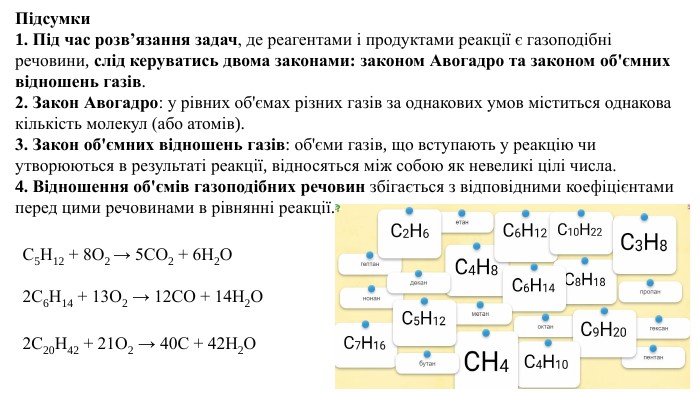
Презентація. Співвідношення об'ємів газів у хімічних реакціях.
Про матеріал
Пропоную до уваги добірку навчального матеріала у вигляді презентації. Презентація за темою "Співвідношення об'ємів газів у хімічних реакціях " може бути корисною та використана під час підготовки до уроку або під час уроку онлайн або офлайн заняття. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
дякую
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку