Презентація "Ступінь окиснення елементів"
Про матеріал
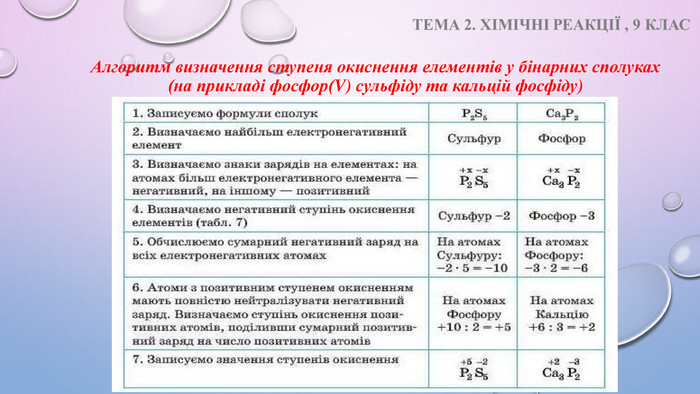
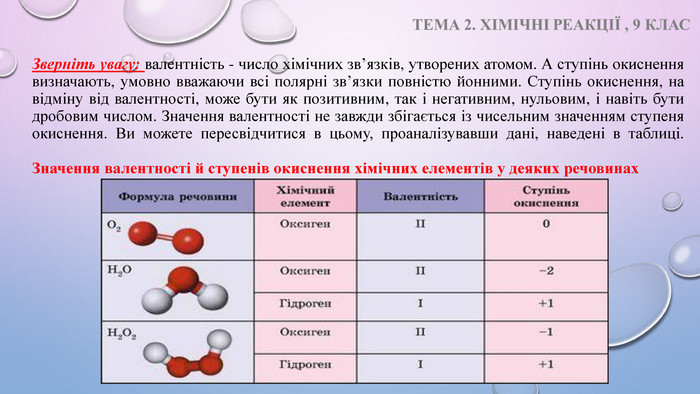
Презентація на тему "Ступінь окиснення. Визначення ступеня окиснення елемента за хім формулою сполуки" 9 клас Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
-
Щиро дякую !
pptx
До підручника
Хімія 9 клас (Григорович О.В.)
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку