Презентація "Тепловий ефект хімічної реакції. Екзотермічні та ендотермічні реакції. Термохімічні рівняння"
Про матеріал
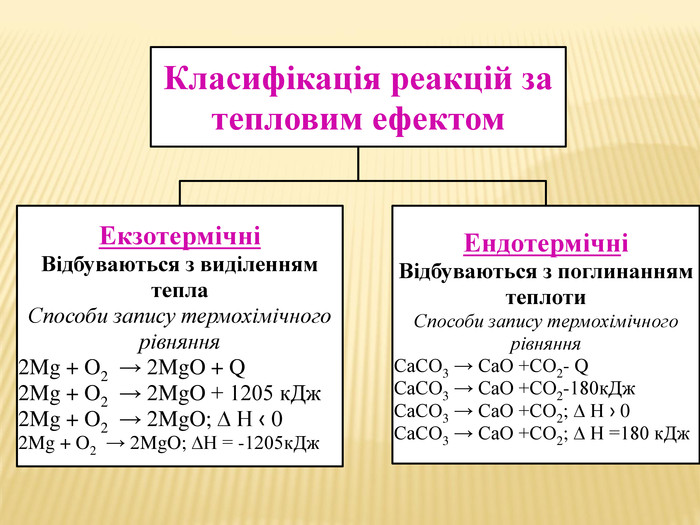
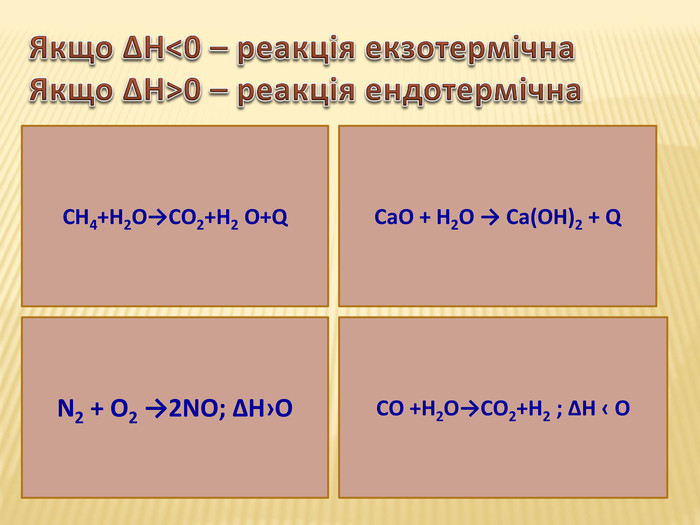
Презентація "Тепловий ефект хімічної реакції. Екзотермічні та ендотермічні реакції. Термохімічні рівняння" допоможе вчителю вдало провести урок із відео-дослідами, різними цікавими завданнями. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки

Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку



























-

Юсин Надія Улянівна
18.12.2023 в 18:52
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Хаблак Людмила
19.11.2023 в 17:04
Дякую!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Кривобородько Віра Борисівна
12.12.2022 в 14:15
Дякую за презентаціію
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Фесенко Надежда
07.12.2022 в 19:53
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 1 відгук