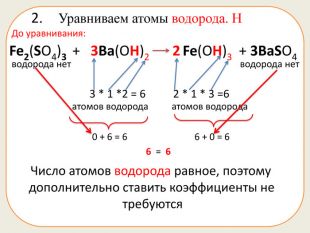
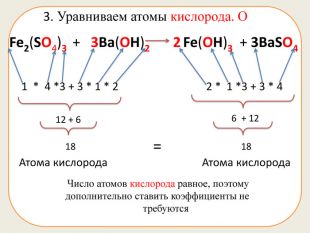
Презентація Вчимося підбирати коефіцієнти у хімічних рівняннях
Про матеріал
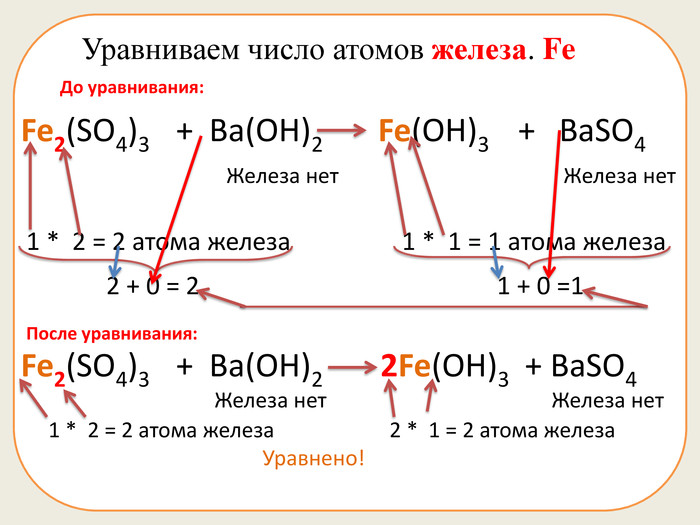
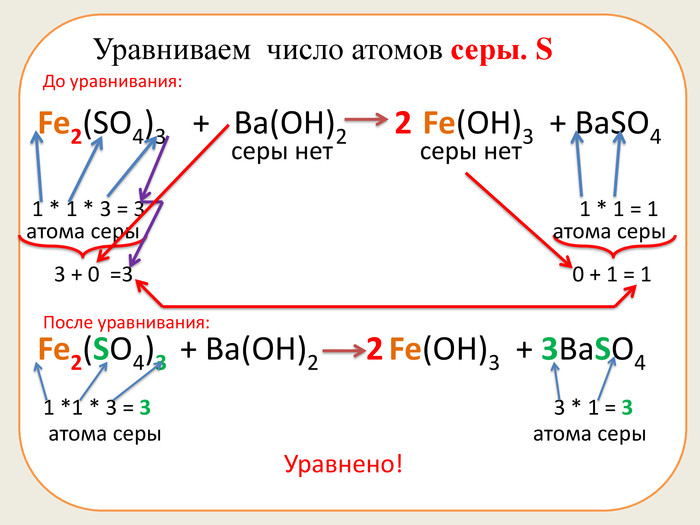
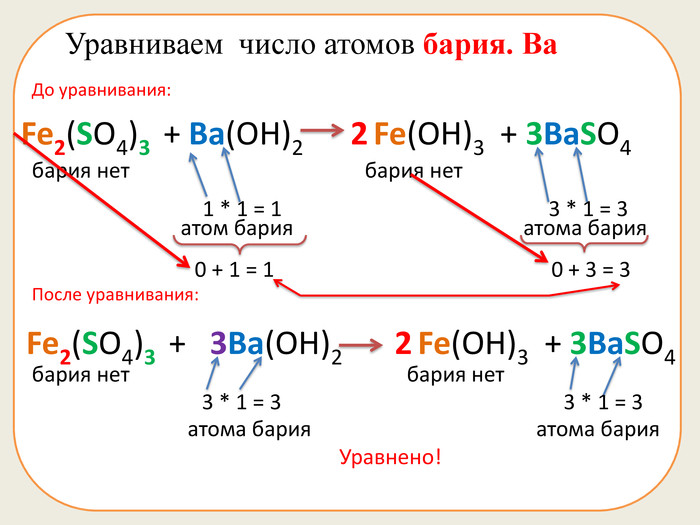
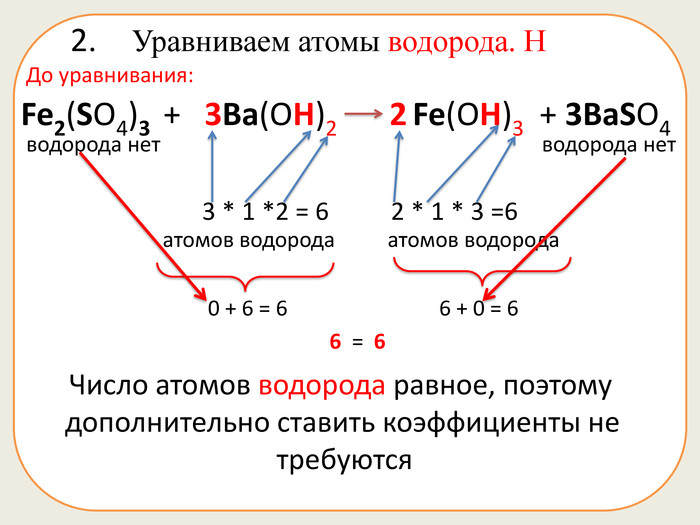
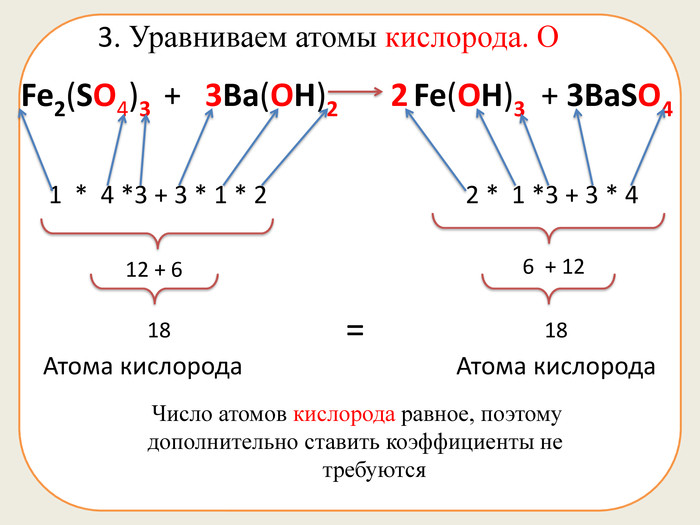
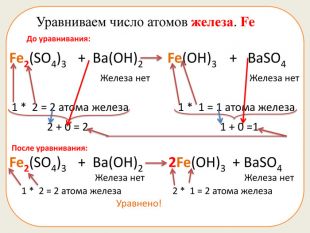
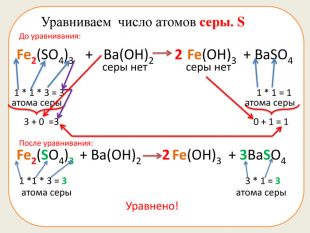
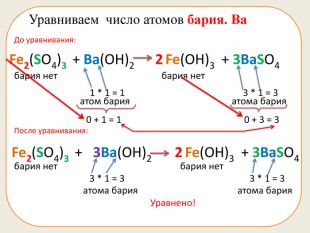
Презентація складається з 20 рівняннь, у яких треба підібрати коефіцієнти. Розрахована на учнів 7 класу. Підійде в якості домашньої роботи, або може бути використана під час самостійної роботи.
Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку