Презентація «Вуглеводи» 9 клас
Вуглеводи: глюкоза, сахароза, крохмаль, целюлоза. Молекулярні формули, фізичні властивості, поширення і утворення в природі. Крохмаль і целюлоза – природні полімери. Застосування вуглеводів, їхня біологічна роль.


















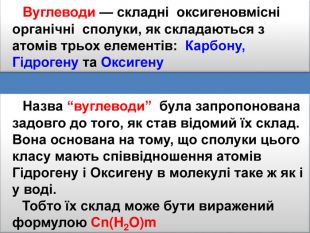
Вуглеводи — складні оксигеновмісні органічні сполуки, як складаються з атомів трьох елементів: Карбону, Гідрогену та Оксигену Назва “вуглеводи” була запропонована задовго до того, як став відомий їх склад. Вона основана на тому, що сполуки цього класу мають співвідношення атомів Гідрогену і Оксигену в молекулі таке ж як і у воді. Тобто їх склад може бути виражений формулою Сn(H2 O)m
Вуглеводи є найпоширенішими в природі органічними сполуками. У рослинах міститься до 80% вуглеводів, а в організмі тварин і людини – до 20%. Їжа людини на 70% складається з вуглеводів. Глюкоза, або виноградний цукор – важливий представник вуглеводів Емпірична формула глюкози – С6 Н12 О6
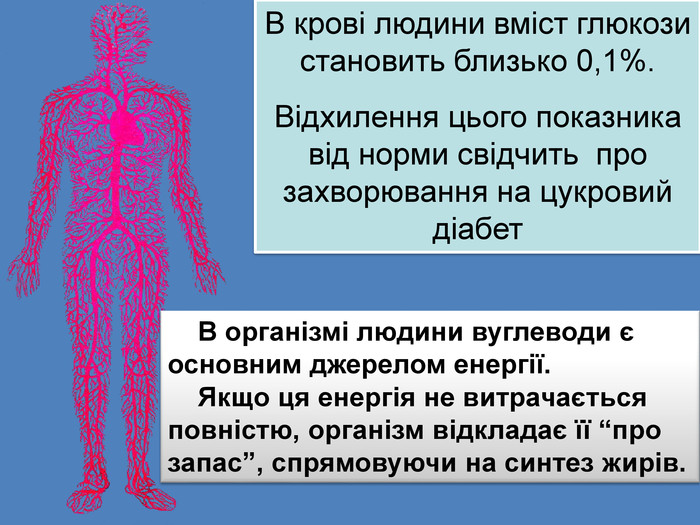
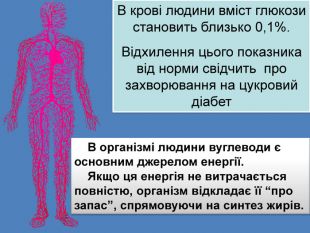
В організмі людини вуглеводи є основним джерелом енергії. Якщо ця енергія не витрачається повністю, організм відкладає її “про запас”, спрямовуючи на синтез жирів. В крові людини вміст глюкози становить близько 0,1%. Відхилення цього показника від норми свідчить про захворювання на цукровий діабет
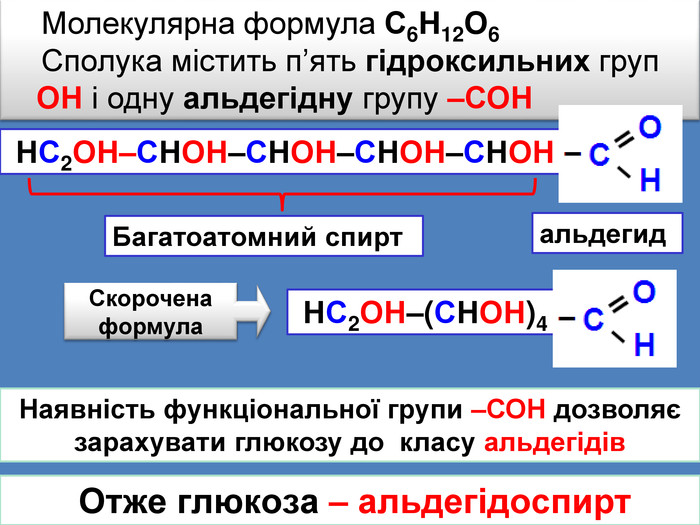
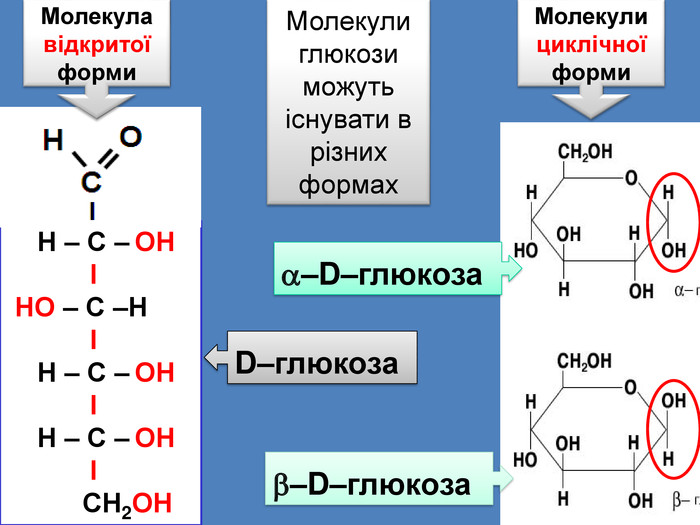
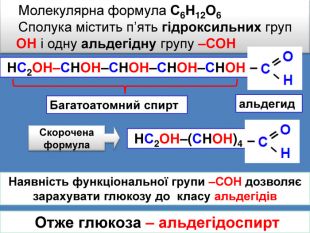
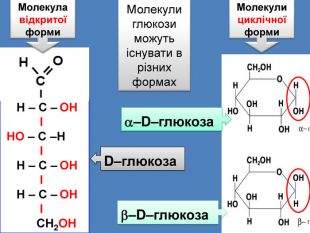
Наявність функціональної групи –СОН дозволяє зарахувати глюкозу до класу альдегідів НС2 ОН–СНОН–СНОН–СНОН–СНОНМолекулярна формула С6 Н12 О6 Сполука містить п’ять гідроксильних груп ОН і одну альдегідну групу –СОН НС2 ОН–(СНОН)4 Скороченаформула. Багатоатомний спиртальдегид Отже глюкоза – альдегідоспирт
У промисловому масштабі глюкозу одержують гідролізом крохмалю (у присутності кислот) з деревини (целюлози). Глюкоза застосовується в медицині для готування лікувальних препаратів, консервування крові, внутрішньовенного вливання і т.д. Глюкоза широко застосовується в кондитерському виробництві, у виробництві дзеркал і оптичних пристроїв (срібнення). Застосування глюкози
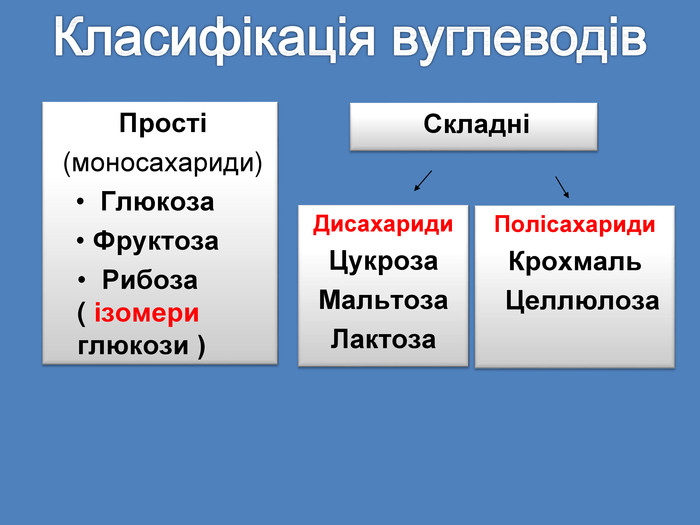
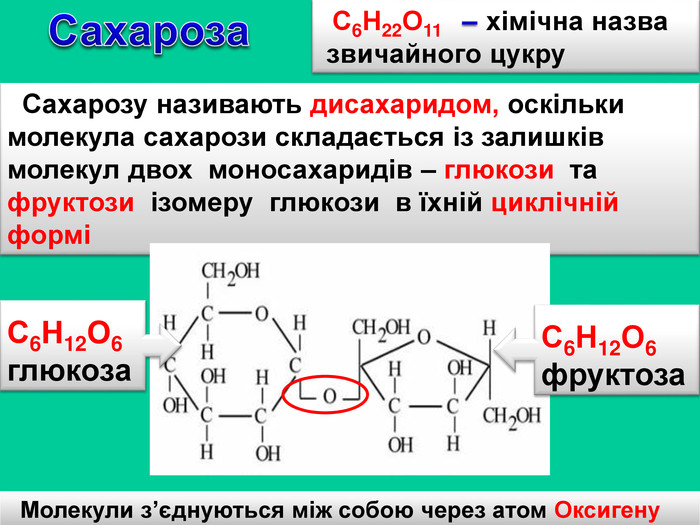
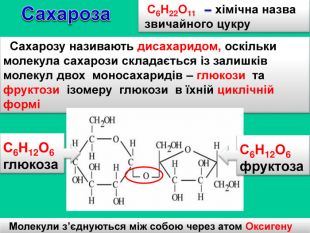
Сахароза. С6 Н22 О11 – хімічна назва звичайного цукру Сахарозу називають дисахаридом, оскільки молекула сахарози складається із залишків молекул двох моносахаридів – глюкози та фруктози ізомеру глюкози в їхній циклічній форміМолекули з’єднуються між собою через атом Оксигену. С6 Н12 О6глюкоза. С6 Н12 О6фруктозаr
Сахароза (буряковий цукор) – біла кристалічна речовина, більш солодка ніж глюкоза, добре розчинна у воді. При нагріванні в присутності іонів Гідрогену сахароза підлягає гідролізу. С6 Н22 О11 + Н2 О → С6 Н12 О6 + С6 Н12 О6 сахароза глюкоза фруктоза Ця хімічна реакція використовується для виробництва штучного меду
Сахароза (буряковий цукор) – міститься у буряках, цукровій тростині та соку дерев клена. Мальтоза (солодовй цукор) – міститься у солоді – пророщених, висушених та розмолотих зернах ячменю, пшениці з яких виготовляють етиловий спирт. Лактоза – молочний цукор. Міститься в молоці (від 4 до 6%)Добавити малюнок
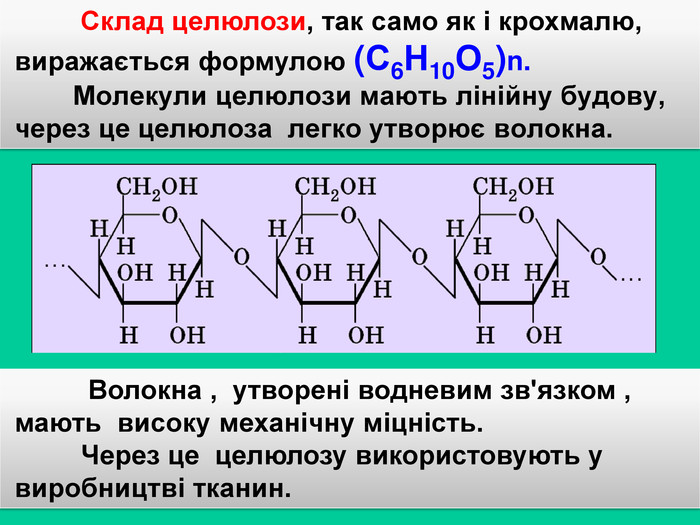
Крохмаль та целюлоза Глюкоза, що утворюється в результаті фотосинтезу, накопичується в плодах, листі та стеблах рослин у формі різних полімерів: крохмалю і целюлози (клітковина) Крохмаль і целюлоза – природні полімери, загальна формула яких (С6 Н10 О5)n Рівняння утворення крохмалю або целюлози: n. С6 Н12 О6 (С6 Н10 О5)n + n. Н2 ОЦя реакція називається реакц. поліконденсації. Мономер – глюкоза. Полімер – целюлоза або крохмаль
Крохмаль Крохмаль – білий порошок, несмачний, нерозчинний у воді. У гарячій воді набухає, утворюючи клейстер (колоїдний розчин). Крохмаль – продукт фотосинтезу. Він є запасною поживною речовиною рослин. Найбільшу кількість крохмалю містять зерна рису (до 80%), пшениці (до 75%), кукурудзи (до 72%), бульби картоплі (до 24%)
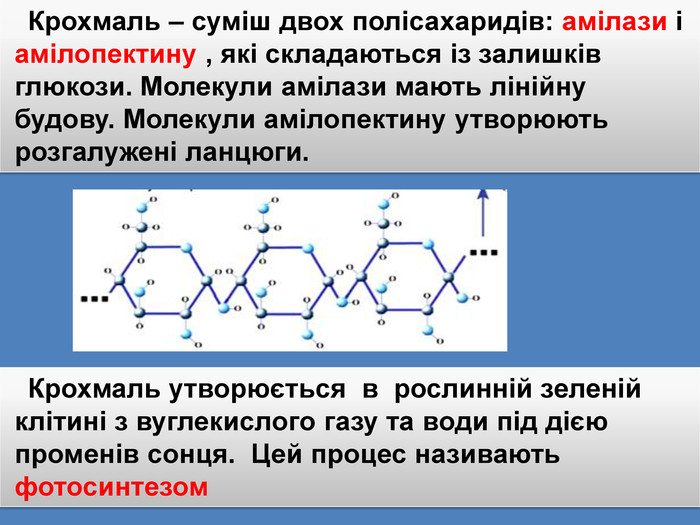
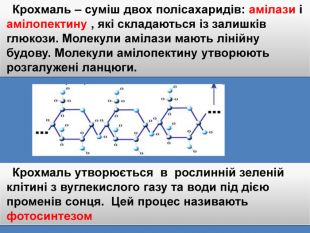
Крохмаль – суміш двох полісахаридів: амілази і амілопектину , які складаються із залишків глюкози. Молекули амілази мають лінійну будову. Молекули амілопектину утворюють розгалужені ланцюги. Крохмаль утворюється в рослинній зеленій клітині з вуглекислого газу та води під дією променів сонця. Цей процес називають фотосинтезом
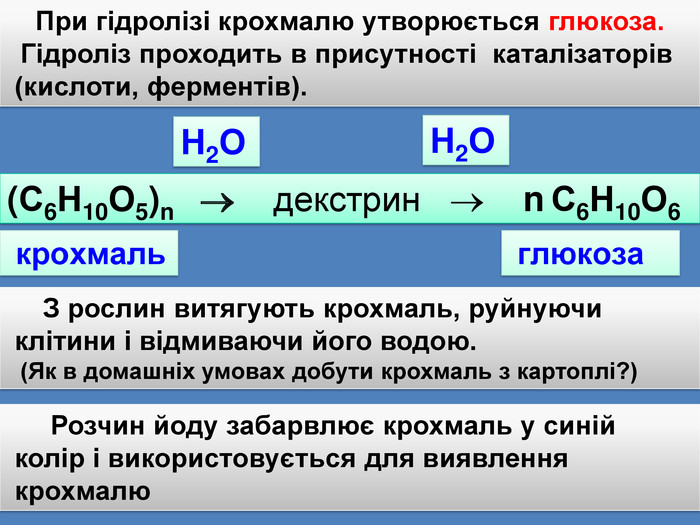
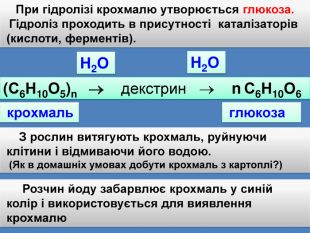
При гідролізі крохмалю утворюється глюкоза. Гідроліз проходить в присутності каталізаторів (кислоти, ферментів).(С6 Н10 О5)n декстрин n С6 Н10 О6 Н2 ОН2 О крохмаль глюкоза З рослин витягують крохмаль, руйнуючи клітини і відмиваючи його водою. (Як в домашніх умовах добути крохмаль з картоплі?) Розчин йоду забарвлює крохмаль у синій колір і використовується для виявлення крохмалю
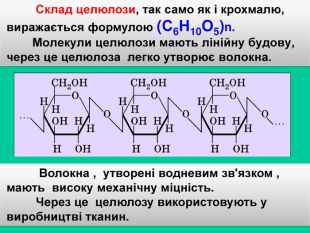
Целюлоза – волокниста речовина, не розчиняється воді й в органічних розчинниках, але добре розчиняється в аміачному розчині купрум (ІІ) гідроксиду. З цього розчину кислоти осаджують целюлозу у вигляді волокон (гідратцелюлоза) В будові макромолекул крохмалю і целюлози є відмінності: Макромолекули складаються з різних ізомерів глюкози;Молекули глюкози мають лінійну структуру;Молекули крохмалю – як лінійну так і розгалужену структуру;
Відмінності в будові молекул визначають відмінності у властивостях полімерів: крохмаль – продукт харчування, целюлоза для цієї мети не придатна. Целюлоза як і крохмаль не має альдегідної групи тому не дає реакції “срібного дзеркала” Целюлозу використовують для виробництва хімічних волокон (штучного шовку), різних видів тканин і сортів паперу, пластмас, лаків тощо. Використання целюлози
Джерела. Григорович О. В. Хімія: підруч. для 9 класу загальноосвіт. навч.закл./ О. В. Григорович .̶ Харків: Вид-во «Ранок», 2017 Шаповалов С. А. Хімія. Довідник старшокласника та абітурієнта. Харків. Торсінг, 2005. Данильченко В.Є Халімон Є. В. Хімія. Навчальний посібник. 8-9 класи – Харків.: Країна мрій, 2008. – 128с.


про публікацію авторської розробки
Додати розробку




















-

Шкідченко Надія Миколаївна
02.05.2025 в 10:50
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Шкідченко Надія Миколаївна
02.05.2025 в 10:50
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Хода Галина
01.04.2025 в 14:29
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Линник Олена
26.04.2023 в 19:55
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Любченко Елена
15.08.2022 в 21:47
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Бицина Оксана Валеріївна
27.04.2022 в 21:56
Загальна:
4.7
Структурованість
5.0
Оригінальність викладу
4.0
Відповідність темі
5.0
-

Чакава Наталія
18.04.2022 в 09:13
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Манжос Олена Юріївна
07.05.2021 в 13:25
Є помилки в формулах. Матеріал розрахований і на 9, і на 10 клас:(((
Загальна:
3.7
Структурованість
5.0
Оригінальність викладу
3.0
Відповідність темі
3.0
-

Фурсова Олена Володимирівна
25.04.2021 в 12:04
Дякую
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Сенецька Оксана Анатоліївна
18.04.2021 в 16:10
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Сивець Наталія
07.04.2021 в 09:07
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Сивець Наталія
07.04.2021 в 09:07
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Берiл Наталiя Олексіївна
04.04.2021 в 22:02
Загальна:
4.7
Структурованість
5.0
Оригінальність викладу
4.0
Відповідність темі
5.0
-

Тодоров Леонід
30.03.2021 в 20:22
Загальна:
4.7
Структурованість
5.0
Оригінальність викладу
4.0
Відповідність темі
5.0
-

Струць Оксана Володимирівна
30.03.2021 в 19:46
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Хомич Людмила Миколаївна
10.04.2020 в 09:45
Дякую за презентацію.
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Паращак Наталія Миколаївна
22.04.2019 в 11:32
дякую, колего, за матеріал до уроку!
Загальна:
4.7
Структурованість
5.0
Оригінальність викладу
4.0
Відповідність темі
5.0
Показати ще 14 відгуків