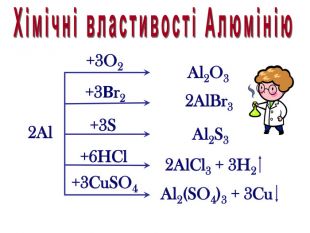
Презентація з хімії "Алюміній як хімічний елемент і проста речовина. Фізичні та хімічні властивості алюмінію"
Про матеріал
Мета: розширити та поглибити знання про метали на прикладі Алюмінію — представника головної підгрупи III групи; розглянути положення Алюмінію в Періодичній таблиці, його фізичні та хімічні властивості. Актуалізувати знання по іншим темам, показати учням зв'язок науки та життя, підтримувати інтерес до хімії, розвивати вміння логічно мислити, працювати з підручником та додатковим матеріалом.
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
ppt
До підручника
Хімія (профільний рівень) 10 клас (Буринська Н.М. та інші)
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку














![Алюміній є амфотерним елементом: взаємодіє с кислотами та лугами. 2Al + 6HCl(розбавлена) = 2AlCl3 + 3H2 8Al + 15H2SO4(конц.) 4Al2(SO4)3 + 3H2S + 12H2O Al + 6HNO3 (конц.) Al(NO3)3 + 3NO2 + 3H2O 2Al + 6NaOH 2Na3AlO3 + 3H2 2Al + 2NaOH + 6H2O = 2Na[Al(OН)4] + 3H2 2Al + 6NaOH(надлишок) + 6H2O = 2 Na3[Al(OH)6] + 3H2 Алюміній є амфотерним елементом: взаємодіє с кислотами та лугами. 2Al + 6HCl(розбавлена) = 2AlCl3 + 3H2 8Al + 15H2SO4(конц.) 4Al2(SO4)3 + 3H2S + 12H2O Al + 6HNO3 (конц.) Al(NO3)3 + 3NO2 + 3H2O 2Al + 6NaOH 2Na3AlO3 + 3H2 2Al + 2NaOH + 6H2O = 2Na[Al(OН)4] + 3H2 2Al + 6NaOH(надлишок) + 6H2O = 2 Na3[Al(OH)6] + 3H2](/uploads/files/161639/58994/63376_images/14.jpg)