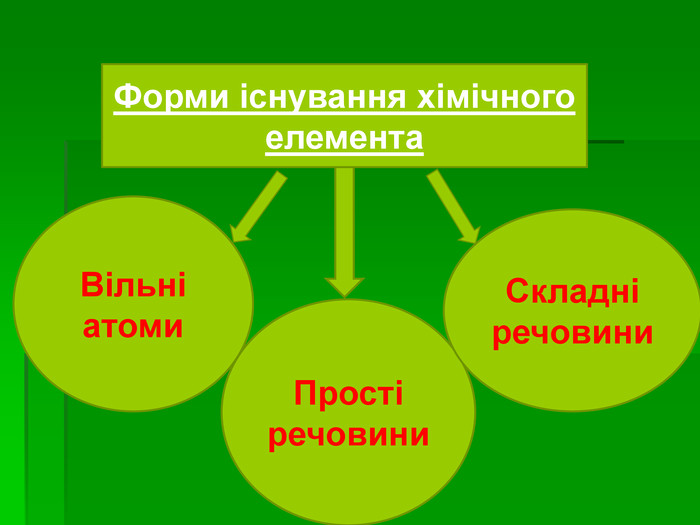
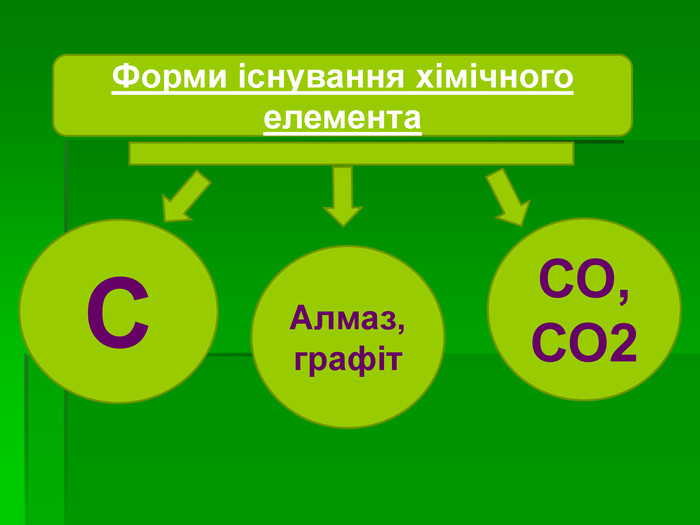
Презентація з хімії на тему " Ступінь окиснення елемента в складній речовині " для 8 класу
Про матеріал
Презентація з хімії на тему "Ступінь окиснення елемента в складній речовині" для 8 класу. Сьогодні презентація стала актуальним інструментом на кожному уроці в творчого вчителя, так як допомагає провести урок цікаво та доступно. Стане в пригоді кожному творчому вчителю.
Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку