Презентація "Загальні способи добування солей"
Про матеріал
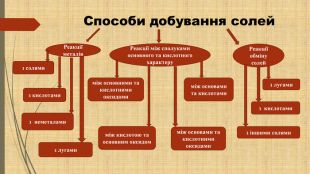
Презентація "Загальні способи добування солей" знайомить учнів 8 класу з 11 способами добування солей. Презентація створена за підручником П.П.Попеля, Л.С.Криклі "Хімія-8", Київ,"Академія", 2016 Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку



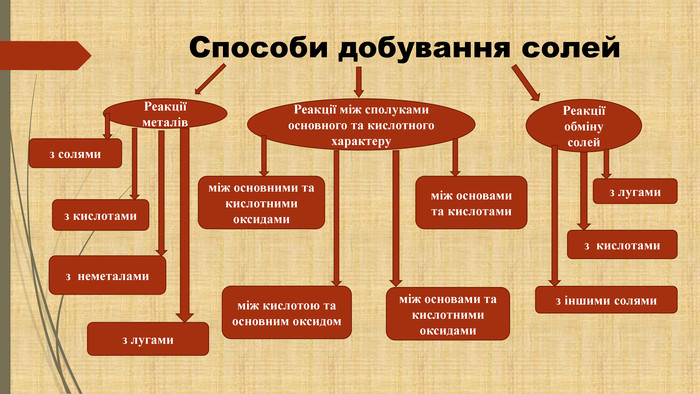
![Добування солей в реакціях за участю металів. Спосіб 1: метал + неметал = сіль безоксигенова 2 Li + S = Li2 SСпосіб 2: метал + кислота (розчин) = сіль + водень Mg + 2 HCl = Mg. Cl2 + H2↑ Zn + H2 SO4 = Zn. SO4 + H2↑Спосіб 3: метал + луг = сіль + водень (Метал повинен походити від елемента, що утворює амфотерні сполуки) Be + 2 Na. OH = Na2 Be. O2 + H2↑ (при нагріванні) Be + 2 KOH + 2 H2 O = K2 [Be(OH)4] + H2↑ Cпосіб 4: метал1 + сіль1 (розчин) = метал2 + сіль2 Fe + Cu(NO3)2 = Cu + Fe(NO3)2 Добування солей в реакціях за участю металів. Спосіб 1: метал + неметал = сіль безоксигенова 2 Li + S = Li2 SСпосіб 2: метал + кислота (розчин) = сіль + водень Mg + 2 HCl = Mg. Cl2 + H2↑ Zn + H2 SO4 = Zn. SO4 + H2↑Спосіб 3: метал + луг = сіль + водень (Метал повинен походити від елемента, що утворює амфотерні сполуки) Be + 2 Na. OH = Na2 Be. O2 + H2↑ (при нагріванні) Be + 2 KOH + 2 H2 O = K2 [Be(OH)4] + H2↑ Cпосіб 4: метал1 + сіль1 (розчин) = метал2 + сіль2 Fe + Cu(NO3)2 = Cu + Fe(NO3)2](/uploads/files/617808/178539/191288_images/4.jpg)