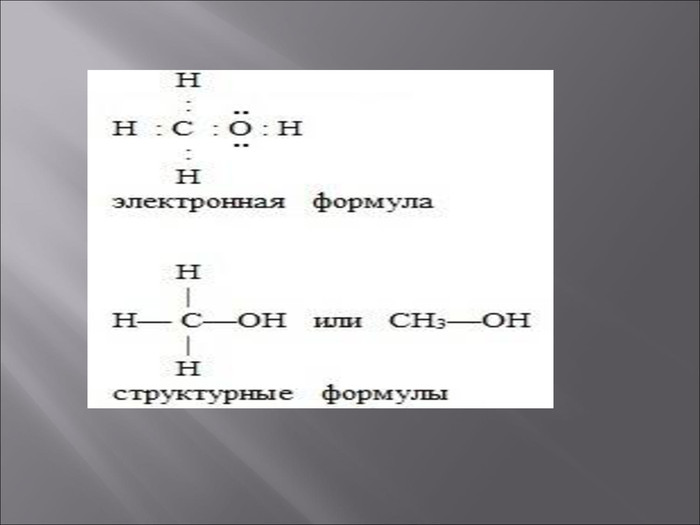
Презентація: Застосування метанолу
Про матеріал
Презентація чудово підійде до одного з етапів уроку: Застосування спиртів, або як проект Перегляд файлу
Зміст слайдів
ppt
До підручника
Хімія 9 клас (Савчин М.М.)
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку