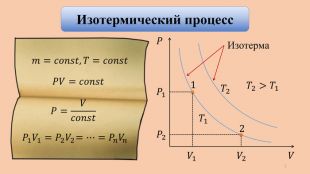
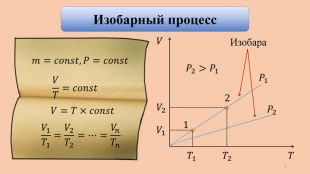
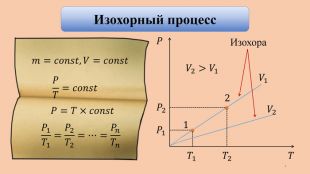
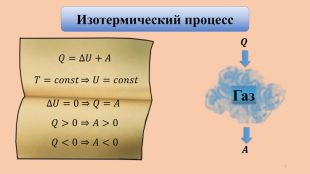
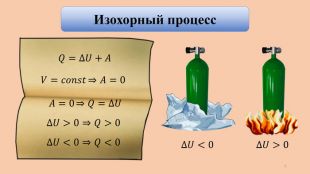
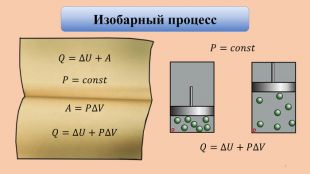
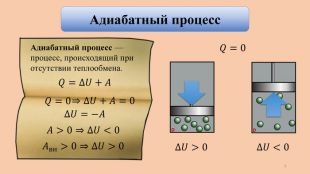
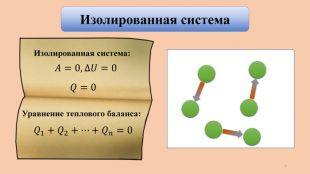
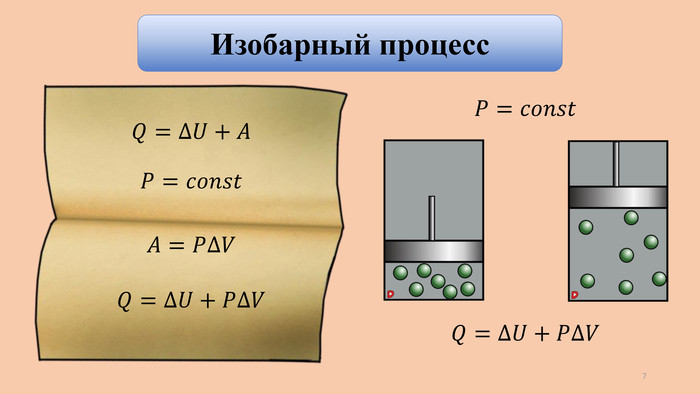
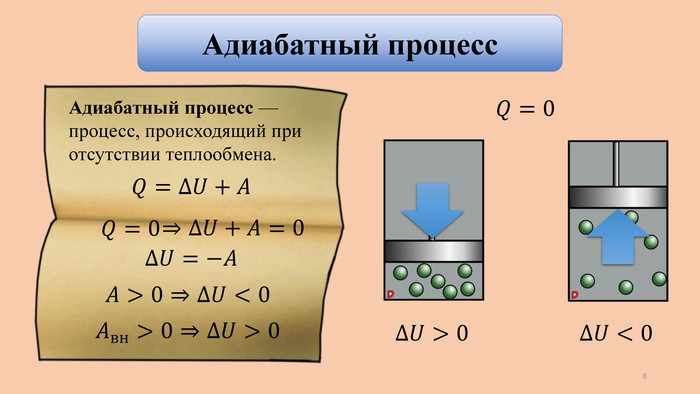
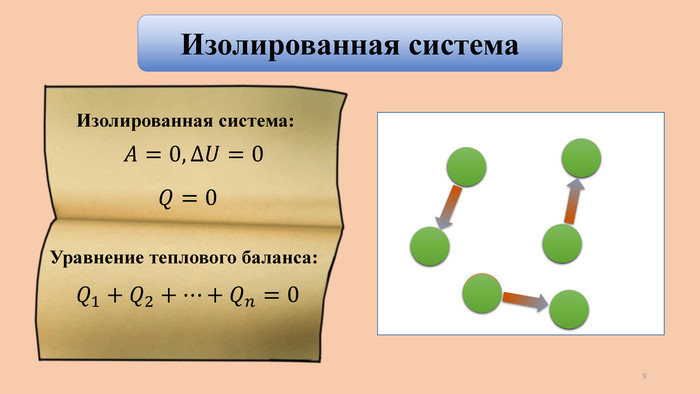
Применение первого закона термодинамики к изопроцессам















Адиабатно расширяясь, водяной пар совершил работу, равную 11 к. Дж. Масса пара составляет 0,5 кг. Если начальная температура пара 390 К, то какова его конечная температура?Дано: 𝑇 − ? 𝑄=0 11 к. Дж 𝐴=11 к. Дж 𝑚=0,5 кг 𝑇0=390 К 𝐻2𝑂 𝑯𝟐𝑶, 𝑻 𝐴=11 к. Дж 𝑯𝟐𝑶, 𝟑𝟗𝟎 К 𝑄=0 390 К 0,5 кг 𝑄=∆𝑈+𝐴 ∆𝑈=−𝐴 ∆𝑈=𝑖2𝑚𝑀𝑅∆𝑇 ∆𝑇=−2𝑖∆𝑈𝑀𝑚𝑅 𝑇−𝑇0=−2𝑖𝐴𝑀𝑚𝑅 𝑇=−2𝑖𝐴𝑀𝑚𝑅+𝑇0 𝑇=−26×11000×0,0180,5×8,31+390=374 К 𝑀𝐻2𝑂=0,018кгмоль 𝑇=−26𝐴𝑀𝑚𝑅+𝑇0 𝑀𝐻2𝑂=0,018кгмоль 10
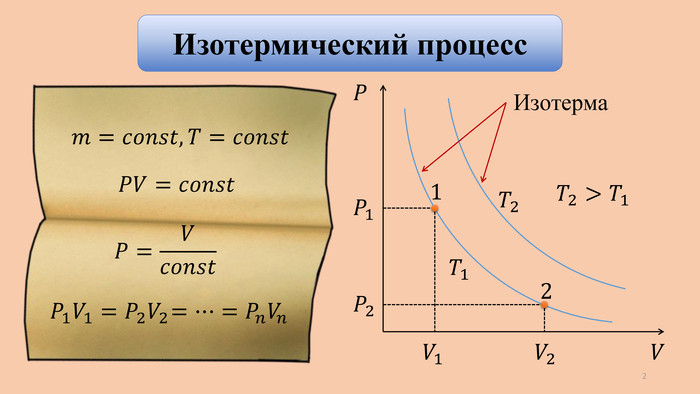
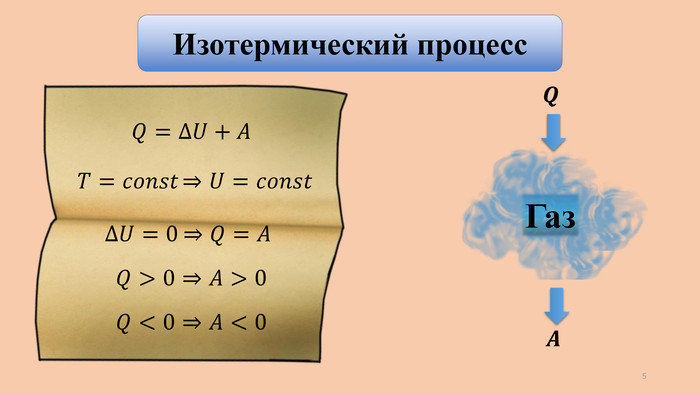
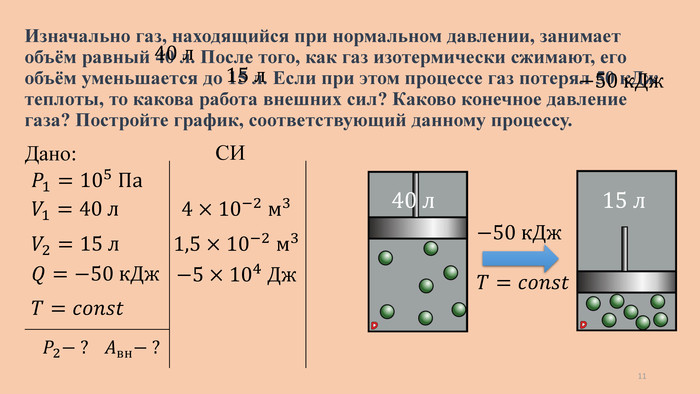
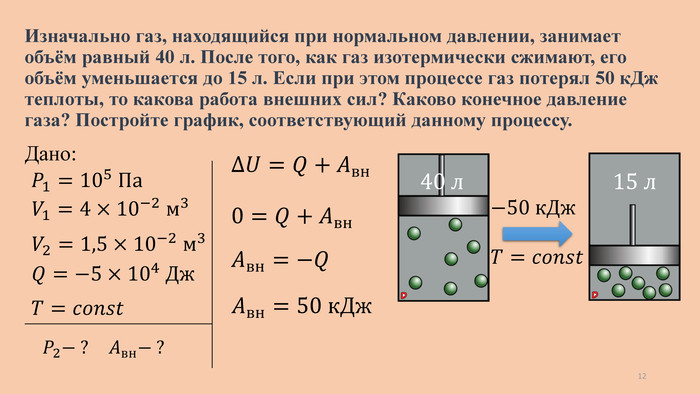
Изначально газ, находящийся при нормальном давлении, занимает объём равный 40 л. После того, как газ изотермически сжимают, его объём уменьшается до 15 л. Если при этом процессе газ потерял 50 к. Дж теплоты, то какова работа внешних сил? Каково конечное давление газа? Постройте график, соответствующий данному процессу.40 л 15 л −50 к. Дж 𝑇=𝑐𝑜𝑛𝑠𝑡 Дано: 𝑃2− ? 𝑃1=105 Па −50 к. Дж 𝑄=−50 к. Дж СИ4×10−2 м3 𝑉1=40 л 𝑉2=15 л 15 л 40 л 1,5×10−2 м3 −5×104 Дж 𝑇=𝑐𝑜𝑛𝑠𝑡 𝐴вн− ? 11
Изначально газ, находящийся при нормальном давлении, занимает объём равный 40 л. После того, как газ изотермически сжимают, его объём уменьшается до 15 л. Если при этом процессе газ потерял 50 к. Дж теплоты, то какова работа внешних сил? Каково конечное давление газа? Постройте график, соответствующий данному процессу. Дано: 𝑃2− ? 𝑃1=105 Па 𝑄=−5×104 Дж 𝑉1=4×10−2 м3 𝑉2=1,5×10−2 м3 𝑇=𝑐𝑜𝑛𝑠𝑡 ∆𝑈=𝑄+𝐴вн 0=𝑄+𝐴вн 𝐴вн=−𝑄 𝐴вн=50 к. Дж 40 л 15 л −50 к. Дж 𝑇=𝑐𝑜𝑛𝑠𝑡 𝐴вн− ? 12
Изначально газ, находящийся при нормальном давлении, занимает объём равный 40 л. После того, как газ изотермически сжимают, его объём уменьшается до 15 л. Если при этом процессе газ потерял 50 к. Дж теплоты, то какова работа внешних сил? Каково конечное давление газа? Постройте график, соответствующий данному процессу.40 л 15 л −50 к. Дж 𝑇=𝑐𝑜𝑛𝑠𝑡 Дано: 𝑃2− ? 𝑃1=105 Па 𝑄=−5×104 Дж 𝑉1=4×10−2 м3 𝑉2=1,5×10−2 м3 𝑇=𝑐𝑜𝑛𝑠𝑡 𝑃𝑉=𝑐𝑜𝑛𝑠𝑡, при 𝑇=𝑐𝑜𝑛𝑠𝑡 𝑃1𝑉1=𝑃2𝑉2 𝑃2=𝑃1𝑉1𝑉2 𝑃2=105×4×10−21,5×10−2≈267 к. Па 𝐴вн− ? 13
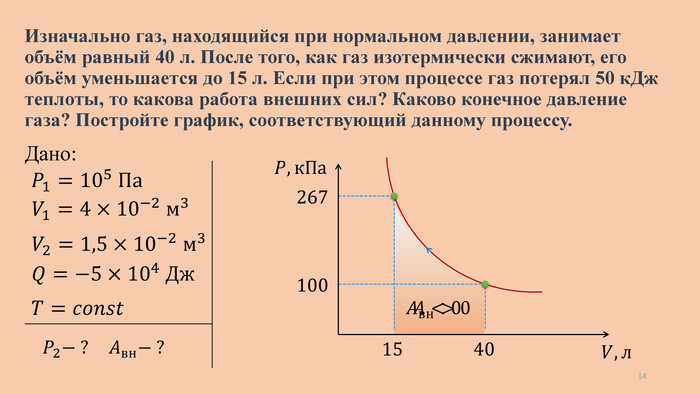
Изначально газ, находящийся при нормальном давлении, занимает объём равный 40 л. После того, как газ изотермически сжимают, его объём уменьшается до 15 л. Если при этом процессе газ потерял 50 к. Дж теплоты, то какова работа внешних сил? Каково конечное давление газа? Постройте график, соответствующий данному процессу. Дано: 𝑃2− ? 𝑃1=105 Па 𝑄=−5×104 Дж 𝑉1=4×10−2 м3 𝑉2=1,5×10−2 м3 𝑇=𝑐𝑜𝑛𝑠𝑡 𝐴вн− ? 267 100 𝑃, к. Па 𝑉, л 15 40 𝐴вн>0 𝐴<0 14
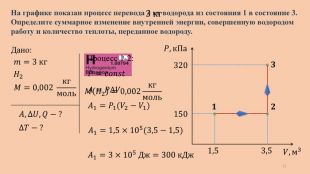
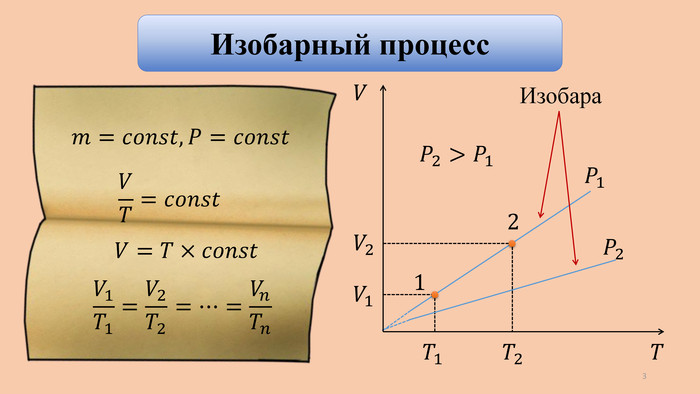
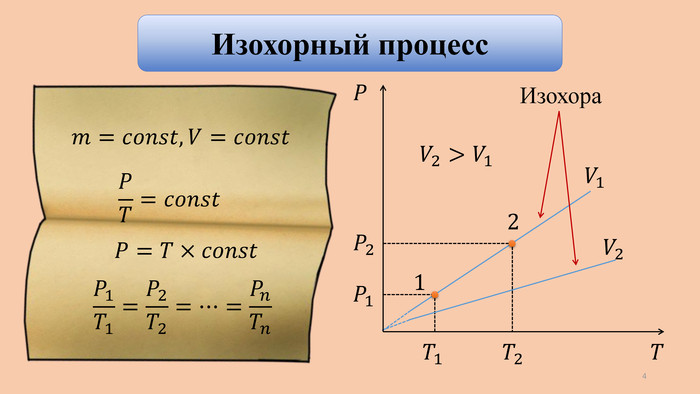
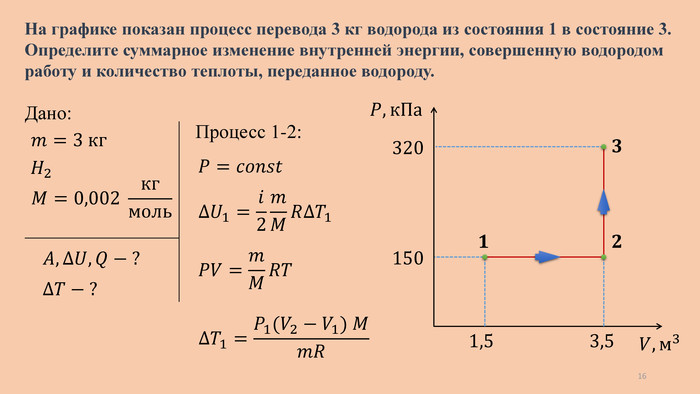
320 150 𝑃, к. Па 𝑉, м3 1,5 3,5 𝟏 𝟐 𝟑 Дано: 𝐴,∆𝑈, 𝑄 − ? 𝐻2 𝑚=3 кг На графике показан процесс перевода 3 кг водорода из состояния 1 в состояние 3. Определите суммарное изменение внутренней энергии, совершенную водородом работу и количество теплоты, переданное водороду.𝑀=0,002 кгмоль ∆𝑇 − ? 3 кг 𝑀𝐻2=0,002кгмоль Процесс 1-2:𝑃=𝑐𝑜𝑛𝑠𝑡 𝐴=𝑃∆𝑉 𝐴1=𝑃1(𝑉2−𝑉1) 𝐴1=1,5×105(3,5−1,5) 𝐴1=3×105 Дж=300 к. Дж 15
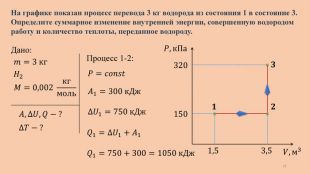
320 150 𝑃, к. Па 𝑉, м3 1,5 3,5 𝟏 𝟐 𝟑 Дано: 𝐴,∆𝑈, 𝑄 − ? 𝐻2 𝑚=3 кг На графике показан процесс перевода 3 кг водорода из состояния 1 в состояние 3. Определите суммарное изменение внутренней энергии, совершенную водородом работу и количество теплоты, переданное водороду.𝑀=0,002 кгмоль ∆𝑇 − ? Процесс 1-2:𝑃=𝑐𝑜𝑛𝑠𝑡 ∆𝑈1=𝑖2𝑚𝑀𝑅∆𝑇1 𝑃𝑉=𝑚𝑀𝑅𝑇 ∆𝑇1=𝑃1(𝑉2−𝑉1) 𝑀𝑚𝑅 16
320 150 𝑃, к. Па 𝑉, м3 1,5 3,5 𝟏 𝟐 𝟑 Дано: 𝐴,∆𝑈, 𝑄 − ? 𝐻2 𝑚=3 кг На графике показан процесс перевода 3 кг водорода из состояния 1 в состояние 3. Определите суммарное изменение внутренней энергии, совершенную водородом работу и количество теплоты, переданное водороду.𝑀=0,002 кгмоль ∆𝑇 − ? Процесс 1-2:𝑃=𝑐𝑜𝑛𝑠𝑡 ∆𝑈1=𝑖2𝑃1(𝑉2−𝑉1) ∆𝑈1=52𝑃1(𝑉2−𝑉1) ∆𝑈1=52×3×105 ∆𝑈1=7,5×105 Дж=750 к. Дж 17
320 150 𝑃, к. Па 𝑉, м3 1,5 3,5 𝟏 𝟐 𝟑 Дано: 𝐴,∆𝑈, 𝑄 − ? 𝐻2 𝑚=3 кг На графике показан процесс перевода 3 кг водорода из состояния 1 в состояние 3. Определите суммарное изменение внутренней энергии, совершенную водородом работу и количество теплоты, переданное водороду.𝑀=0,002 кгмоль ∆𝑇 − ? Процесс 1-2:𝑃=𝑐𝑜𝑛𝑠𝑡 𝑄1=∆𝑈1+𝐴1 𝐴1=300 к. Дж ∆𝑈1=750 к. Дж 𝑄1=750+300=1050 к. Дж 18
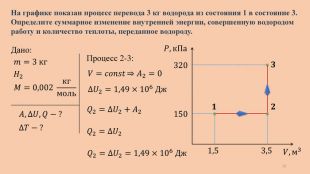
320 150 𝑃, к. Па 𝑉, м3 1,5 3,5 𝟏 𝟐 𝟑 Дано: 𝐴,∆𝑈, 𝑄 − ? 𝐻2 𝑚=3 кг На графике показан процесс перевода 3 кг водорода из состояния 1 в состояние 3. Определите суммарное изменение внутренней энергии, совершенную водородом работу и количество теплоты, переданное водороду.𝑀=0,002 кгмоль ∆𝑇 − ? Процесс 2-3:𝑉=𝑐𝑜𝑛𝑠𝑡 ⇒𝐴2=0 ∆𝑈2=𝑖2𝑚𝑀𝑅∆𝑇2 ∆𝑇2=𝑉2(𝑃3−𝑃2) 𝑀𝑚𝑅 ∆𝑈2=𝑖2𝑉2(𝑃3−𝑃2) ∆𝑈2=52×3, 5(3,2−1,5)×105 19
320 150 𝑃, к. Па 𝑉, м3 1,5 3,5 𝟏 𝟐 𝟑 Дано: 𝐴,∆𝑈, 𝑄 − ? 𝐻2 𝑚=3 кг На графике показан процесс перевода 3 кг водорода из состояния 1 в состояние 3. Определите суммарное изменение внутренней энергии, совершенную водородом работу и количество теплоты, переданное водороду.𝑀=0,002 кгмоль ∆𝑇 − ? Процесс 2-3:𝑉=𝑐𝑜𝑛𝑠𝑡 ⇒𝐴2=0 ∆𝑈2=1,49×106 Дж 𝑄2=∆𝑈2+𝐴2 𝑄2=∆𝑈2=1,49×106 Дж 𝑄2=∆𝑈2 20
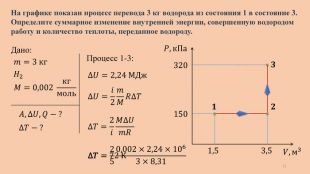
320 150 𝑃, к. Па 𝑉, м3 1,5 3,5 𝟏 𝟐 𝟑 Дано: 𝐴,∆𝑈, 𝑄 − ? 𝐻2 𝑚=3 кг На графике показан процесс перевода 3 кг водорода из состояния 1 в состояние 3. Определите суммарное изменение внутренней энергии, совершенную водородом работу и количество теплоты, переданное водороду.𝑀=0,002 кгмоль ∆𝑇 − ? Процесс 1-3:∆𝑈=∆𝑈1+∆𝑈2 𝑄=𝑄1+𝑄2 𝐴=𝐴1+𝐴2 ∆𝑈=2,24 МДж 𝑄=2,54 МДж 𝐴=300 к. Дж 21
320 150 𝑃, к. Па 𝑉, м3 1,5 3,5 𝟏 𝟐 𝟑 Дано: 𝐴,∆𝑈, 𝑄 − ? 𝐻2 𝑚=3 кг На графике показан процесс перевода 3 кг водорода из состояния 1 в состояние 3. Определите суммарное изменение внутренней энергии, совершенную водородом работу и количество теплоты, переданное водороду.𝑀=0,002 кгмоль ∆𝑇 − ? Процесс 1-3:∆𝑈=2,24 МДж ∆𝑈=𝑖2𝑚𝑀𝑅∆𝑇 ∆𝑇=2𝑖𝑀∆𝑈𝑚𝑅 ∆𝑇=250,002×2,24×1063×8,31 ∆𝑇=72 К 22
{BC89 EF96-8 CEA-46 FF-86 C4-4 CE0 E7609802}Название процесса. Постоянный параметр. Следствие постоянства параметра. Запись первого закона термодинамики. Изохорный. Объём, V𝐴=0𝑄=∆𝑈Изотермический. Температура, Т∆𝑈=0𝑄=𝐴Изобарный. Давление, Р𝐴=𝑃∆𝑉𝑄=∆𝑈+𝑃∆𝑉Адиабатный. Количество теплоты, Q𝑄=0∆𝑈=−𝐴{BC89 EF96-8 CEA-46 FF-86 C4-4 CE0 E7609802}Название процесса. Постоянный параметр. Следствие постоянства параметра. Запись первого закона термодинамики. Изохорный. Объём, VИзотермический. Температура, ТИзобарный. Давление, РАдиабатный. Количество теплоты, QОсновные выводы24


про публікацію авторської розробки
Додати розробку