Розрахунковізадачі 1. Обчислення за хімічними рівняннями відносного виходу продукту реакції.
Обчислення за

 |
х м чними
 |

|
|
|
|
|
Засвоїти алгоритм розв'язування задач на обчислення за х м чними р вняннями в дносного виходу продукту реакц ї. |
||
|
|
|
|
|
Навчитися обчислювати за х м чними р вняннями в дносний вих д продукту реакц ї. |
Компетентност
 Предметн компетентност : учн обчислюють за х м чними р вняннями в дносний вих д продукту реакц ї, обґрунтовуючи обраний спос б розв’язання.
Предметн компетентност : учн обчислюють за х м чними р вняннями в дносний вих д продукту реакц ї, обґрунтовуючи обраний спос б розв’язання.
 Ключов компетентност : сп лкування державною мовою, математична компетентн сть, основн компетентност у
Ключов компетентност : сп лкування державною мовою, математична компетентн сть, основн компетентност у
природничих науках технолог ях, еколог чна грамотн сть здорове життя, ум ння вчитися упродовж усього життя.
Практично при проведенн будь-якого х м чного процесу в дбувається втрата деякої к лькост реагуючих речовин.
 Тому для одержання бажаної маси (чи об’єму)продукту реакц ї необх дно враховувати виробнич втрати, тобто розраховувати практичний вих д реакц ї , навпаки, за практичним виходом розраховувати маси (об’єми, к льк сть речовини) реагент в.
Тому для одержання бажаної маси (чи об’єму)продукту реакц ї необх дно враховувати виробнич втрати, тобто розраховувати практичний вих д реакц ї , навпаки, за практичним виходом розраховувати маси (об’єми, к льк сть речовини) реагент в.
Маси (об’єми) продукт в реакц ї, розрахован за р внянням реакц ї, називаються теоретичним виходом.
 Теоретичний вих д приймають за 100%, тому що одержати продукт в реакц ї б льше, н ж ця розрахункова величина неможливо.
Теоретичний вих д приймають за 100%, тому що одержати продукт в реакц ї б льше, н ж ця розрахункова величина неможливо.
 Маси (об’єми) продукт в реакц ї, обчислен з урахуванням втрат, називаються практичним виходом. Практичний вих д завжди менший за теоретичний.
Маси (об’єми) продукт в реакц ї, обчислен з урахуванням втрат, називаються практичним виходом. Практичний вих д завжди менший за теоретичний.
 Вих
Вихд продукту розраховують за формулою:
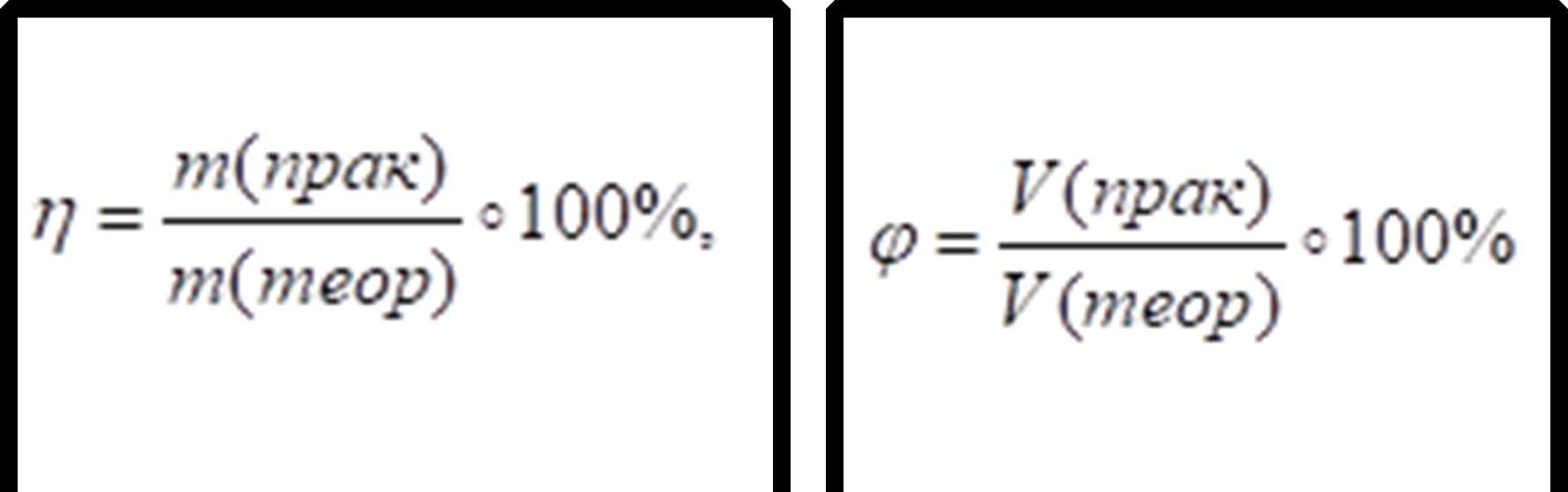
Чому бувають втрати?
Зд йснення будь-якоготехнолог чного процесу неможливе без певних втрат речовин.
Втратив дбуваються вже при транспортуванн сировини, її подр бненн , розчиненн , завантаженн в реактор.
Багатореакц й, як зд йснюють на х м чних заводах, є оборотними. Тому досягтиповногоперетворення вих дних речовин на ц льов продукти не вдається.
 Кр м того, нод водночас з основною реакц єю в дбувається нша (поб чна), частина реагент в витрачається на утворення сторонн х речовин.
Кр м того, нод водночас з основною реакц єю в дбувається нша (поб чна), частина реагент в витрачається на утворення сторонн х речовин.
Отже, продукту реакц ї завжди утворюється менше, н ж розраховано за х м чним р внянням.



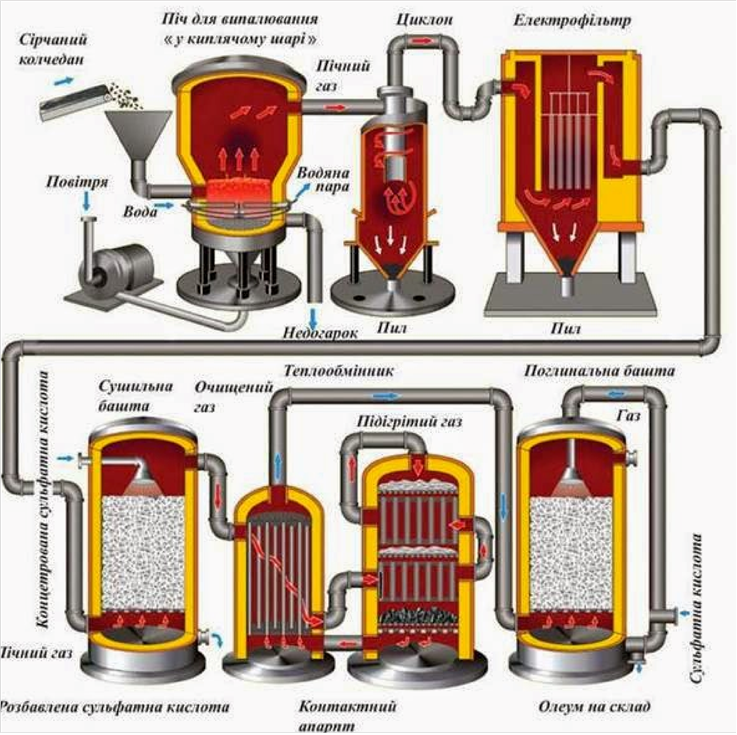 У технц головним способом добування амаку є прямий
У технц головним способом добування амаку є прямий
синтез його з азоту водню за реакцєю:
N2+3H2 2NH3
Розр зняємо два вихода продукту реакц ї:
Теоретичний вихд в дпов дає мас (m) або
об'єму (V) або к лькост речовини ( ), що знаходимо за
р внянням реакц ї. m(теор.) – маса
теоретичного виходу
V (теор.) – об’єм теоретичного виходу Практичний вихд— це маса або об'єм або
 к льк сть речовини, що отримують п д час виробництва. m(пр.) маса
к льк сть речовини, що отримують п д час виробництва. m(пр.) маса
практичного виходу
V (пр.) – об’єм практичного виходу
Вих д продукту реакц ї
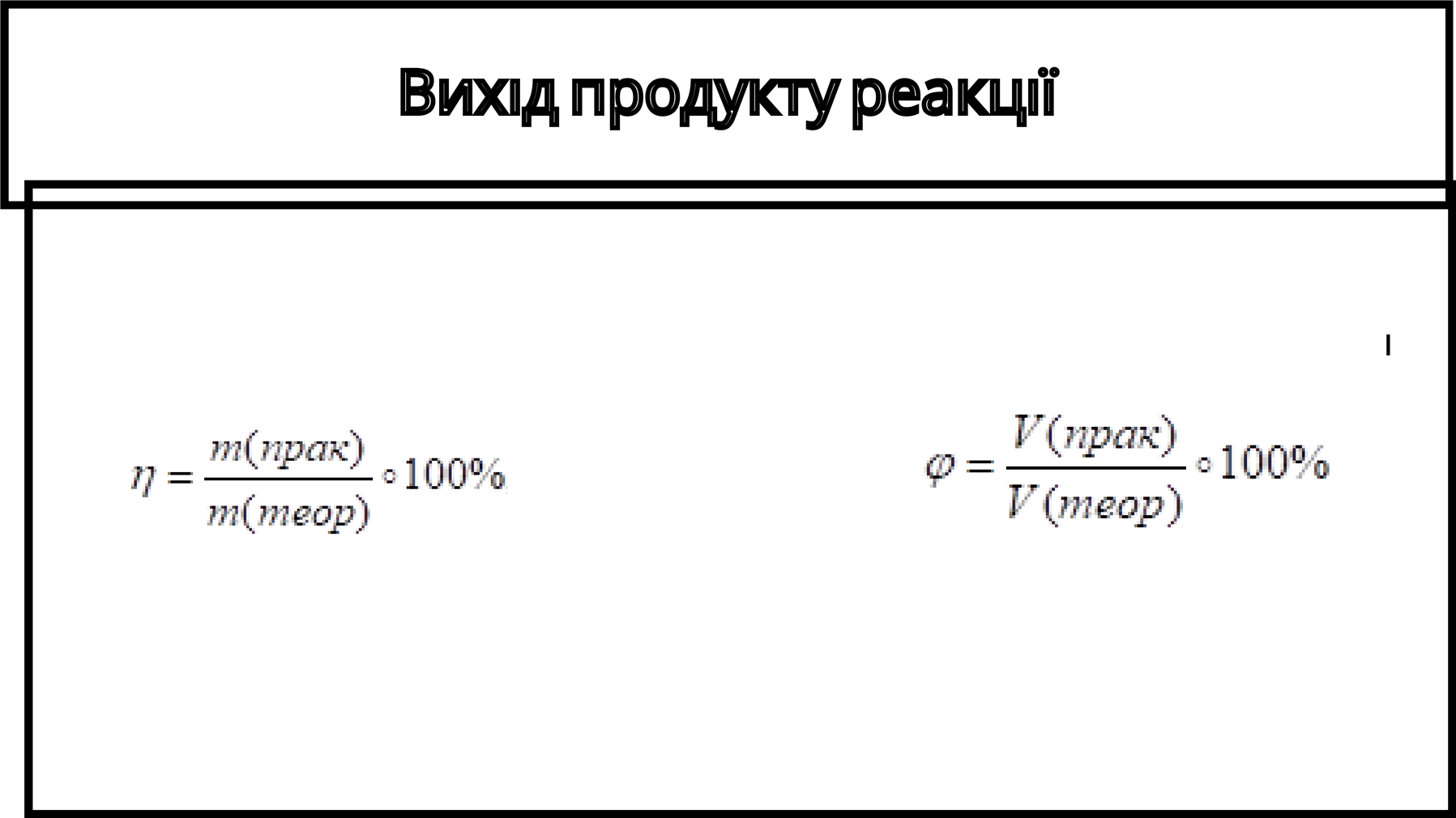 Величину, яка характеризує повноту переб гу х м чної реакц ї або ступ нь перетворення речовини на ншу, називають в дносним виходом продукту реакц ї. Цю величину позначають грецькою л терою η (ета) обчислюють за формулами:
Величину, яка характеризує повноту переб гу х м чної реакц ї або ступ нь перетворення речовини на ншу, називають в дносним виходом продукту реакц ї. Цю величину позначають грецькою л терою η (ета) обчислюють за формулами:
Вихд продукту — це в дношення реальної маси (об’єму чи к лькост речовини) продукту (практичний вих д) до теоретично
можливої, обчисленої за р внянням реакц ї (теоретичний вих д); виражається у в дсотках ( %) або частках одиниц .
 Алгоритм обчисл
Алгоритм обчислення виходу продукту реакц ї пор вняно з теоретично можливим
Порядок дій Приклади виконаних дй
1) Прочитайте текст Із негашеного вапна масою 112 г одержали
задач продукту вапно в д теоретично масою 120 можливогог. Обчисл ть. вих д гашене
Дано: 2) Запишіть скорочено m(СаО) = 112г
умову задачі mпрак(Са(ОН)2) = 120г
Знайти: η - ?
3) Запиш ть р вняння
реакц ї СаО + Н2О = Са(ОН)2
Алгоритм обчислення виходу продукту реакц ї пор вняно з теоретично можливим
Порядок дій Приклади виконаних дй
4) П дкресл ть формули речовин, про як йдеться в умов задач
СаО+ Н2О = Са(ОН)2
 5.Укажіть над підкресленими формулами вихідні кількості речовин, під формулами – дані, закономірні для рівняння реакції. Увага! По рівнянню реакції знаходять масу теоретичну!
5.Укажіть над підкресленими формулами вихідні кількості речовин, під формулами – дані, закономірні для рівняння реакції. Увага! По рівнянню реакції знаходять масу теоретичну!
112г х г
СаО +Н2О = Са(ОН)2
n = 1 моль n = 1 моль
М = 56 г/моль М = 74 г/моль
m = 56 г m = 74 г






 Дяку
Дякую за
 увагу
увагу

про публікацію авторської розробки
Додати розробку
