Самостійна робота до теми "Вуглеводні". 2 варіанти.
10 клас Тема. В У Г Л Е В О Д Н І
![]() Варіант 1 (1-16---0,5б.)
Варіант 1 (1-16---0,5б.)
1. Молекулярна формула пропану:
а) С3Н7; б) С3Н6; в) С3Н8; г) С5Н12.
2. Гомологи – це сполуки, що мають …
а) подібну будову молекул і різні хімічні властивості;
б) подібну будову молекул і подібні хімічні властивості;
в) однаковий якісний та кількісний склад;
г) містять однакову кількість атомів Карбону та Гідрогену.
3. Вкажіть хімічну формулу болотного газу:
а) СО; б) СО2; в) СН4; г) С2Н6;
4. Який насичений вуглеводень за нормальних умов є газом?
а) С6Н14; б) С7Н16; в) С10Н22; г) С3Н8.
5. Закінчіть рівняння реакції СН4 + О2 → … .
Вкажіть суму всіх коефіцієнтів.
а) 4; б) 5; в) 6; г) 7.
6. Вкажіть формулу радикалу етилу:
а) С4Н9; б) С2Н5; в) С3Н7; г) СН3.
7. Визначте відносну молекулярну масу алкану, молекула
якого містить 12 атомів Карбону:
а) 170; б) 168; в) 160; г) 150.
8. Яка речовина не реагує з метаном?
а) Cl2; б) О2; в) НСl; г) Br2.
9. Яка речовина належить до насичених вуглеводнів?
а) С3Н8; б) С3Н6; в) С3Н4; г) С6Н12.
10. Під яким кутом розміщуються валентні зв’язки в молекулах алканів?
а)104°; б) 107°; в) 108°; г) 109°.
11. Продуктами реакції горіння органічних речовин є …
а) вода і чадний газ; б) вуглекислий і чадний газ;
в) вуглекислий газ і вода; г) вода і метан.
12. До якого типу хімічних реакцій належить реакція метану з хлором?
а) обміну; б) сполучення; в) заміщення; г) розкладу.
13. Яка формула дихлороетану?
а) СН2Сl2; б) C2H2Cl2; в) C2H3Cl2 ; г) C2H4Cl2.
14. Яка валентність Карбону в органічних сполуках?
а) два; б) три; в) чотири; г) п’ять.
15. Вкажіть шостий член гомологічного ряду насичених вуглеводнів:
а) пентан; б) гептан; в) гексан; г) октан.
16. Вкажіть формулу насиченого вуглеводню, що містить 17 атомів Карбону:
а) С17Н34; б) С17Н35; в) С17Н36; г)С17Н30
17. Шляхом спалювання вуглеводню масою 8,6 г одержали 26,4 г
вуглекислого газ у та 12,6 г в оди. Густина вуглеводню за повітрям
дорівнює 2,966. Установіть формулу вуглеводню. (2 бали)
18. Напишіть рівняння реакцій, з допомогою яких можна здійснити такі
перетворення: (2 бали)
кальцій карбід → ацетилен → етилен → хлороетан → етилен
19. Напишіть рівняння реакцій, з допомогою я ких мо жна здійснити такі перетворення:
CH4 → CH3Cl → C2H6 → C2H5Br (2 бали)
20. Виведіть молекулярну формулу вуглеводню, який має відносну
молекулярну масу 78, якщо масова частка Карбону в ньому дорівнює 92,3 %? (2 бали)
21. Дайте назву органічним речовинам, за їх формулами
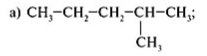
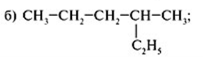 (1 бали)
(1 бали)
22. Оберіть під якими літерами розташовані ізомери:
а) СН3-СН2-СН2-СН2-СН3 в) СН3-СН2-СН2-СН3
![]()
![]() СН3 СН3
СН3 СН3
![]() б) СН3-СН-СН2-СН3 г) СН3 -С-СН3
б) СН3-СН-СН2-СН3 г) СН3 -С-СН3
СН3
(1 бали)
23. Поясніть, чому за рівних об’ємів етену й етину останній може
приєднати у два рази більше водню. (2 бали)

10 клас Тема. В У Г Л Е В О Д Н І
![]() Варіант 2 (1-16---0,5б.)
Варіант 2 (1-16---0,5б.)
1. Молекулярна формула бутану:
а) СН4; б) С4Н8; в) С3Н8; г) С4Н10.
2. Ізомерами називаються сполуки, що мають …
а) однакову молекулярну формулу, але різну будову та властивості;
б) однакову молекулярну формулу і будову, але різні властивості;
в) різні молекулярні формули, але подібні будову та властивості;
г) різні молекулярні формули і будову, але подібні властивості.
3. Яка формула рудникового газу?
а) С2Н6; б) СО2; в) СН4; г) С3Н6.
4. Який насичений вуглеводень за нормальних умов є рідиною?
а) СН4; б) С3Н8; в) С6Н14; г) С4Н10.
5. Закінчіть рівняння реакції С2Н6 + О2 → .. Вкажіть суму всіх коефіцієнтів.
а) 21; б) 19; в) 17; г) 14.
6. Вкажіть формулу радикалу пропілу:
а) СН3; б) С2Н5; в) С4Н9; г) С3Н7.
7. Визначте відносну молекулярну масу алкану, молекула якого
містить 10 атомів Карбону:
а) 142; б) 152; в) 130; г) 140.
8. Вкажіть речовину, яка не реагує з метаном:
а) Br2; б) KOH; в) O2; г) Cl2.
9. Вкажіть формулу насиченого вуглеводню:
а) С25Н50; б) С25Н51; в) С25Н52; г) С25Н48.
10. Молекула метану має форму …
а) куба; б) тетраедра; в) трикутника; г) октаедра.
11. При термічному розкладі етану утворюється …
а) чадний газ і водень; б) вуглекислий газ і водень;
в) вуглець і водень; г) вуглець і метан.
12. Метан не вступає в реакції …
а) окиснення; б) заміщення; в) приєднання; г) розкладу.
13. Яка речовина є хлорпохідною метану?
а) C3H6Cl3; б) CH3Cl; в) C2H4Cl2; г) CH2F2.
14. Яка загальна формула насичених вуглеводнів?
а) CnH2n; б) CnH2n-2; в) CnH2n+2; г) CnH2n-6.
15. Вкажіть дев’ятий член гомологічного ряду насичених вуглеводнів:
а) октан; б) декан; в) гексан; г) нонан.
16. Вкажіть формулу насиченого вуглеводню, що містит 18 атомів
Карбону:
а) С18Н40; б) С18Н34; в) С18Н38; г) С18Н36
17. Напишіть рівняння реакцій, з допомогою яких можна
здійснити такі перетворення: (2 бали)
CH4 → C2H6 → C2H5Cl → C2H4 → CO2
18. Напишіть рівняння реакцій, з допомогою яких можна здійсни-
ти такі перетворення: (2 бали)
етан → бромоетан → бутан → ізобутан → карбон(ІV) оксид.
19. Продуктами повного окиснення вуглеводню є карбон(IV) оксид
масою 26,4 г і вода масою 5,4 г. Відносна густина вуглеводню за
воднем дорівнює 39. (2 бали)
20. Масова частка Карбону у вуглеводні становить 83,33 %. Густина
парів вуглеводню за воднем дорівнює 36. Визначте формулу
вуглеводню. Скільки ізомерів він має? Напишіть структурні
формули цих ізомерів і назвіть їх. (2 бали)
21. Серед наведених нижче формул знайдіть структурні формули
гомологів н-бутану:
![]() а) CH2 – CH2 – CH3;
а) CH2 – CH2 – CH3;
CH3
б) CH3 – CH2 – CH2 – CH2 – CH3;
в) CH3 – CH3
г) CH2 = CH – CH2 – CH3; (1 бали)
22. Дайте назву органічним речовинам, за їх формулами
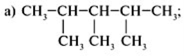
![]() (1 бали)
(1 бали)
23. Поясніть, чому за рівних об’ємів етену й етину останній може
приєднати у два рази більше водню. (2 бали)



про публікацію авторської розробки
Додати розробку
